Porušenie hemostázy. Vyčerpanie koagulačných faktorov. c) závažné poškodenie pečene

PATHOFYSIOLÓGIA SYSTÉMU HEMOSTÁZY
Hodnota hemostatického systému
1. uchovanie krvi v kvapalnom stave (primeraný pomer aktivity koagulačných a antikoagulačných systémov)
2. Zabráňte a zastavte krvácanie (udržiavanie konštantného objemu krvi v obehu)

TYPY HEMOSTÁZY
cievne doštičiek
(Počiatočné)
- ZASTAVENIE BLEEDING V MICRO SHIPS
koagulačné
(Sekundárne)
FORMÁCIA FIBRÍNOVÝCH ODPADOV

KOMPONENTY HEMOSTÁZOVÉHO SYSTÉMU
* VASKULÁRNA STEN
* krvné doštičky (monocyty, erytrocyty)
* PLASMOVÉ SYSTÉMY:
- PROKOAGULYANTY
- ANTIKOAGULANTY
- FIBRINOLYTIC
- KALLIKREIN-KININOVAYA

KLASIFIKÁCIA HEMOSTASOVÝCH PORÚCH
PRE etiológiu
- HEREDITÁR
- AKQUIRED
PRE ROZVOJOVÝ MECHANIZMUS
- VASKULÁRNE PORUCHY
hemostáza
- ZLYHANIE KOAGULATÓRNEJ HEMOSTÁZY
PRE SMERU ZMIEN
- HYPOCOAGULÁCIA
- HYPERKAGULÁCIA

gipokoagulyatsii
Znížená schopnosť krvných zrazenín s tendenciou k opätovnému krvácaniu a krvácaniu (spontánne alebo po malých úrazoch)

etiológie
1. TROMBOCYTOPIA
2. trombocytopatia
3. VASOPATHY
4. KOAGULOPATIA

trombocytopénia
Patologický stav charakterizovaný znížením počtu krvných doštičiek. (menej ako 150 · 109 / l)

HEREDITÁRNA TROMBOCYTOPÉNIA
Spravidla je súčasne sprevádzané abnormálnymi defektmi doštičiek

AKTUÁLNA TROMBOCYTOPÉNIA (KLASIFIKÁCIA V RÁMCI ROZVOJOVÉHO MECHANIZMU)
POŠKODENIE PLATELETOV
- imunitné komplexy
- mechanická trauma (splenomegália, hemangióm)
UPLOčENÉ TROMBOCYTOVÉ VZDELÁVANIE
(aplastická anémia, chemické a radiačné poškodenie červenej kostnej drene, náhrada hematopoetického tkaniva nádorom)
ZVÝŠENÉ POUŽITIE PLATELETOV
(trombóza, DIC)

Imúnna trombocytopénia
GETEROIMMUNNAYA
* Vyskytuje sa častejšie v deti
** dôvod - zmeny v antigénnej štruktúre krvných doštičiek (počas poklesu rubeoly, kiahní, adenovírusových vírusov, haptínov získaných z liečiv - chinidínu, sulfónamidov, rifampicínu, vakcín)
***Priaznivý kurz (ak je príčina odstránená, dôjde k úplnej regenerácii)

Imúnna trombocytopénia
autoimunitné
Vyskytuje sa častejšie dospelí
dôvod - nedostatok imunitnej tolerancie voči antigénom vlastných krvných doštičiek
Provokatívne faktory: drogy, vírusy, baktérie

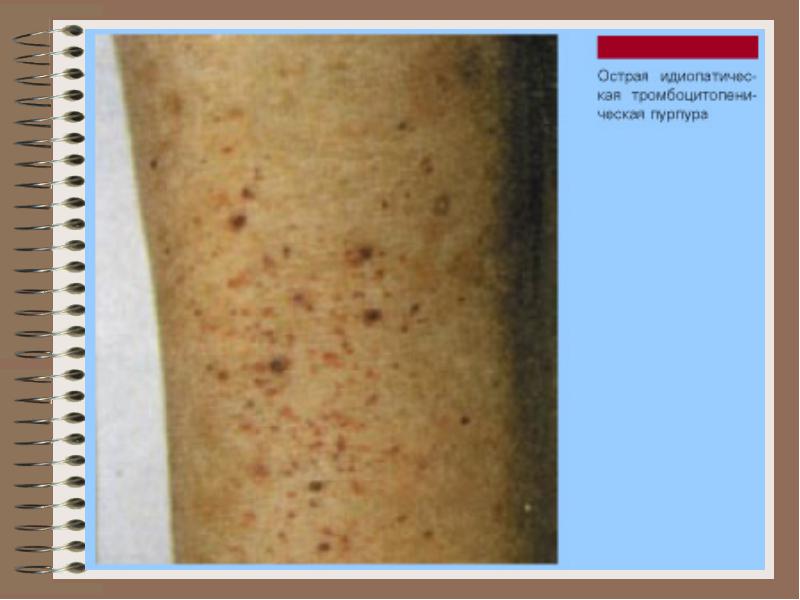
Autoimunitná trombocytopénia
VERLEHOPÁLNA CHOROBA
(autoimunitná chronická trombocytopenická purpura)
* Na počítanie povrchu trombocytov IgG sa zvyšuje 10 krát
* Hlavným miestom syntézy Ig G je slezina
* Princip liečby:
- splenektómia
- kortikosteroidy
- imunosupresíva
* Neexistuje úplná liečba.

thrombocytopathy
Zhoršená hemostáza v dôsledku kvalitatívnej inferiority alebo dysfunkcie krvných doštičiek, ktorá je charakterizovaná porušením hemostázy krvných doštičiek, výskytom krvácania tkanív a orgánov

BEZ PORUŠENIA REAKCIE LIBERÁCIE GRANULOV
Glantsman trombasténia
* Dedičstvo - autozomálne recesívne
*dôvod - neprítomnosť glykoproteínov 2b a 3a v plášti krvných doštičiek
*patogenézy- krvné doštičky neovplyvňujú fibrinogén a neagregujú
*príznaky: petechie, krvácanie z nosa, krvácanie z maternice ( môže byť smrteľné!)

Dedičná trombocytopatia
S PORUŠENÍM REAKCIE LIBERÁCIE GRANULOV
dedičstvo - autozomálne recesívne
dôvod - znížená aktivita cykloxygenázy, nízka aktivita kontraktilných proteínov
patogenézy - nedostatok agregácie pri interakcii s kolagénom, nedostatok uvoľňovania granúl
príznaky:

Dedičná trombocytopatia
S PORUŠENÍM A UVOĽNENÍM OBSAHU GRANULOV
Herjman Pudlakova choroba (AR)
* dôvod - porušenie hromadenia hustých granúl (ADP, adrenalín, serotonín, Ca2 +),
* patogenézy - v interakcii s kolagénom nedochádza k agregácii, nedochádza k uvoľneniu obsahu granúl
* príznaky: petechie, krvácanie z nosa, krvácanie z maternice

Dedičná trombocytopatia
S DÔSLEDKOU ZARIADENIA ZLÚČENIA A ZOSTAVY
Von Willebrand-Jurgensov syndróm (AR)
dôvod - nedostatok faktora Willebrand
patogenézy - zhoršenie adhézie krvných doštičiek v dôsledku nedostatku faktora 8
Bernard Sulova choroba (AR)
dôvod - nedostatok glykoproteínu 1 na krvných doštičkách
patogenézy - interakcia krvných doštičiek s von Willebrandovým faktorom, f. 5, f. 11
Znaky - krvácanie z kapilár ( najmä počas puberty alebo pri pôrode)

Dedičná trombocytopatia
NEDOSTATOK A ZNÍŽENÁ DOSTUPNOSŤ f.3
Trombocytopatia Bowe a Aries
dôvod - nedostatok f.3 krvných doštičiek
patogenézy - neexistuje žiadna interakcia medzi krvnými doštičkami a prokoagulantmi
príznaky: petechie, krvácanie z nosa, krvácanie z maternice

Dedičná trombocytopatia
Trombocytopatia v kombinácii s inými dedičnými anomáliami
Whiskott-Aldridgeov syndróm
- dôvod - v krvných doštičkách je niekoľko hustých granúl (ADP, serotonín, adrenalín, Ca2 +), alfa granule (beta-tromboglobulín, fibrinogén, fibronektín, rastový faktor)
- patogenézy - Zhoršená adhézia a agregácia trombocytov, zhoršenie uvoľňovania granúl
- príznaky:hemoragický syndróm nastáva skoro, môže dôjsť k smrteľnému krvácaniu

Získaná trombocytopatia (etiológia)
1. leukémie- málo granúl v krvných doštičkách spôsobených zrýchlenou maturáciou, zníženou adhéziou a agregáciou
2. NahromaďteIg M - poškodenie receptorov imunitnými komplexmi, porušenie interakcie krvných doštičiek s prokoagulantmi (imunitné ochorenia)
3. hypovitaminóza B12 - uvoľnenie granúl narušené
4. Účinky liekov

Liečivá trombocytopatia
* A inhibítory syntézy tromboxánu A2
steroidné protizápalové lieky
- nesteroidné protizápalové lieky (aspirín blokuje agregáciu trombocytov počas 4-6 dní)
* Stimulátory vzdelávania cAMP
-papaverin
- eufylín
-abolické steroidy
* Antagonistov Ca-iónov
-verapamil
-korinfar

VAZOPATIYA
Hemoragická diatéza v dôsledku funkčného a morfologického nedostatku cievnej steny
- vrodené
- získané

HORNÁ VASOPATÉDA
Bol. Randyu-Osler (hemoragická telangiektázia)
Bol. Fabry (difúzny angiokeróm trupu)
Dedičná trombocytopenická mikroangiomatóza

HORNÁ VASOPATÉDA
dôvod - dedičná porucha vývoja spojivového tkaniva, vrátane vaskulárne subendotelium
vlastnosť
- ohniskové cievne zriedenie
- rozšírenie lumen mikrovesselov
- malé kolagénové vlákna v subendoteli
- plavidlá sú ľahko zranené
- slabá priľnavosť a agregácia krvných doštičiek v dôsledku nedostatku kolagénových vlákien
**Znaky - nazálne, pľúcne-bronchiálne a gastrointestinálne krvácanie (sú fatálne)

ZÍSKANÁ VASOPATÉDA
1. A diopaticheskaya (Kaposiho sarkóm)
- etiológia - neznáma
2. stagnujúci (dermatitída Klotza, dermatitída Favra Rakusho)
- etiológia - chronické srdcové zlyhanie, lokálna venózna insuficiencia
3. dystrofné
Steroidná purpura - hyperfunkcia nadobličiek, liečba kortikosteroidmi - inhibujú syntézu kolagénu
Zhoršovanie - nedostatok Vit.S
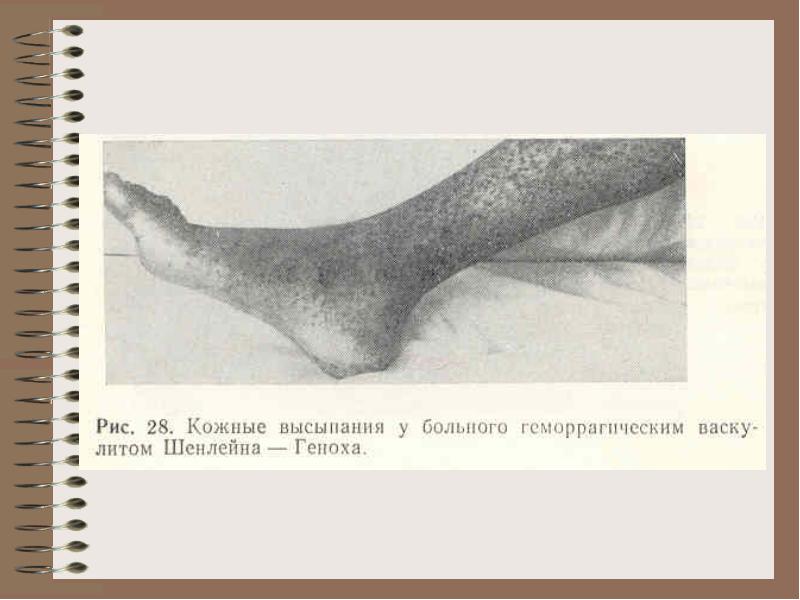
Bol.Shenlein-Genokha - vaskulárne poškodenie imunitných komplexov
4. neurogénna
Klinické príznaky - krvácanie kože

koagulopatie
Hemoragická diatéza, ktorá sa vyskytuje v dôsledku patológie koagulačného systému hemostázy
** dedičný
** získané

Dedičná koagulopatia
Geneticky spôsobená koagulačná porucha spôsobená nedostatkom alebo molekulárnou abnormalitou látok zodpovedných za koagulačnú hemostázu

Dedičná koagulopatia
Klasifikácia
1. Koagulopatia spôsobená izolovaným narušením vnútorného mechanizmu tvorby protrombinázovej aktivity (hemofília A, B, C, Willebrand b., Hagemanova nedostatočnosť)
2. Koagulopatia spôsobená izolovaným porušením externého mechanizmu tvorby protrombinázovej aktivity (hypoprokonvertinémia - nedostatok 7 l)
3. Kombinované porušenie vonkajšieho a vnútorného mechanizmu tvorby protrombinázovej aktivity (parahemofília - nedostatok 5 libier, b.Steuart-Prouer - nedostatok 10 libier)
4. porušenie konečného štádia koagulácie krvi (afibrinogénia)

ŠTATISTIKA
Medzi všetkými formami koagulopatie trpia:
Hemofília A 68 - 78%
B , Willebrand 9 - 18%
Hemofília B 6 - 13%
Hemofília C, parahemofília a hypoprokonvertinémia 1 - 2%
Zostávajúce formy - klinická kazuistika

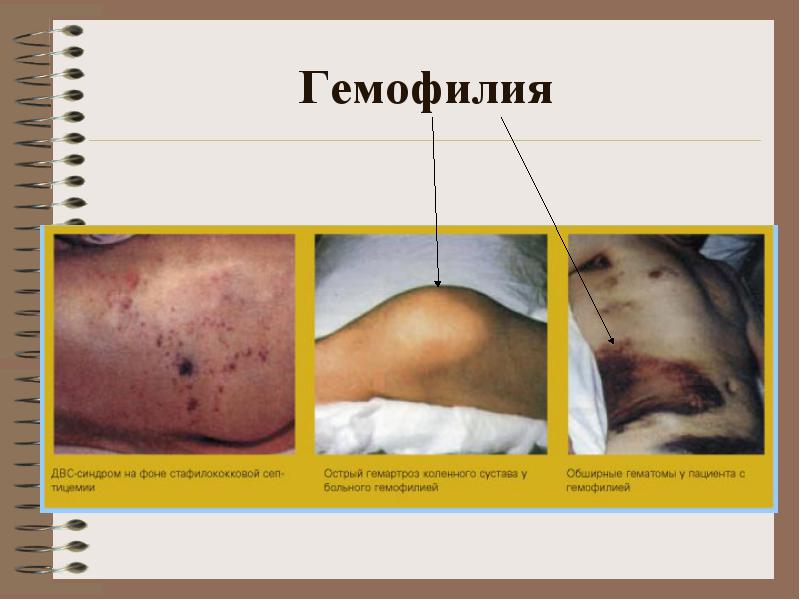
Hemofília A
Hemoragická diatéza v dôsledku dedičnej nedostatočnosti prokoagulačnej časti faktora 8
Faktor 8 (proteín s vysokou molekulovou hmotnosťou)
1. Prokoagulant glykoproteínu (VIII: K)
2. Glykoproteín, ktorý vykonáva adhéziu krvných doštičiek (VIII: FV)
3. Glykoproteín, ktorý aktivuje adhéziu krvných doštičiek pod vplyvom ristomycínu (VIII: Rkoff)
4. Antigénny marker VIII: K (VIII: K AG)
5. Antigénny marker VIII: Rkof (VIII: Rkof AG)
Aktivita VIII: K a VIII: PV klesá s klesajúcou multimerickou štruktúrou a iba 8 faktormi

Hemofília A
* Uh tiologiya - génová abnormalita v chromozóme X, ktorá riadi syntézu prokoagulačná časť f. 8 (Viii: k)
** III - muži (46, XhY)
** typy
- Syntéza hemofílie A + (antigén-pozitívna forma - anomálna) VIII: K), 8 - 10% trpí
- hemofília A- (antigén-negatívna forma - nie je syntetizovaná VIII: K), Trpí 90-92%
**** poradňa: krvácanie vo veľkých kĺboch, hematómy (subkutánne, intramuskulárne), závažné a dlhotrvajúce post-traumatické krvácanie. Možné krvácanie do brušných orgánov, gastrointestinálne krvácanie

hemofílie
hemofílie
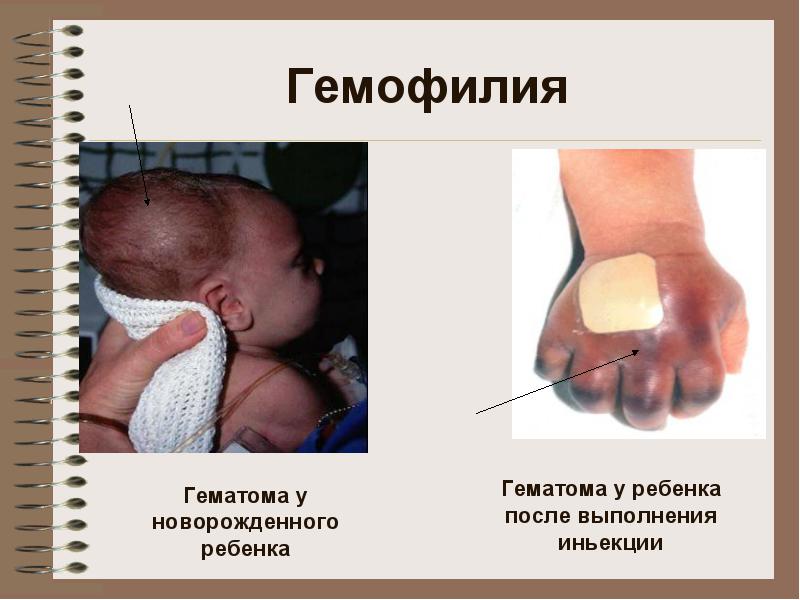
Hemofília B
etiológie - génová anomália v chromozóme X, ktorý riadi syntézu f. 9
Chorí muži (46, XhY)
- ženy (46, XhXh), (45, XhO)
*** Zobrazenia
- Syntéza hemofílie B + (antigén pozitívna forma - anomálna) f. 9)
- hemofília B- (antigén-negatívna forma - nie je syntetizovaná f. 9)
poradňa: krvácanie vo veľkých kĺboch, hematómy (subkutánne, intramuskulárne), závažné a dlhotrvajúce post-traumatické krvácanie. Možné krvácanie do brušných orgánov, gastrointestinálne krvácanie

ZÍSKANÁ KOAGULOPATIA
vlastnosť - polydeficient
etiológie
1. Imunná inhibícia prokoagulantov (konflikt rhesus)
2. Nedostatok vit. K-koagulačné faktory (7, 10, 9, 2)
a) narušená syntéza v črevách (dysbakterióza, hnačka)
b) porušenie absorpcie vit. K (nedostatok žlče)
c) závažné poškodenie pečene
3. Predávkovanie heparínom

hyper koaguláciu
ZVÝŠENÁ KAPACITA KRVY, KTORÁ ZAČNETE BUNCH V PLAVIDLÁCH
trombóza
DIC

DIC-SYNDRÓM (SYNDRÓM ROZSIABENEJ VNÚROVASKULÁRNEJ KOAGULÁCIE KRVI)
Klasifikácia
* Podľa klinického priebehu
1) akútne (okamžité formy sú charakterizované ťažkým priebehom)
2) chronické
* Podľa prevalencie
1) lokalizované
2) všeobecné

etiológie
Infekcie, septické stavy
otras (so septikom - úmrtnosť 100%)
Chirurgické intervencie, popáleniny
Všetky podmienky terminálu, zastavenie srdca
Akútna intravaskulárna hemolýza
Obstetrálna patológia (20-25%)
Hemoblastóza (s leukémiou - 33-45%)
Deštruktívne procesy v parenchýmových orgánoch
Alergické reakcie

Etapy DIC
1) Hyperkoagulácia (tvorba viacerých krvných zrazenín v dôsledku aktivácie koagulačného systému)
2) konzumná koagulopatia (vyčerpanie koagulačného systému, nadmerné používanie krvných doštičiek na tvorbu krvných zrazenín)
3) Hypokoagulácia (zníženie aktivity koagulantov, aktivácia antikoagulancií, aktivácia fibrinolýzy)
4) Dokončenie (zotavenie, komplikácie, smrť)

Patogenéza DIC
1) hyperthrombinemia (tromboplastín vstupuje do krvi vo veľkom množstve z poškodených tkanív a podporuje tvorbu trombínu). Pri infekciách aktivované makrofágové monocyty syntetizujú svoje vlastné koagulanty (f.7, f.10, f.9, f.2)

Patogenéza DIC
2) Masívna agregácia doštičiek (spôsobuje vývoj konzumácie trombocytopénie a komplikuje krvácanie)
3) Trauma a hemolýza erytrocytov (produkuje veľa ADP, čo zvyšuje adhéziu a agregáciu krvných doštičiek)

Patogenéza DIC
4) "Výbuch humorálnej proteázy" (pri aktivácii prokoagulantov, antikoagulantov, fibrinolitických látok, proteínov systému kalikreín-kinín, systému komplementu v krvi, sa hromadia mnohé produkty rozpadu proteínov, ktoré sú veľmi jedovaté a poškodzujú cievy a tkanivá)

Patogenéza DIC
5) Vyčerpanie systému prenájmu fibrín
(prispieva k trombóze)
6) Vyčerpanie koagulačných faktorov krvi
(spôsobujú vznik krvácania)

Klinika DIC
1. Hemokoagulačný šok
dôvod
* porušenie mikrocirkulácie (spôsobuje vývoj hypoxie tkaniva)
* akumulácia toxických produktov proteolýzy
prejavy
zníženie krvného tlaku
* zníženie centrálneho venózneho tlaku
* krvácanie (vyvolanie hemoragického šoku)

Klinika DIC
2. Hemostatické poruchy
a) hyperkoagulácia
Hlavným prejavom je trombóza.
Krv koaguluje in vitro
b) hypocoagulation
Hlavným prejavom je krvácanie
(zároveň je vyčerpaný systém fibrinolýzy)

Klinika DIC
3. trombocytopénia
Vyskytuje sa v dôsledku tvorby veľkého množstva krvných zrazenín v cievach (konzumácia trombocytopénie)

Do tejto skupiny patria geneticky determinované hypokoagulácie, ktoré sa vyznačujú nedostatkom, ako aj molekulárnymi abnormalitami koagulačných faktorov krvi.
Takže 83-90% všetkých hereditárnych krvácavých porúch je 2 typy faktorov nedostatočnosti VTII hemofílie A (70-78%) a von Willebrandovej choroby (9-18%); ďalších 6 až 13% je spojených s nedostatkom faktora IX (hemofília B). Deficit len dvoch koagulačných faktorov - VIII a IX - predstavuje asi 96-98% všetkých dedičných koagulopatií. Deficit faktorov VII a V je zaznamenaný v 0,5-1,5% faktora X - v 0,3-0,5% prípadov.
Nie všetky porušenia v systéme zrážania krvi sú sprevádzané krvácaním: môžu byť neprítomné alebo mierne.
Hemofília A. Toto ochorenie je najčastejšou koagulopatiou, ktorá je založená na nedostatku faktora VIII (antihemofilný globulín) a je jediná z nich s recesívnym X-chromozomálnym dedičstvom.
Rozmanitosť foriem patológie faktora VIII odzrkadľuje zložitosť jeho štruktúry. V krvi cirkuluje faktor VIII vo forme proteínového komplexu pozostávajúceho z množstva podobných podjednotiek.
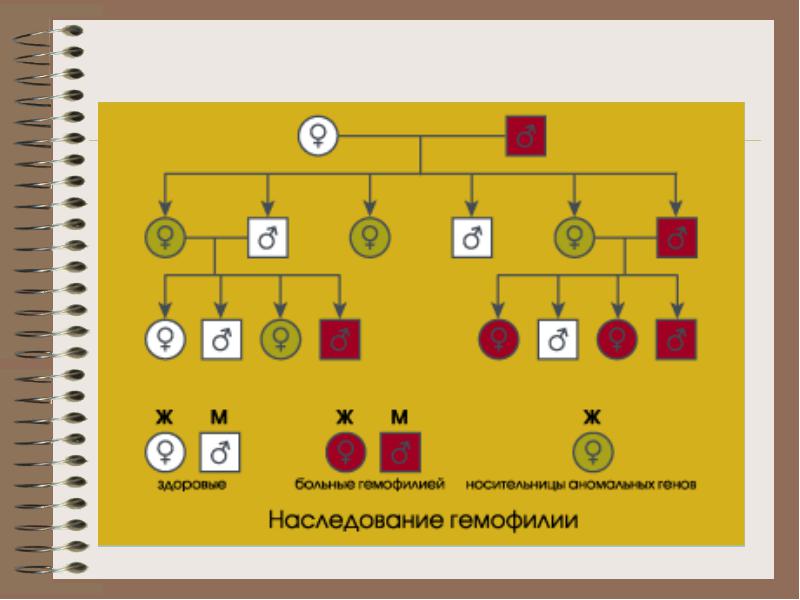
dedičstvo. Gén hemofílie, ktorý sa nachádza v chromozóme X, je zdedený chorým človekom všetkými jeho dcérami, ktorí neskôr nevyhnutne nesú chorobu, zatiaľ čo synovia pacienta zostanú zdraví (kvôli tomu, že získajú X chromozóm zo zdravého matky).
Treba tiež poznamenať, že žena nosiča hemofílie má v 50% prípadov možnosť zrodiť zdravého syna a polovica dcér sa stane nosičom hemofilického génu.
Ženské nosiče spravidla netrpia krvácaním, pretože druhý normálny X chromozóm poskytuje syntézu faktora VIII, ktorý vo väčšine prípadov postačuje na zabezpečenie hemostázy.
Rýchlosť faktora VIII sa však mení vo veľmi veľkých medziach (60-250%). Z tohto hľadiska môže byť u niektorých vysielačov hladina faktora VIII v plazme 11-20%, čo vytvára riziko krvácania z poranení, operácií a pôrodu. Lekár by si mal pamätať na toto nebezpečenstvo počas chirurgických zákrokov u matky, sestry a najmä dcéry pacientov s hemofíliou. Pred chirurgickým zákrokom a pred pôrodom by mali kontrolovať hladinu faktora VIII v plazme a pri dávkach pod 25% profylakticky podávať kryoprecipitát v dávke 7-10 U / kg denne.
Detekcia nosiča génu pre hemofíliu je uľahčená podrobnou štúdiou familiárnej hemoragickej anamnézy vo všetkých príbuzných krvi matky.
V hemofílii A sa vyskytuje dedičná genetická príhoda v 70-75% prípadov a u hemofílie B - u 90-91%. Gén hemofílie A nepochybne často mutuje, pretože počet pacientov sa po mnoho storočí nezmenšil, hoci až donedávna značná časť z nich zomrela pred dosiahnutím plodu, čo viedlo k prirodzenému poklesu abnormálnych X chromozómov.
Symptómy porúch koagulačnej hemostázy
Závažnosť krvácania závisí od nedostatku faktora VIII v plazme, ktorého obsah je v rôznych hemofilných rodinách geneticky naprogramovaný.
Úroveň faktorov s jasným hemofilným účinkom (VIII alebo IX) v rozmedzí od 0 do 1% spôsobuje mimoriadne závažný priebeh posudzovanej patológie, úroveň faktorov od 1 do 2% spôsobuje vážne, od 2 do 5% mierneho a viac ako 5% ľahký priebeh ochorenia. V druhom prípade existuje pravdepodobnosť krvácania, čo predstavuje vážne nebezpečenstvo pre život pacienta, čo je mimoriadne dôležité pri vykonávaní rôznych chirurgických zákrokov alebo v prípade poranenia.
Klinický obraz hemofílie dominuje krvácanie vo veľkých kĺboch končatín, hlboké subkutánne, intermuskulárne a intramuskulárne hematómy, ťažké a dlhotrvajúce krvácanie so zraneniami, hematúria (výskyt krvi v moči). Ďalšie krvácanie sa pozoruje menej často, vrátane ťažkých a nebezpečných, ako sú retroperitoneálne hematómy, hemorágie v brušných orgánoch, gastrointestinálne krvácanie a intrakraniálne krvácanie.
Existuje jasný vekový vývoj prejavov ochorenia. Pri narodení sa môžu pozorovať viac alebo menej rozsiahle cefalematómy (krvácanie pod periosteom kostí lebky), subkutánne a intradermálne krvácanie, neskoré krvácanie z pupočníka. Niekedy sa choroba objaví počas prvej intramuskulárnej injekcie, čo môže spôsobiť veľký, život ohrozujúci intermuskulárny hematóm. Dojčenie často sprevádza nie veľmi ťažké krvácanie.
V prvých rokoch života sa často vyskytuje krvácanie zo sliznice ústnej dutiny, spojené s poškodením rôznymi ostrými predmetmi. Keď sa dieťa učí chodiť, pády a modriny sú často sprevádzané hromadeným nazálnym krvácaním a hematómami na hlave, krvácaním v očnej objímke a tiež následnými orbitálnymi hematómami, ktoré môžu viesť k strate zraku. Dieťa začalo plaziť, typické krvácanie v oblasti hýždia.
Potom sa dostanete do popredia krvácanie vo veľkých kĺbov končatín. Akútne hemorágie v kĺboch sa objavujú skôr, tým závažnejšia hemofília. Prvé krvácanie predisponuje k opakovaniu v tých istých kĺboch. U každého pacienta s osobitnou pretrvávajúcou a frekvenciou je postihnuté krvácanie kĺbov I - III. Je to spôsobené morfologickou reštrukturalizáciou a sekundárnymi zápalovými zmenami v tkanivách kĺbu.
Bolo zistené, že synoviálna membrána je hlavným a pravdepodobne jediným zdrojom krvácania do kĺbu, pretože po úplnej synovektómii (odstránenie synoviálnej membrány) sú také krvácania opakujúce sa a nevracejú sa. Najčastejšie postihnuté kolenné kĺby, po ktorom nasleduje členok a lak, a potom s výrazným poklesom bedier. Krvácania v malých kĺboch rúk a nôh (menej ako 1% všetkých lézií) a medzistavcové kĺby sú relatívne zriedkavo pozorované. V závislosti od veku a závažnosti ochorenia je každý pacient postihnutý kĺbmi I - II až VIII - XII.
Klinicky je dôležité rozlíšiť akútne krvácanie v kĺboch (primárne a opakujúce sa), chronickú hemoragicky destruktívnu osteoartrózu (artropatie), sekundárny imunitný reumatoidný syndróm ako komplikáciu hlavného procesu.
Akútna hemartróza - náhly vzhľad (často po malom poranení) alebo prudké zvýšenie bolesti v kĺbe. Koža kĺbu je červená a horúca na dotyk. Bolesť sa rýchlo (v priebehu niekoľkých hodín) uvoľní po prvej transfúzii kryoprecipitátu alebo antihemofilnej plazmy a takmer okamžite zmizne pri súčasnom odstránení krvi z kĺbu. Ak nie je bolestivý syndróm s touto liečbou vylúčený, potom by sa mala vyhľadávať ďalšia patológia - intraartikulárna zlomenina, roztrhnutie kondylu, väzba tkaniva.
Osteoartróza je rozdelená na štádiá založené na klinických a rádiologických údajoch. Pri klasifikácii sa rozlišujú 4 stupne poškodenia kĺbov.
V I. alebo v skorom štádiu môže byť zväčšený objem spoja (s rozšírením kĺbového priestoru) v dôsledku krvácania. V "chladnom" období nie je funkcia kĺbov narušená, ale radiograficky sa môže zistiť zahustenie a zhrubnutie kĺbovej kapsuly v dôsledku infiltrácie hemosiderínom.
V štádiu II sa odhalili typické zmeny segmentu subkarpusu epifýz - okrajové vzory, tvorba jediného oválneho malého bunkového poškodenia a cysty. Osteoporóza je výraznejšia, kĺbová medzera sa zachová, ale môže byť mierne zúžená.
V štádiu III je kĺb prudko zväčšený, deformovaný, má nerovnomernú a nerovnomernú štruktúru a určuje výrazné strate svalov. Mobilita postihnutých kĺbov je viac-menej obmedzená kvôli poškodeniu samotného kĺbu a zmenám svalov a šliach. Radiograficky sú kĺby zahustené, ostré deformované, kĺbové povrchy sú sploštené, epifýzy sú zväčšené kvôli rastu kostného tkaniva, diafýza je znížená, medzera kĺbov je zúžená. Osteoporóza je vyslovená, intraartikulárne zlomeniny sa vyskytujú ľahko. Vo stehennej kosti je pre hemofíliu charakteristická kráterová alebo tunelovitá deštrukcia kostnej substancie v oblasti medzilodonosnej fossy. Patella je čiastočne zničená. Intra-artikulárna chrupavka je zničená, pohyblivé, často rozdelené fragmenty týchto chrupaviek, často zakotvené v starých organizovaných krvných zrazeninách, sa nachádzajú v kĺbe dutiny. Existujú rôzne typy subluxácie a posunutia kostí.
V štádiu IV je funkcia kĺbu takmer úplne stratená, kĺbový priestor je zúžený, zle zobrazený na snímke a často zarastený spojivovým tkanivom. Skleróza perineálnych častí kosti sa vyslovuje v kombinácii s tvorbou trhlín a tvorbou cystov v epifýzach. Možné patologické intraartikulárne zlomeniny. Kostná ankylóza je extrémne zriedkavá a v skutočnosti sa nikdy nepozorovala, pokiaľ v minulosti nedošlo k nesprávnej liečbe (s predĺženou imobilizáciou končatiny).
S vekom závažnosť a prevalencia kĺbových lézií neustále rastie a sú zhoršené výskytom periartikulárnych hematómov.
Sekundárny reumatoidný syndróm (Barkaganov syndróm - Egorova), prvýkrát opísaný autormi v roku 1969, je bežnou formou poškodenia kĺbov u pacientov s hemofíliou. V mnohých prípadoch je to vidieť, pretože je vrstvené na predchádzajúcich krvácaní v kĺboch a deštruktívnych procesoch v kĺboch, ktoré sú vlastné hemofílii. Starostlivé vyšetrenie pacientov uľahčuje diagnostiku sekundárneho reumatoidného syndrómu, ktorý je nevyhnutný pre ďalšiu správnu liečbu. Tento syndróm je sprevádzaný chronickým zápalovým procesom (často symetrickým) v malých kĺboch rúk a nôh, ktoré neboli predtým ovplyvnené krvácaním, s následnou typickou deformáciou, bolesťou v veľkých kĺboch, ktoré sa nezastavujú a často sa zhoršujú po plazmatických transfúziách a injekciách kryoprecipitátu. Tento syndróm sa vyskytuje aj s výraznou rannou tuhosťou v kĺboch, neustálym priebehom kĺbového procesu z kontaktu s čerstvými hemoragiami, vzhľadom alebo ostrým zvýšením laboratórnych príznakov zápalového procesu, vrátane imunologických, s nárastom sérových globulínov, sialových kyselín, fibrinogénu, zvýšenie koncentrácie cirkulujúcich imunitných komplexov a v niektorých prípadoch aj titre reumatoidného faktora. U väčšiny pacientov sa syndróm objavuje vo veku 10-14 rokov, vo veku 20 rokov jeho frekvencia dosahuje 5,9% a 30 rokov - na 13%.
Vzhľadom na vek sa výskyt a závažnosť všetkých lézií kĺbov neustále vyvíja, čo vedie k postihnutiu a prinúti pacientov, aby používali barle, invalidné vozíky a iné zariadenia.
Progresie poškodenia kĺbov je závislá na frekvencii akútne krvácanie do kĺbov, včasnosti a užitočnosti ich spracovanie (do začiatku transfúziu krvi veľmi dôležité), kvalitné ortopedickú starostlivosť pacientovi, vhodné využitie fyzikálnej terapie, rehabilitácia ovplyvňuje voľbu povolania a rad ďalších okolností. V súčasnosti sú všetky tieto otázky mimoriadne relevantné, pretože očakávaná dĺžka života pacientov s hemofíliou v dôsledku úspechu nápravnej liečby sa dramaticky zvýšila.
Nasledujúce typy rozsiahlych a namáhaných hematómov sú pre pacienta dosť ťažké a nebezpečné: subkutánne, intermuskulárne, subfazické a retroperitoneálne. Postupne sa zvyšujú, môžu dosiahnuť obrovské rozmery, obsahujú 0,5 až 3 litre krvi a viac, vedú k vzniku anémie u pacientov, spôsobujú kompresiu (kompresiu) a deštrukciu (zničenie) okolitých tkanív a ciev, ktoré ich kŕmia, nekrózu. Napríklad retroperitoneálne hematómy často úplne zničia veľké oblasti panvových kostí (priemer zóny deštrukcie je až 15 cm alebo viac), hematómy na nohách a ramenách zničia trubicovité kosti a pätu. Smrť kostného tkaniva tiež spôsobuje krvácanie pod periostom. Táto deštrukcia kostí na rádiografoch je podobná deštrukcii nádoru (napríklad pri osteosarkómoch). Hematómy sú často kalcifikované a niekedy vedú k tvorbe nových kostí (osteoneogenéza). Môžu uzavrieť kĺby a úplne ich imobilizovať.
Mnoho hematómov, ktoré vyvíjajú tlak na nervové kmeň a svaly, spôsobujú paralýzu, zhoršenú pohyblivosť, citlivosť, rýchlo progresívnu svalovú atrofiu. Pri krvácaní v oblasti iliopsoas svalov sú charakteristické najmä ohybové pohyby stehna. Zvláštna pozornosť sa venuje tým hematómom, ktoré môžu spôsobiť rozvoj stenózy horných dýchacích ciest. Takéto hematómy zahŕňajú hematómy mäkkých tkanív submandibulárnej oblasti, hematómy krku, hltanu a hltanu.
U 14 až 30% všetkých pacientov s hemofíliou sa objavuje hojné a dlhotrvajúce krvácanie obličiek, ktoré vážne ohrozuje život pacienta a je ťažké liečiť. Toto krvácanie sa môže vyskytnúť spontánne aj v súvislosti s poraneniami bedrovej oblasti spojenej s pyelonefritídou a pravdepodobne v dôsledku zvýšenej exkrécie vápnika v moči spôsobenej deštrukciou kostného tkaniva u pacientov s hemofíliou. Analgetiká (kyselina acetylsalicylová atď.), Hojné transfúzie krvi a plazmy vedúce k rozvoju sekundárnej trombocytopatie v dôsledku dodatočného negatívneho účinku na obličky môžu prispieť k objaveniu alebo zvýšeniu takéhoto krvácania. Krvácaniu obličiek často predchádza dlhotrvajúca mikroemutúria (malý počet červených krviniek v moči), ktorá sa zaznamenáva aj v intervaloch medzi epizódami hrubej hematúrie (veľké množstvo červených krviniek v moči viditeľných pre oko).
Vzhľad krvi v moči je často sprevádzaný ťažkými dysurickými udalosťami, záchvatmi obličkovej koliky v dôsledku tvorby krvných zrazenín v močových cestách. Tieto javy sú zvlášť intenzívne a výrazné pri liečbe pacientov, keď sa dočasne obnoví normálna hemostáza. Na ukončenie hematúrie často predchádza renálna kolika a často - dočasná absencia moču s azotémiou.
Krvácanie z obličiek je náchylné k obnoveniu, ktoré môže v priebehu rokov viesť k vážnym dystrofickým deštruktívnym zmenám v tomto orgáne, sekundárnej infekcii a amyloidóze a smrti z uremie (požívanie metabolických produktov normálne vylučovaných močom a krvou).
Veľké krvácanie z gastrointestinálneho traktu u pacientov s hemofíliou sa môže vyskytnúť spontánne, hoci vo väčšine prípadov sa vyvoláva pri užívaní kyseliny acetylsalicylovej, butadiónu a iných liekov. Druhým zdrojom krvácania sú klinicky výrazné alebo "skryté" žalúdočné alebo duodenálne vredy, ako aj erozívna gastritída rôzneho pôvodu. Avšak difúzne kapilárne krvácanie sa niekedy pozoruje bez akýchkoľvek deštruktívnych zmien slizníc. Tieto diapedemické krvácania, pri ktorých je črevná stena dlhší čas nasiaknutá krvou, rýchlo vedie k anémickej kóme, akútnej vaskulárnej insuficiencii a smrti.
Krvácanie v okružie, rovnako ako veľké a malé omentum často vytvárajú falošný dojem vývoja u pacientov s akútnou chirurgické patológiu brušných orgánov, ako je akútny zápal slepého čreva, črevná obštrukcia, ktorý je zvlášť výrazné v prípade krvácania pod serózu v črevnej stene. Jedinou smernicou v takýchto situáciách môže byť rýchla účinnosť intenzívnej substitučnej liečby. Okamžitý začiatok takejto terapie sa odporúča v každom prípade - tak na odstránenie krvácania, ako aj na prípravu pacienta na operáciu. Potom sa všetko rozhodne výsledkom liečby Ak po injekcii koncentrátu faktora VIII (alebo IX) bolestivý syndróm a iné príznaky akútneho brucha rýchlo ustúpia, potom pacient môže pokračovať v sledovaní počas pokračovania intenzívnej substitučnej liečby (nekomplikované vnútorné krvácanie). Ak účinok náhradnej terapie nestačí, je potrebný chirurgický zákrok.
Krvácania do mozgu a miechy a ich membrány v hemofílii sú takmer vždy spojené buď s poraneniami alebo s použitím liekov, ktoré narušujú hemostatickú funkciu krvných doštičiek. Medzi okamihom zranenia a vývojom krvácania môže dôjsť k ľahkej perióde trvajúcej 1-2 hodiny až deň.
Charakteristickým príznakom, ktorý rozlišuje hemofíliu od inej patológie, je predĺžené krvácanie v prípade poranenia a operácie. Roztrhané rany sú oveľa nebezpečnejšie ako lineárne ruptúry. Krvácanie sa často nevyskytuje ihneď po poranení, ale po 1-5 hodinách
Tonsilektómia (odstránenie mandlí) pre hemofíliu je oveľa nebezpečnejšia ako operácia brucha.
Extrakcia zubov, najmä domorodých, je často sprevádzaná krvácaním niekoľkodňových anemizácií nielen z dier zubov, ale aj z hematómov, ktoré sa tvoria na mieste infiltrácie tkanív novokainom. Tieto hematómy spôsobujú zničenie čeľuste. Pri hemofílii by sa zuby mali odstrániť na pozadí účinku antihemofilných liekov v celkovej anestézii. Odstránenie niekoľkých zubov je najlepšie vykonané súčasne.
Niektoré z komplikácií hemofílie sú spôsobené stratou krvi, kompresiou a deštrukciou tkaniva hematómu a infekciou hematómov. Veľká skupina komplikácií je tiež spojená s poruchami imunity. Najnebezpečnejším z nich je detekcia veľkého množstva protilátok proti krvnému koagulácii (alebo IX) v krvi pacientov, ktorá modifikuje hemofíliu v takzvanej inhibičnej forme, pri ktorej hlavná metóda liečby - transfúzna terapia takmer stráca svoju účinnosť. Okrem toho opakované podávanie antihemofilných liekov často spôsobuje rýchly nárast počtu týchto protilátok u pacientov, v dôsledku čoho sa transfúzna terapia, ktorá pôvodne dala určitý účinok, čoskoro stane zbytočným.
Frekvencia inhibičnej formy hemofílie sa pohybuje od 1 do 20%, častejšie od 5 do 15%. V závažných formách hemofílie sa inhibítory objavujú v krvi pacientov neporovnateľne častejšie než v pľúcach a u pacientov starších ako 12 rokov - oveľa častejšie ako v mladšom veku. V inhibičných formách sa výrazne zhoršuje hemostatická funkcia krvných doštičiek, krvácanie do kĺbov a krv v moči sa stáva častejšie a poškodenie kĺbov je výrazne vyššie.
Z ďalších imunoalergických porúch sa niekedy pozoruje trombocytopénia, zriedkavo kombinovaná s leukopéniou, autoimunitná hemolytická anémia s pozitívnym Coombsovým testom, veľká eozinofília, amyloidóza obličiek.
Diagnóza porúch koagulačnej hemostázy
Hemofília je diagnostikovaná u všetkých pacientov s hematómovým typom krvácania a poškodením muskuloskeletálneho systému, ako aj s pretrvávajúcim oneskoreným krvácaním počas operácií. Pri indikatívnej diagnostike je dôležitá identifikácia zníženia intenzity koagulácie (koagulácie) krvi v takýchto bežných vzorkách ako koagulačný čas, aktivovaný parciálny tromboplastínový čas a autokoagulačný test s normálnymi hodnotami trombínu a protrombínového času.
S cieľom určiť, ktoré koagulačné faktory sú nedostatočné, sa uchýlia do pomoci korekčných testov s použitím testu generovania tromboplastínu alebo autokoagulačného testu.
Typ hemofílie možno tiež identifikovať pomocou "testov miešania": do plazmy vyšetrovaného pacienta v rôznych skúmavkách sa pridajú vzorky plazmy, v ktorých nie je prítomný jeden koagulačný faktor (VIII, IX alebo XI). Neprítomnosť normalizácie koagulácie v jednej zo skúmaviek naznačuje nedostatok rovnakého faktora v obidvoch zmiešaných plazmách, t.j. nedostatok pacienta.
Diagnóza hemofílie končí určením nedostatku faktora v kvantitatívnom zmysle, čo je dôležité pre správne posúdenie závažnosti ochorenia a substitučnej liečby.
Liečba porúch koagulačnej hemostázy
Hlavnou metódou liečby a prevencie hemofilného krvácania v akomkoľvek mieste a akomkoľvek pôvode je intravenózne podanie dostatočných dávok krvných prípravkov obsahujúcich faktor VIII. Faktor VIII je premenlivý a prakticky neprestáva v konzervovanej krvi, natívnej a suchej plazme. Iba priame krvné transfúzie od darcu po pacienta s hemofíliou, ako aj intravenózne infúzie krvných produktov so zachovaným faktorom VIII (antihemofilná plazma, kryoprecipitát, koncentráty faktora VIII s rôznym čistením) sú vhodné na substitučnú liečbu.
Priame darcovstvo od darcu sa uchýli len vtedy, keď lekár nemá iné antihemofilné lieky. Hrubá chyba je transfúzia krvi z matky pacienta, pretože je nosičom ochorenia a hladina faktora VIII je výrazne znížená.
Kvôli krátkému polčasu faktora VIII v krvi pacienta (približne 6-8 hodín) by sa krvné transfúzie, napríklad transfúzie antihemofilnej plazmy, mali opakovať aspoň trikrát denne. Aby sa zabránilo masívnemu krvácaniu a spoľahlivo pokryli rôzne chirurgické zákroky, ak by sa hladina antihemofilného faktora mala udržať nad 30-40%, takáto transfúzia krvi a plazmy je nevhodná. Aj keď je čas zrážania a doba recalcifikácie (saturácia krvi s vápnikom) normalizovaná u pacientov s hemofíliou so zvýšením koncentrácie faktora VIII až na 3-4%, táto úroveň nestačí na prevenciu krvácania počas operácií. Preto sa počas liečby a predoperačnej prípravy musí zamerať iba na kvantitatívne stanovenie faktora VIII (alebo na autokoagulogram), ale nie na ukazovatele celkového času zrážania, testu konzumácie protrombínu a iných metód s nízkym prahom citlivosti.
Rovnaký objem antihemofilnej plazmy je približne 3-4 krát účinnejší ako čerstvá konzervovaná krv. V jednorazových dávkach 10-15 ml / kg av dennej dávke 30-50 ml / kg, rozdelenej na 3 časti (prvá dávka je 1,5 krát viac ako 2 po sebe), antihemofilná plazma vám umožní krátko udržať 10-15% hladiny faktora VIII , Hlavným rizikom tejto liečby je to, že pacient preťažuje krvný obeh pacienta, čo môže viesť k vzniku pľúcneho edému. Použitie antihemofilnej plazmy v koncentrovanej forme nemení situáciu, pretože vysoká koncentrácia injikovaného albumínu (proteínu) spôsobuje intenzívny pohyb tekutiny z tkanív do krvi, v dôsledku čoho cirkulujúci objem krvi stúpa rovnakým spôsobom ako pri plazmatickej transfúzii pri normálnom riedení. Koncentrovaná suchá anti-hemolytická plazma má len tú výhodu, že faktor C je v nej koncentrovanejší a v malom objeme je rýchlejšie vstreknutý do krvného obehu pacienta. Suchá antihemofilná plazma pred použitím sa zriedi destilovanou vodou na 1 / 3-1 / 2 pôvodného objemu. Liečba antihemofilnou plazmou je dostatočná na zmiernenie väčšiny akútnych krvácaní v kĺboch (okrem najzávažnejších), prevencie a liečby menšieho krvácania.
Najviac spoľahlivá a účinná koncentrácia hemofílie faktora VIII. Kryoprecipitát zostáva najdostupnejším z nich - plazmatické bielkoviny extrahované ochladením (kryo-zrážanie), pri ktorých stačí faktor VIII, fibrinogén a faktor XIII, ale nie je dosť albumín a niektoré ďalšie proteíny. Nízky obsah albumínu v lieku umožňuje vstúpiť do krvného obehu pacientov vo veľmi veľkých množstvách a zvýšiť koncentráciu faktora VIII na 100% alebo viac bez obáv z preťaženia obehu a pľúcneho edému. Hlavnou nevýhodou kryoprecipitátu je jeho nepravidelnosť v činnosti.
Kryoprecipitát sa musí skladovať pri teplote -20 ° C, čo sťažuje jeho transport. Pri rozmrazení lieku rýchlo stráca aktivitu. Tieto nedostatky neobsahujú suché kryoprecipitáty a moderné koncentráty faktora VIII. Môžu byť uložené v bežnej chladničke a používané v teréne.
Množstvo faktora VIII, ktoré je obsiahnuté v 1 ml "spriemerovanej" darcovskej plazmy, tj plazmy so 100% obsahom antihemofilného globulínu, sa považuje za jednotku aktivity antihemofilného liečiva.
Na zastavenie krvácaní v kĺboch a menšie krvácanie vrátane ich prevencie počas extrakcie zubov je zvyčajne dostatočné zvýšiť hladinu faktora VIII na 15-20%. Viac nebezpečné vnútorné a vonkajšie krvácanie, ako aj vývoj hematómov v mäkkých tkanivách si vyžadujú udržanie hladiny faktora VIII nad 30-40%, pre ktoré sa kryoprecipitát alebo iné koncentráty faktora VIII podávajú v dávke 20-30 U / kg; pri veľkých operáciách a zraneniach, hematúriu a gastrointestinálnom krvácaní sa dávka kryoprecipitátu zvýši na 40-60 U / kg av niektorých prípadoch viac.
Avšak nadmerný Zavedenie kryoprecipitátu, sú nežiaduce, pretože vytvára vysokú koncentráciu fibrinogénu v krvi, čím sa narušený mikrocirkulácie v orgánoch, a je tu nebezpečenstvo trombózy a DIC.
Frekvencia podávania antihemofilných liekov je určená rozsahom, v ktorom bolo pri každom podaní možné zvýšiť koncentráciu faktora VIII v plazme. Takže ak by sa koncentrácia faktora zvýšila na 40%, potom za 6-8 hodín klesne na 20% a pri počiatočnom zvýšení na 120% sa dosiahne úroveň 20% len za deň. Moderné koncentrované prípravky faktora VIII (kryoprecipitát atď.) Môžu byť obmedzené na 1-2 intravenózne injekcie denne. Dostatočný účinok náhradnej terapie sa dosiahne len vtedy, ak sú splnené nasledujúce podmienky: všetky antihemofilné lieky sa podávajú intravenózne len v prúde, v najkoncentrovanejšej forme a čo najskôr po ich deaktivácii bez miešania s inými infúznymi roztokmi. Jedným z hlavných dôvodov zlyhania substitučnej liečby sú kvapkanie injekcií krvných produktov, ktoré nezvyšujú hladinu faktora VIII v plazme.
Až do ukončenia stabilného krvácania sa má zabrániť zavedeniu akýchkoľvek krvných náhrad a hemopreparácií (krvných produktov), ktoré neobsahujú antihemofilné faktory, pretože to vedie k zriedeniu faktora VIII a zníženiu jeho koncentrácie.
Včasné odstránenie (aspirácia) krvi, ktorá sa vyliala do kĺbu, nielenže okamžite potláča bolestivý syndróm, zabraňuje ďalšej koagulácii krvi v kĺbe, ale tiež znižuje riziko vzniku a rýchleho rozvoja osteoartritídy. Na prevenciu a zmiernenie sekundárnych zápalových zmien po aspirácii krvi lekár predpisuje zavedenie 40-60 mg hydrolyzónu do kĺbu. Podporná transfúzna terapia, ktorá sa uskutočňuje počas prvých 36 dní, zabraňuje ďalšiemu krvácaniu a umožňuje skoré zahájenie tried fyzickej liečby, čo prispieva k rýchlejšiemu a úplnejšiemu obnoveniu funkcie postihnutej končatiny, zabraňuje atrofii svalov.
Pohyb postihnutého kĺbu by sa mal rozvíjať postupne: počas prvých 5 až 7 dní po odstránení imobilizačného obväzu sa aktívne pohyby uskutočňujú tak v postihnutom kĺbe, ako aj v iných kĺboch končatín, čím sa postupne zvyšuje frekvencia a trvanie cvičenia. Neskôr od 6. do 9. dňa prejdú na cvičebné cvičenia s použitím bicyklových ergometrov, pedálových brán na ruky a elastických tyčí. A až v dňoch 11. - 13. deň, aby sa eliminovala zvyšková tuhosť a obmedzilo maximálne ohnutie alebo nekrvácanie, sa pasívne cvičenia vykonávajú s opatrnosťou pod kontrolou antihemofilných plazmových transfúzií alebo malých dávok kryoprecipitátu.
Súčasne od 5. - 7. dňa sú predpísané fyzioterapeutické účinky - hydrokortizónová elektroforéza, anodická galvanizácia.
V prípade krvácaní v mäkkých tkanivách je potrebná intenzívnejšia liečba ako pri krvácaní v kĺboch, pri liečbe antihemofilnými liekmi. Pri anemizácii pacienta sú predpísané ďalšie transfúzie červených krviniek. Ak sa objavia príznaky infekcie hematómu, okamžite sa predpíše širokospektrálne antibiotiká. Akékoľvek intramuskulárne injekcie na hemofíliu sú kontraindikované, pretože môžu spôsobiť rozsiahle hematómy a pseudotumory. Penicilín a jeho polosyntetické náprotivky sú tiež nežiaduce, pretože spôsobujú dysfunkciu trombocytov vo vysokých dávkach a zvyšujú krvácanie.
Včasná a intenzívna antihemofilná terapia prispieva k rýchlemu rozvoju hematómov. Hematómové prepichnutie a aspirácia krvi sa musia vyhnúť. Pokračujte v transfúznej terapii od 5 do 7 dní. Obalené hematómy sa odstránia, ak je to možné, chirurgicky spolu s kapsulou pod krytom intenzívnej starostlivosti s koncentrátmi antihemofilných faktorov.
V prípade krvácania z nosa by sa lekár nemal uchýliť k tesnej tamponáde, najmä k zadnej strane, pretože okamžite po odstránení tampónov krvácanie u takýchto pacientov takmer vždy pokračuje s ešte väčšou silou.
Pre pokiaľ možno rýchle zastavenie krvácania z nosa byť použité antihemophilic plazme a antigemofilicheskie lieky v kombinácii s zavlažovania nosovej sliznice riešenie aminokaprónovú, trombín alebo adroksonom.
Krvácanie z obličiek, pri ktorom sú transfúzie antihemofilnej plazmy a nízke dávky kryoprecipitátu neúčinné, predstavuje vážne nebezpečenstvo pre pacientov. Odporúčané priemerné dávky antihemofilných liekov (30-40 U / kg) tiež nie vždy zastavujú krvácanie alebo ich zastavujú maximálne 1 až 2 dni. Zvyšuje účinnosť použitia antihemofilných liekov prednizónu (20-30 mg / deň u dospelých pacientov).
Na úľavu gastrointestinálneho krvácania sa majú v kombinácii s kyselinou aminokapronovou dávky až 0,2 g / kg používať veľké dávky koncentrátov antihemofilných faktorov.
Treba poznamenať, že prednisolón sa má predísť používaniu prednizolónu na krvácanie v gastrointestinálnom trakte, použitie prednizolónu je najnebezpečnejšie pre vredy žalúdka a dvanástnika.
Malo by sa pamätať na to, že krvácanie do žalúdka sa často spúšťa prijímaním v súvislosti s bolesťou v kĺboch, zubnom alebo bolesti hlavy acetylsalicylová kyselina, Brufen, indometacín, butazolidonov. U pacientov s hemofíliou môže dokonca aj jedna dávka kyseliny acetylsalicylovej spôsobiť krvácanie do žalúdka.
Pri prevencii a liečbe chronickej osteoartritídy a iných poranení pohybového aparátu je potrebné zvážiť rôzne spôsoby ochrany kĺbov a predchádzania úrazom končatín. Na to sa šijacie gumové štíty šiť okolo kolenných, členkových a lakťových kĺbov, všetky športy spojené so skákaním, pádom a modrínami (vrátane cykloturistiky a motocykla) sú zakázané. Dôležitú úlohu zohráva najskoršia možná a úplná liečba akútnych krvácaní vo svaloch a kĺboch, intenzívne celoročné terapeutické cvičenie. Na tento účel sa skladajú z komplexov atraumatických cvičení vo vode, na mäkkých podložkách a cvičebných prístrojoch - bicyklových ergometroch, ručných bránach. Triedy sa musia začať v predškolskom veku alebo v mladšom školskom veku, to znamená pred chronickou osteoartrózou, poruchou pohyblivosti a ďalšími ťažkými poruchami vyvinutými v muskuloskeletálnom systéme.
Komplexná liečba je doplnená o fyzioterapeutické (vysokofrekvenčné prúdy, elektroforézu glukokortikosteroidov) a balneologické liečebné metódy, ktoré zahŕňajú: bahno, krokové kúpele a radónové kúpele. Pri častých a pretrvávajúcich krvácaníach v tých istých kĺboch sú vybranými metódami rádioterapia a synovektómia (odstránenie synoviálnej membrány kĺbu).
Rádioterapia sa vykonáva v jednej dávke 25-50 R (pre akútne krvácanie) na 50-100 R pre chronickú osteoartritídu. Reakcie sa opakujú po 1 až 2 dňoch, celková dávka sa pohybuje od 400 do 1000 R. U detí mladších ako 14 rokov je potrebná určitá opatrnosť z dôvodu možnosti poškodenia zón rastu kostí, a preto celková dávka by nemala presiahnuť 400 R. V posledných rokoch, a vnútornú expozíciu injekciou rádioaktívnych izotopov do kĺbov.
Synovektómia uskutočnená jediným rezom je vysoko účinná metóda na liečbu hemofilných lézií kĺbov, prevenciu ťažkej osteoartritídy. Tento typ liečby eliminuje následné krvácanie v ovládanom kĺbe, zabezpečuje zachovanie jeho normálnej konfigurácie a funkcie. Tento účinok sa vyskytuje s pomerne skorou operáciou - s artrózou I. až II. Stupňa a s léziami III. - IV. Stupňa, synovektómia spravidla už nie je vhodná. Tak ako všetky ostatné operácie, synovektómia sa uskutočňuje s použitím kryoprecipitátu alebo iných koncentrátov antihemofilných faktorov.
Iné ortopedické postupy často vykonávať ahilloplastiku predlžovacích kostí s cieľom obnoviť spoločný priestor, vo vážnych prípadoch - plošných spojov stlačený v normálnej polohe. Neoceniteľné služby, ale zároveň prináša zariadenie Volkova - Hovhannisyan, Ilizarovův a ostatnými zabezpečuje opravu rýchlo a spoľahlivo bez extrémne nebezpečné pre pacientov s predĺženou imobilizáciou končatín. Obnovenie spoločného priestoru bez použitia týchto zariadení všeobecne je takmer nemožné.
S dostatočnou kryoprecipitátu substitučnou terapiou (v prvých 7-8 dní - 30-40 U / (kg x deň), potom - polovica množstva) u pacientov, poskytovaných úplne spoľahlivé hemostázy; krvácanie a krvácanie v miestach lúčov nie sú dodržiavané.
Moderné metódy substitučnú terapiu a použitie ortopedických prístrojov sa výrazne zmenila prognózu zlomenín u pacientov s hemofíliou. Nie je to tak dávno, tieto zlomeniny nehojí, často komplikované falošnými spojmi a dokonca viesť k strate končatiny, potom pod vplyvom veľkých dávok kryoprecipitátu, zatiaľ čo zblíženie a dobré zariadenie kostnej fixácie je poskytovaná prostredníctvom hojenie zlomenín v zvyčajnom čase vyššie zmienené.
Za vynikajúce terapeutické problémy, patrí boj proti osteoporóze, cýst a Vnútrokostné pseudotumor, ktorý nemá sklon k osumkovaniyu. Tieto procesy dať vážne komplikácie a niekedy nútení uchýliť sa k amputácii.
Liečba komplikovanej hemofílie. Najnebezpečnejší je detekcia v krvi u pacientov s hemofíliou veľké množstvo protilátok proti faktoru VIII, ktoré určujú inhibičné transformáciu hemofílie v tvare. Inhibítor je schopný inaktivovať veľmi veľké množstvo podaného faktora VIII z vonkajšej strany, a preto je primárna liečba - substitučná terapia transfúzia - sú neúčinné, alebo sa stanú úplne neúčinné.
V procese transfúzna terapii (s 4-6-tý deň) titer protilátky sa môže zvýšiť.
Ak je potrebné substitučná terapia zo zdravotných dôvodov, je dočasne schopný prekonať účinok podávanie protilátky obrovských množstvo koncentrátu faktora VIII (500-1000 U / kg), alebo plazmaferéza (odstránenie pacienta s niekoľkými litrov plazmy nahradí čerstvým antihemophilic), spolu s faktorom VIII injekcie mega ,
Ukázalo sa, schodnejšou aplikáciu v inhibítora hemofílie A tzv bypass zaobchádzanie - podávanie koncentrátov faktora IX, X a II. Ich použitie vo vysokých dávkach poskytuje polovica pacientov s inhibítorom hemofíliu zastavenie krvácania. Avšak, trombogénna potenciál týchto známych liečiv, ich schopnosť vyvolať vývoj DIC a trombózy, zvlášť pri použití kyseliny aminokaprónovú a ďalších krvných zrazenín. Môže vyvinúť také porušenie a bypass terapia inhibičný formu hemofílie. Napríklad popísané prípady infarktu myokardu u mladých pacientov s hemofíliou opätovné faktorov koncentrátov protrombínového komplexu. Podľa niektorých autorov, s inhibičný hemofíliou účinnejšie, než je obvyklé, a tzv aktivovaných protrombínového komplexu prípravkov, alebo komplex faktora IX. Sú však viac ako 10 krát drahšie ako neinvestičného koncentráty tie isté faktory. Aby sa znížilo riziko diseminovanej intravaskulárnej koagulácie a trombózy sa odporúča zavádzať tieto faktory, antitrombínu III, alebo s vopred hlboko zmrazené plazmy, spolu s malými dávkami kontrikala.
Údaje o účinku prednizónu na množstvo protilátok v krvi sú kontroverzné, ale väčšina autorov však na vedomie, že u pacientov s liečbou hemofílie je málokedy efektívna. Imunosupresíva (azatioprin, atď.), Často znižujú množstvo protilátky, ale ich použitie je nebezpečné vzhľadom k rozvoju trombocytopénia, hemofília, ktorý môže významne zhoršiť hemoragickej javy.
Ak sa u pacientov s hemofíliou inhibítormi nie je pozitívny trend, kedy substitučná terapia pred operáciou treba vždy starostlivo skontrolujte, či je prítomný v plazme inhibítor.
Počas zhoršenie reumatoidnej sekundárneho syndrómu, ako aj v priebehu intenzívnej substitučnej terapie, a to najmä v prípade, že neoslabuje, ale posilňuje bolesti kĺbov, poskytuje dobrý účinok prednizolónu (20-40 mg na deň po dobu jedného mesiaca, nasledované postupným poklesom na najnižšiu dávku).
Veľmi dôležité pre prevenciu krvácania je minimalizovať riziko zranení, škrtov atď., Od raného detstva. Vyradené z používania sú ľahko rozbité hračky (vrátane kovu a plastu), ako aj nestabilné a ťažké predmety. Nábytok by mal byť so zaoblenými hranami, vyčnievajúcimi okrajmi zabalenými bavlnou alebo penovou gumou, podlahou pokrytou vlasovým kobercom. Komunikácia a hranie pacientov s dievčatami namiesto chlapcov je vhodnejšia.
Pre pacienta je dôležitá správna voľba povolania a pracoviska. V najvážnejších prípadoch je jedinou účinnou metódou zmierňovania ochorenia systematické, raz za 10 dní intravenózne podávanie kryoprecipitátu alebo akéhokoľvek iného dostupného koncentrátu faktora VIII. Jedna dávka lieku na takúto prevenciu je 400 až 800 IU.
Veľmi dôležitá pre prevenciu ťažkých lézií pohybového aparátu je čo najskoršie podanie prípravkov faktora VIII na modriny a iné poranenia, ako aj na prejav akútnej bolesti kĺbov, čo naznačuje, že sa začalo presakovanie krvi. Okamžité zavedenie koncentrácií antihemofilných faktorov (špeciálny pohotovostný tím alebo hemofilné centrum alebo vyškolení rodičia) prerušuje tvorbu alebo exacerbáciu krvácania na samom začiatku, zabraňuje ničivým zmenám v kĺbe. Núdzová prvá pomoc je základnou súčasťou fyzickej rehabilitácie pacientov a prevencie závažných a nezvratných zmien kĺbov, kostí a svalov. Dramaticky znižuje počet hospitalizácií, priemerná ročná dĺžka pobytu v nemocnici, nezaťažuje deti zo školy.
Po zintenzívnení substitučnej transfúznej terapie sa zvyšuje počet ľudí infikovaných sérovou hepatitídou, závažné reakcie na zavedenie hemopreparátov sa zvyšujú a dochádza k mnohým ďalším poruchám imunity.
Génová profylaxia pre hemofíliu ešte nebola vyvinutá. Určenie pohlavia vyšetrením sexuálneho chromatínu a karyotypu amniotických buniek získaných metódou amniocentézy umožňuje včasné ukončenie tehotenstva, ale nepreukazuje, či je plod nosičom hemofilného génu. Tehotenstvo sa zachová, ak je plod mužom, pretože všetci synovia pacientov sa narodili zdravo a prerušili sa, ak je plod samica, pretože všetky dcéry pacientov s hemofíliou sú nosičmi choroby.
Ženy - nositeľmi hemofília, s 50% pravdepodobnosťou narodenia pacienta (v prípade, že plod je muž) alebo Prevádzajúci hemofília (v prípade plodu ženského pohlavia), narodenia dievčat len nesie riziko rodiny hemofilikov s prvej generácie na druhú, a zároveň sa zvyšuje celkový počet nosičov choroby.
Ministerstvo zdravotníctva Ruskej federácie schválila liek Revoleyd (Eltrombopag) na použitie u detí. Nový liek je indikovaná u pacientov trpiacich chronickou imunitný trombocytopénia (idiopatická trombocytopenická purpura, ITP), zriedkavé ochorenie krvného systému.
03.03.2017
Kanadskí vedci z University of Ottawa sa chystá revolúciu v regeneratívnej medicínu. V jednom z posledných pokusov boli schopní rast ľudské ucho od obvyklého jablká.
27.02.2017
Odborníci Prvý Pavlov Medical University v St. Petersburg, vytvorili nanočastice, s ktorými možno diagnózu infarktu a pred infarktom pacienta. Aj v dlhodobých štúdií, budú nanočastice využiť ...
Zdravotnícke články
Takmer 5% zo všetkých malígnych nádorov je sarkóm. Sú veľmi agresívne, rýchle šírenie prostredníctvom hematogenního a sklon k recidívam po ošetrení. Niektoré sarkómy sa vyvíjajú v priebehu rokov a nič nepreukazujú ...
Vírusy nie sú len vznášať vo vzduchu, ale tiež môžu dostať na zábradlie, sedadlá a iné povrchy, pri zachovaní ich aktivitu. Preto pri cestovaní alebo na verejných miestach, je žiaduce nielen eliminovať komunikáciu s inými ľuďmi, ale tiež, aby sa zabránilo ...
Získať dobrý zrak a rozlúčiť sa okuliarov a kontaktných šošoviek - sen mnohých ľudí. Teraz sa to môže stať realitou rýchlo a bezpečne. Nové vlastnosti laserovej korekcie videnia otvára úplne bezkontaktný spôsob Femto-LASIK.
Kozmetické prípravky, ktoré sú určené na starať sa o našu pokožku a vlasy, v skutočnosti nemusí byť tak bezpečný, ako si myslíme
Zložité mechanizmy, ktoré podporuje krv v kvapalnom stave, a to bez jeho koagulácie v lumenu cievy, alebo presakovanie cez cievnu stenu, sa nazýva hemostáza. Vzhľadom k tomu, patologických stavov spojených s krvnými zrazeninami sa zaoberal v ďalšej kapitole, mal by vziať do úvahy iné zmeny spojené s poruchami hemostázy.
Krvácanie (krvácanie z gréckeho haima -. Krv a reín - prietok) sa nazýva krvi v cievnom riečišti alebo v centre pre životné prostredie (vonkajšie krvácanie) alebo v telových dutinách, dutých orgánov lumen (vnútorné krvácanie). Príklady vonkajších krvácanie sú metrorágia (maternice), meléna (črevné) a vnútorné - hemopericardium, hemotorax, hemoperitoneum a hemartrózy (v perikardiálna dutine, pohrudnice, brucha alebo kĺbov v tomto poradí).
V závislosti od zdroja krvácania sa delia na arteriálne, žilovej, arteriálna, venózna (zmiešané), kapiláry, parenchymatózne (kapilárnej z solídnych orgánov) a srdce.
Zvláštny druh krvácanie je krvácanie, v ktorých krv extravascularly akumuláciu v tkanivách. Existujú štyri typy:
Hematóm - hemorágia s poruchou integrity tkaniva a tvoria dutinu;
Hemoragickej impregnácia (infiltrácia) - krvácanie zachovanie intaktné tkanivá;
Ekchymóza (podliatiny) - krvácanie do rovinné kože, podkožia, sliznice;
Petechie - určiť, krvácanie do kože, slizníc a serózna membrány, vnútorné orgány.
Niekoľko petechické krvácanie, splývajúce spolu vo väčšej veľkosti, zvané hemoragickej purpura a modriny až 2 cm v priemere - ekchymóza.
Mechanizmy krvácanie alebo hemorágia zahŕňajú:
Medzera (haemorragia za rhexin), vyplývajúce z poranení alebo nekrózy nemodifikovaná nádoby (srdcové tečenie pri infarkte myokardu), zápal (syfilitickú mezaortit s ruptúrou aorty), postihnutého cievna aneuryzma;
Korózia (haemorragia za diabrosin), alebo arrosive krvácanie, ktoré sa vyvíja v zničení cievnej steny zápalu (viac purulentná), zhubný nádor, nekróza (kazeózna nekrózy krvácanie tuberkulóznej dutiny), pôsobenie chemických látok (žalúdočnej šťavy môže spôsobiť krvácanie z žalúdočných vredov), klíčenie choriových klkov cievne vajíčkovod s ektopickej tehotenstva;
Diapedézu (haemorragia za diapedesin, z gréckeho dia -. Prostredníctvom, Peda - skákanie), pričom výstup z krvi zvýšená permeabilita ciev, väčšinou neporušený s mikrovaskulárnych v ťažkej hypoxie, intoxikácie, infekcie, rôzne koagulopatia, hemoragická diatéza. Pomerne často diapedetic krvácanie vyvinutý pre hypertenznej krízy, systémové vaskulitídy, leukémie, hemofília, urémia.
Tendencia k spontánnemu krvácaniu alebo krvácanie v reakcii na ešte menšie poškodenie bol nazývaný hemoragická diatéza. Tento stav je spojený s kvalitatívne alebo kvantitatívne zmeny krvných doštičiek nedostatočnú koaguláciu, patologické krehkosti alebo zvýšenú vaskulárnu permeabilitu ako dedičné a získané.
Hlavné príčiny krvácania (krvácanie) sú:
1. Zlepšená cievnej krehkosti pozorovali pri jeho vrodených vád, infekcií a intoxikáciou, hypo- a beriberi, steroidné terapiu;
2. Poruchy krvných doštičiek. Medzi ne patrí trombocytopénia akéhokoľvek pôvodu, vrodená alebo získaná adhézie oslabenie (von Willebrandovho choroba, Bernard-Soulier, dedičná hemoragická diatéza, atď.), Oslabený agregácie doštičiek alebo zníženie sekrécie;
3. vrodený nedostatok koagulačných faktorov (hemofília A pre faktor VIII, hemofílie B podľa faktora IX, von Willebrandovej choroby, iných koagulačných faktorov), alebo viac získané pôvodu (ochorenie pečene, nedostatok vitamínu K, niektoré imunitný lézie);
4. Prebytočný intravaskulárna koagulácia, ako je roztrúsená intravaskulárna koagulácia, - (. Pozri nasledujúce prednáška) DIC.
Exodus krvácanie môže byť výhodné (vstrebávanie extravazáciu krvi, organizácie, zapuzdrenie, vzdelanie "hrdzavé" cysty) a nepriaznivé (hnisanie vstup infekcie).
Hodnota krvácania je spôsobená jeho vzhľadom, závažnosťou a trvaním. Napríklad, infarkt infarkte myokardu s hemopericardium tvorby rýchlo vedie k smrti pacienta, aj keď celkový počet streamovaného krvi je zvyčajne nie viac ako 100 až 200, s tepnového krvácania môže vyvinúť masívne straty krvi a akútna anémia s fatálnymi následkami. Dlhšie mierne krvácanie z chronického žalúdočného vredu alebo dvanástnikové vredy spôsobuje chronické hemoragickej anémie. Znamenať krvácanie závisí predovšetkým na jeho lokalizáciu, a to iba na jeho veľkosti. Dokonca aj malé krvácanie do mozgu môže spôsobiť stratu životne dôležitých centier, opuch mozgu a smrť pacienta, zatiaľ čo dokonca nekomplikovaný masívne krvácanie do podkožia nepredstavuje ohrozenia života.
Plasmorrhages - výstup z lúmen krvnej plazmy impregnačný nádoby sa okolitého tkaniva (plazmatická impregnačný) v dôsledku zvýšenej priepustnosti ciev. Plasmorrhages dochádza transendoteliální náležite ultrafiltráciu (výťažok plazmy pórov bazálnej membrány endotelu zvýšením hydrostatického alebo osmotického tlaku), šírenie (spôsobené gradientom plazmy zložiek v lumen a z nádoby), microvesicular dopravu (mikropinotsitoz alebo tsitopemzis vyskytujúce sa v dôsledku činnosti systémov enzým endoteliálnych) , Uvoľňovanie medzi endoteliálnou plazmou je tiež možné. Tak plasmorrhages definované poškodenie cievnej steny (predovšetkým jeho intima) a zmeny v krvných konštanty. Morfologické štúdie mikrovaskulárna stena hustne a stáva homogénna, zatiaľ čo elektrónové mikroskopické vyšetrenie v opuchnutých endotelových buniek má veľký počet mikrovezikul, fenester a tvorba tunel, vzhľad medzibunkových medzier, uvoľnenie intimální bazálnej membrány. Akumulácia plazmy zložiek vedie k poškodeniu buniek a medzibunkovej látky v cievnej stene a perivaskulárnej tkaniva, ktorého výsledok sa vyvíja hyalinóza, a vo vážnych prípadoch - fibrinoidní nekrózu.
Shock - závažný chorobný stav vyznačujúci sa tým, cirkulačného kolapsu (akútne obehové zlyhanie) po superstrong dopad na hemostázy. Rozlišovať hypovolemický, srdcové a cievne typy septického šoku.
Hypovolemický šok spôsobený rýchlym poklesom na 20% alebo viac z cirkulujúceho objemu krvi, ktorá pri pohľade so stratou akútna krvi, dehydratácia. To znamená, že straty tekutín a elektrolytov je možné s rozsiahlymi popáleninami (vzhľadom k výkonu plazmového z poškodených Mikrocirkulačná ciev) s ťažkým vracaním, hnačkou hojné.
Srdcové šok sa vyvíja v závislosti na poklese objemu zdvihu v porážke srdce je pozorovaná u infarktu myokardu, závažné myokarditídy, akútnej mitrálnej alebo aortálnej regurgitácia, protetických trombózy ventil, pretrhnutie interventrikulárního septom hemotamponade srdca košele. Výrazný pokles vo výsledkoch krvného tlaku k významnému zníženiu krvného zásobenia tkanív, hypo-volemic podobným zmenám.
Septik (toxický-infekčné) šok sa vyskytuje v prítomnosti infekcie spôsobené gram-negatívne (E. coli, Proteus, Klebsiella, atď) Menej grampozitívne (staphylo-, streptokoky, pneumokokov) mikroflóry. Vylučované toxíny (hlavne endotoxín) aktivovať komplement, koagulácie, fibrinolýzy, ako aj doštičiek a neutrofilov. V dôsledku toho, stimulované tvorba oxidu dusnatého (silný vazodilatátora), tumor nekrotizujúci faktor a, interleukín spôsobujúce akútne obehové zlyhanie.
Vaskulárne (redistribúcia), môže byť neurogénna šok (traumatické, bolesti, poranenia miechy ako komplikácia anestézia) alebo anafylaktických indukovanej generalizované reakcie precitlivenosti. V dôsledku výrazného vazodilatáciu, zvýšenej priepustnosti kapilár a arteriovenózne resetovanie redistribučnú intravaskulárneho objemu krvi, sprevádzané významným znížením celkovej periférnej vaskulárnej rezistencie.
Šok v jeho vývoji prechádza v troch etapách:
1. neprogredujúcich (skoré) fáze šoku je charakterizovaný poklesom krvného tlaku a objemu srdcového výdaja pri zachovaní relatívne normálnej prívod krvi do životne dôležitých orgánov. To je spôsobené vyrovnávacej vazokonstrikciu ciev, najmä kože a čriev. S vyčerpaním adaptačných mechanizmov šok prechádza do ďalšej fázy;
2. Progresívne rôzne fázy šoku klinické symptómy, hlboké kolaps spôsobené zníženou krvi plniť všetky orgány a tkanivá (tkaniva hypoperfúzie v dôsledku zvyšujúcej sa arteriálnej dilatácie Keying), rozvoj metabolických a obehových porúch. 3. nevratný šok stupeň je výrazný nedostatok krvného obehu na úrovni mikrocirkulácie v narušeniu integrity cievnej steny, rýchlo rastúce multiorgánové zlyhanie, končiť smrťou pacienta.
Morfologické vyšetrenie poukazuje na generalizované dystrofické a nekrotické zmeny, fenomény DIC syndrómu (petechiálne krvácanie, stazenie, tromby v mikrovaskulatúre). Navyše vzhľadom na zvláštnosti štruktúry a fungovania rôznych orgánov v každom z nich vznikajú zvláštne zmeny - orgány šoku. Teda vývoj nekrotickej nefrózy (nekróza epitelu epitelu epitelu) je charakteristická pre šokovú obličku. Šoková pľúca sa prejavuje ohniskami atelectázy, seróznym hemoragickým edémom, niekedy so stratou fibrínových vlákien (hyalínových membrán). V mozgu sa objavuje ischemická encefalopatia, ktorá sa prejavuje edémom, bodavým krvácaním a ložiskom nekrózy. V srdci sú pozorované malé, väčšinou subendokardiálne ložiská krvácania a nekróza myokardu, mastná dystrofia kardiomyocytov s príznakmi ich retrakcie. V kortikálnej vrstve nadobličiek dochádza k poklesu až po úplné vymiznutie lipidov používaných na syntézu steroidných hormónov. V gastrointestinálnom trakte sú zistené krvácania, erózie a akútne vredy v sliznici. Šoková pečeň sa vyznačuje tukovou dystrofiou hepatocytov a v niektorých prípadoch aj ich centrolobulárnou nekrózou.
Prognóza šoku závisí od typu, závažnosti, štádia, v ktorej sa liečba začína, prítomnosti komplikácií. V súčasnosti s vážnym kardiogénnym alebo septickým šokom dosahuje úmrtnosť 50% alebo viac.
Kľúčové pojmy narušenej hemostázy:
1. Hemostatické poruchy, koagulopatia (koagulopatia, koagulo- + grécko - patos - utrpenie, choroba) - zhoršená funkcia krvných koagulačných a antikoagulačných systémov.
2. Hyperkoagulačný trombotický stav- stav sprevádzaný patologickým procesom zvýšenej zrážanlivosti krvi v dôsledku zvýšenej agregácie krvných doštičiek, aktiváciou plazmatických a tkanivových koagulačných faktorov s tvorbou krvných doštičiek a fibrínových zrazenín.
3. Hypokoagulačný hemoragický stav- stav sprevádzaný patologickým procesom znižovania zrážanlivosti krvi v dôsledku poklesu agregácie doštičiek, inaktivácie faktorov koagulácie plazmy a tkaniva s výskytom krvácania a krvácania.
4. DIC (trombotický hemoragický stav) - diseminovaná intravaskulárna koagulácia krvi - typický patologický proces hemostatických porúch v dôsledku postupne sa vyskytujúceho zrážací reakcie hyper koaguláciu (tvorba šírených krvných zrazenín v cievach mikrocirkulácie) a antikoagulačné (deplécie trombogénna faktorov a zvyšujúce fibrinolýza), sprevádzané masívnym krvácaním, ťažkú hemokoagulácie šok a akútna dystrofia vnútorných orgánov.
V akých chorobách dochádza k porušeniu hemostázy:
Hemostáza - zložitý proces, ktorý zabraňuje alebo zastaví prietok krvi z lumen, poskytuje vzhľad fibrínu zväzku potrebné pre obnovu integrity tkaniva, a nakoniec sa odstráni fibrín, keď potreba zmizne. V tomto procese sú zapojené štyri hlavné fyziologické mechanizmy.
Použitie krv hemostatický systém plní svoju dôležitú funkciu - udržanie kvapalného skupenstva krvi prúdiacej v cievach, a koagulácie krvi tým, poškodenie cievnej steny, a tým zastavenie krvácania a udržanie objemu krvi a zloženie. Systém hemostázy je viaczložkový. Jedná sa krvné doštičky a ostatné krvné bunky, cievne steny extravaskulárnej tkaniva, biologicky aktívnych látok (na doštičky vaskulárne hemostázy), v plazme, tkanivové faktory zrážanlivosti (koagulácia hemostázy) úzko leží s antikoagulantom, fibrinolytickej a kalikreín-kinínového systémy. Porušenie niektorej z týchto zložiek vedie k patologickým zastavenie krvácania.
Klasifikácia porúch hemostázy. Patológia hemostázy je klasifikovaný primárny lézií svojich jednotlivých zložiek v destičkovitých cievne poruchy hemostázy a koagulačné hemostázu. Podľa etiológie týchto porúch môžu byť získané a dedičné, a na smere zmien rozdelených do zníženie zrážania krvi (hypocoagulation) a zvýšenie krvnej zrážanlivosti (hyperkoagulability), ktorý môže byť lokálna (trombóza) a generalizované (DIC).
Zníženie koagulácie krvi
Zníženie zrážanie krvi sa nadmerné krvácanie (hemoragické syndróm) - recidíve krvácanie, krvácanie vyskytujúce ako spontánne a s menšími zraneniami.
Doštičiek-vaskulárne hemostáza je narušená v kvantitatívnych a kvalitatívnych zmien krvných doštičiek (trombocytopénia a thrombocytopathy) a lézií cievnej steny.
Trombocytopénia sa nazýva pokles počtu krvných doštičiek v krvi pod normou (180-320 G / l alebo 180-320x109 / l). Spontánne krvácanie sa však vyskytuje len vtedy, keď ich počet klesne pod 30 g / l. Pod trombocytopatiami rozumie kvalita podradnosti a dysfunkcie krvných doštičiek s normálnym alebo zníženým obsahom.
Príčiny nízkej koagulácie krvi. Príčinou trombocytopénia imunitných odpovedí sú často mení antigénne štruktúru krvných doštičiek pôsobením vírusov, lieky, antiagregačné autoprotilátky formulácie (s chronickou lymfatickou leukémiou, idiopatickej trombocytopénie), krvných doštičiek nezlučiteľnosti medzi matkou a antigény plodu. Okrem toho sa trombocytopénia vyvíja v dôsledku poruchy megakaryocytového výhonku kostnej drene ionizujúcim žiarením, chemikálií alebo jeho nahradením nádorovými metastázami, leukemickými infiltráty. Zníženie trombocytopoézy môže byť spôsobené nedostatkom kyanokobalamínu a kyseliny listovej, dedičnou poruchou tvorby krvných doštičiek (vrátane tých, ktoré majú nedostatok trombocytopoetínov). Trombocytopénia sa vyskytuje v dôsledku mechanického poškodenia trombocytov so splenomegáliou, umelých srdcových chlopní, ako aj zvýšenej spotreby krvných doštičiek s lokálnou a generalizovanou intravaskulárnou koaguláciou krvi.
Etiologické faktory, ktoré spôsobujú trombocytopatiu, zahŕňajú pôsobenie toxických látok a liekov (alkohol, kyselina acetylsalicylová), ionizujúce žiarenie, endogénne metabolity (uremia, cirhóza pečene); deficiencia cyanokobalamínu, hormonálne poruchy (hypotyreóza). V membránovej štruktúre a biochemickej kompozícii krvných doštičiek (nedostatok trombostenínu, faktor 3, ATP, ADP, G-6-FDG, membránové receptory pre faktory V, VIII, XI atď.) Existujú genetické defekty.
Hemoragické vazopatiyah lézie cievnej steny, čo vedie k narušeniu doštičky vaskulárnej hemostázy a krvácanie, dochádza v dôsledku zvýšenej permeability steny krvných ciev a jeho degradácii v rozpore s syntézu kolagénu (pre potravinárske nedostatku kyseliny askorbovej, vrodených chýb v syntéze kolagénu) pôsobením biologicky aktívnych látok ( alergia), rádiotoxíny (ožarová choroba), imunitná hemoragická vaskulitída, zníženie angiotrofickej funkcie krvných doštičiek počas trombocytov Otvorenie a thrombocytopathy, zničenie leukemické infiltráciu cievnej steny. Jednou z príčin krvácania je zníženie tvorby vaskulárnej steny endotelu von Willebrandovho faktora - zložky s veľkou molekulou koagulačného faktora VIII - krvi (dedičná choroba von Willebrandovej choroby). Tento faktor sa hromadí v krvných doštičkách a pri degranulácii sa uvoľňuje.
Na normálnu priľnavosť krvných doštičiek k kolagénovej stene je nevyhnutné a bez nej sa nevytvorí trombóm krvných doštičiek. Hemoragický syndróm sa pozoruje aj pri zvýšenej membránovej peroxidácii membránových fosfolipidov, v dôsledku čoho sa v endotelu syntetizuje a vylučuje nadmerné množstvo silných inhibítorov agregácie trombocytov, prostacyklínov. Okrem toho zhoršená neurogénna a humorálna regulácia vaskulárneho tónu vedie k zníženiu cievnej hemostázy krvných doštičiek, čo vedie k nemožnosti blokovania malých ciev trombocytárnym trombom.
Patogenéza nízkej koagulácie krvi. Existujú štyri hlavné mechanizmy trombocytopénie: pokles produkcie, zvýšená deštrukcia, zvýšená spotreba (trombóza), prerozdelenie krvných doštičiek.
Prerušenie hemostázy a vývoj krvácania počas trombocytopénie v dôsledku nasledujúcich mechanizmov:
- zvýšená mikrovaskulárna priepustnosť erytrocytov a iných krvných zložiek (diapedemické krvácanie) a vaskulárna krehkosť v dôsledku dystrofie steny pri vypnutí funkcie angiotrofných krvných doštičiek;
- zníženie funkcie adhéznej agregácie doštičiek;
- porušenie reakcie uvoľňovania krvných koagulačných faktorov krvných doštičiek, ADP, serotonínu, adrenalínu, antiheparínového faktora, čo má za následok nedostatočnú tvorbu trombov krvných doštičiek, absenciu vazospazmu a spomalenie koagulácie;
- zníženie zrážania zrazeniny ako dôsledok zníženia aktivity kontraktilného proteínu krvných doštičiek - trombostenín (faktor trombocytov 8).
V patogenéze trombocytopatie je možné rozlíšiť dva hlavné mechanizmy ich výskytu: tvorba patologických krvných doštičiek v kostnej dreni a deštrukcia krvných doštičiek vo všetkých častiach krvného systému. Patogenéza trombocytárnej hemostázy s trombocytopatiou je rovnaká ako pri trombocytopénii, pretože je spojená s deaktiváciou funkcií krvných doštičiek.
Porušenie koagulačnej hemostázy vedúce k vzniku krvácania môže byť spôsobené nasledujúcimi faktormi:
- získané a dedičné zníženie alebo skreslenie syntézy koagulačných faktorov plazmy a krvných doštičiek a zložiek systému kalikreín-kinín;
- inhibícia alebo zvýšená spotreba týchto faktorov;
- zvýšenie endogénnych antikoagulancií;
- aktivácia fibrinolytického systému;
- Predávkovanie antikoagulanciami, fibrinolytickými a defibrinujúcimi liekmi. Toto všetko je základom porušenia jednej z troch fáz krvnej koagulácie a zrážania krvných zrazenín alebo ich kombinovanej zmeny.
Príčiny porušenie prvej fáze zrážania krvi - tvorba tromboplastínu - ich budú produkty redukcia faktorov (IX, X) v patológiu pečene, tvorba protilátok proti niektoré faktory (VIII, IX) v ochorení, patogenézy, ktorý má autoimunitné zložku (leukémia, kolagén) alebo predávkovanie takého univerzálneho antikoagulantu ako heparínu. Existujú genetické chyby v syntéze faktorov VIII, IX a XI, ktorých nedostatok je základom pre vznik hemofílie (sekvencia týchto faktorov je hemofília A, B a C).
Porušenie druhej fázy zrážania krvi - trombínu - dochádza nielen pre choroby pečene, ale aj v hypo- a beriberi K pri znížený príliš syntézu v pečeni faktorov II, V, VII, zapojený v tejto fáze (s obštrukciou, enteritída, rozsiahle resekcia tenkého čreva, liečivá dysbakterióza). Výskyt inhibítorov imunitného faktorov V, VII (napríklad pri liečbe streptomycín sulfátu), zvýšili ich vylučovanie obličkami, dedičným deficitom (faktor V, keď paragemofilii) alebo inaktiváciu komponenty antikoagulačný systém - antitrombínu, heparín (s anafylaktický šok, predávkovanie heparínu).
Hemoragická diatéza spojená s poruchou koagulácie tretia fáza - fáza tvorby fibrínu dochádza znížením syntézy fibrinogénu v infikovaných pečene patologického procesu, svetla alebo v dôsledku dedičné hypo-, afibrinogenemia a fibrinstabiliziruyuschego nedostatočnosť faktora (faktor XIII). Avšak výrazne častejšie je porušenie tretej fázy dôsledkom zvýšenej fibrinolýzy v prípade poranenia (operácie) pľúc, maternice, pankreasu; popáleniny, šok. To je v dôsledku zvýšenej krv vstupuje do aktivátora plazminogénu (plazminogénu) - tkaniva, mikrobiálne fibrinokinaz, leuko- a erytrocytov aktivátory, zložiek kalikreín-kinínového a systém komplementu heparínových komplexy s fibrinogén, plazminogén a adrenalínu (tieto komplexy poskytujú neenzymatické fibrinolýzu B. A . Kudryashov).
Patogenéza. Hlavný odkaz v patogenéze hemoragickej diatéza, ktorý sa vyvíjal v rozpore s niektorou z fáz zrážania krvi, je chronické strate krvi a jeho následkov, rovnako ako štrukturálne a funkčné zmeny v mieste krvácania (v kĺboch, vnútorných orgánov, kože a iných tkanív).
Zvýšená koagulácia krvi
Zvýšenie koagulácie krvi sa prejavuje lokálnou (trombózou) alebo generalizovanou intravaskulárnou krvnou koaguláciou, ktorá je založená na porušení trombocytárnej a koagulačnej hemostázy.
Hyperkoagulácia môže byť spôsobená:
- zvýšenie funkčnej aktivity krvného koagulačného systému v dôsledku zvýšeného príjmu prokoagulancií a aktivátorov zrážania krvi do krvi;
- zvýšenie obsahu krvných doštičiek;
- zníženie antitrombotických vlastností cievnej steny;
- zníženie aktivity krvného antikoagulačného systému;
- oslabenie fibrinolýzy.
Všeobecnej (rozšírené) intravaskulárna koagulácia (DIC), - závažná porucha hemostázy, ktorý sa vyskytuje pri prekročení bezprostrednej krvný procoagulants a aktivátory koagulácia, ktoré vedú k tvorbe viac mikrotrombov v cievach mikrocirkuláciu a potom vývoj hypocoagulation, trombocytopénia a krvácanie vedie "spotreba" faktorov koagulačného systému a zvýšenie funkčnej aktivity systému antikoagulácie a fibrinolýzy krvi, po ktorom nasleduje vyčerpanie všetkých t EX systémy.
Etiológie. Univerzálnosť a nešpecifikácia DIC je spôsobená rôznorodosťou kauzálnych faktorov jeho výskytu. Patrí medzi ne predovšetkým zovšeobecnené infekcií a septických stavov, všetky druhy šoku, úrazovej chirurgie, pôrodníckej patológie (predčasné odlúčenie, ručné odstránenie placenty), akútna intravaskulárnej hemolýzy, urémia v zlyhanie obličiek, všetky koncové stavy.
Patogenéza. Hlavný odkaz v patogenéze generalizované hyperkoagulovatelné je nerovnováha medzi kalikreín-kinínového, koagulácie, antikoagulačnej a fibrinolytického systému v krvi pri vstupe do krvného obehu veľké množstvo prokoagulačnej a aktivátorov. To vedie k narušeniu krvi tak dôležitú funkciu ako zachovanie normálneho stavu agregácie, čo vedie k fáze hyper koaguláciu krvných zrazenín v cievach a zastaví jej pohyb s rozvojom ťažkých degeneratívnych a funkčných porúch v orgánoch a tkanivách sú často nekompatibilné so životom. V následnej fáze hypokoagulácie spôsobuje krvácanie a strata schopnosti zrážať a agregovať krvné doštičky krvácanie, čo je zle prístupné terapeutickej korekcii. S priaznivým výsledkom tretí príde - fáza obnovy, pri ktorej sa normalizuje hemostáza.
 Anglická abeceda s prepisom
Anglická abeceda s prepisom Výber najlepšieho mixu pre slabé a predčasne narodené deti
Výber najlepšieho mixu pre slabé a predčasne narodené deti Saturnove astronomické údaje
Saturnove astronomické údaje