Нарушаване на хемостазата. Изчерпване на коагулационните фактори. в) тежко увреждане на черния дроб

ПАТОФИЗИОЛОГИЯ НА ХЕМОСТАЙСКАТА СИСТЕМА
Стойността на хемостатичната система
1. Запазване на кръвта в течно състояние (адекватно съотношение на активността на системите на коагулация и антикоагулация)
2. Предотвратяване и спиране на кървенето (поддържане на постоянен циркулиращ кръвен обем)

ВИДОВЕ ХЕМОСТАЗА
Съдова-тромбоцитите
(Първоначално)
- СПИРАЧНО ЗАБАВЯНЕ В МИКРО КОРАБИ
коагулацията
(Вторичен)
ФОРМИРАНЕ НА ОПАКОВКИ ЗА ФИБРИРАНЕ

КОМПОНЕНТИ НА ХЕМОСТАЙСКАТА СИСТЕМА
* ВАСКУЛАРНА СТЕНА
* Тромбоцитите (моноцити, еритроцити)
* ПЛАЗМА СИСТЕМИ:
- PROKOAGULYANTY
- Антикоагуланти
- FIBRINOLYTIC
- КАЛИКРЕЙН-КИНИНОВАЯ

КЛАСИФИКАЦИЯ НА ХЕМОСТАЙСКИТЕ ПРОБЛЕМИ
ЗА ЕТИЛОГИЯ
- ХЕРЕДИТАР
- придобити
ЗА МЕХАНИЗМА ЗА РАЗВИТИЕ
- ВЪЗДУХОВНИ ТРУДОВЕ
хемостаза
- Разстройства на коагулационната хемостаза
ЗА ПОЯСНЕНИЕ НА ПРОМЕНИТЕ
- Хипокоагулация
- ХИПЕРКАГУЛАЦИЯ

gipokoagulyatsii
Намалена способност на кръвта да се съсирва с тенденция към повторно кървене и кръвоизлив (спонтанно или след леки наранявания)

етиология
1. ТРОМБОЦИТОПИЯ
2. тромбоцитопатии
3. Васопатия
4. COAGULOPATHY

тромбоцитопения
Патологично състояние, характеризиращо се с намаляване на броя на тромбоцитите в кръвта. (по-малко от 150 · 109 / l)

ХЕРЕДИТАРНА ТРОМБОЦИТОПЕНА
Като правило то се съпровожда едновременно с необичайни дефекти на тромбоцитите

ПРИДОБИВАНА ТРОМБОЦИТОПЕНА (КЛАСИФИКАЦИЯ ПО РАЗВИТИЕВ МЕХАНИЗЪМ)
УВРЕЖДАНЕ НА ПЛАТЕВЕТЕ
- имунни комплекси
- механична травма (спленомегалия, хемангиома)
ПОДГОТОВНО ТРЪБНО ОБУЧЕНИЕ
(апластична анемия, химическо и радиационно увреждане на червения костен мозък, замяна на хематопоетична тъкан с тумор)
УВЕЛИЧАВАНЕ НА ПОЛЗВАНЕТО
(тромбоза, DIC)

Имунна тромбоцитопения
GETEROIMMUNNAYA
* Появява се по-често в деца
** причина - промени в антигенната структура на тромбоцитите (когато рубеола, едра шарка, аденовирусни вируси изчезнат, получени от лекарства хаптени - хинидин, сулфонамиди, рифампицин, ваксини)
***Положителен курс (ако причината се елиминира, възниква пълно възстановяване)

Имунна тромбоцитопения
АВТОИМУНЕН
Появява се по-често в възрастни
причина - липса на имунна толерантност към антигените на собствените тромбоцити
Провокативни фактори: лекарства, вируси, бактерии

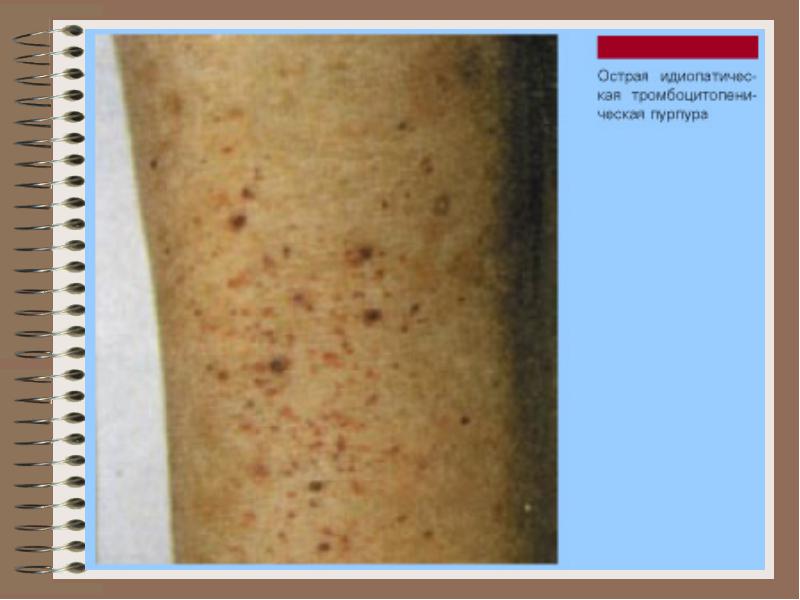
Автоимунна тромбоцитопения
ВЕРЛЕОФОВ ЗАБОЛЯВАНЕ
(автоимунна хронична тромбоцитопенична пурпура)
* На броя на плочите на тромбоцитите IgG увеличава 10 пъти
* Основното място на синтеза на IgG е далак
* Принцип на лечение:
- спленектомия
- кортикостероиди
- имуносупресори
* Няма пълно лечение.

thrombocytopathy
Нарушена хемостаза поради качествена непълноценност или дисфункция на тромбоцитите, която се характеризира с нарушение на хемостазата на кръвоносните съдове, появата на кървене от тъкани и органи

БЕЗ НАРУШАВАНЕ НА РЕАКЦИЯТА НА ГРАНУЛИТЕ ЗА ЛИБЕРИЯ
Глантсман Тромбастия
* Наследяване - автозомно рецесивно
*причина - отсъствието на гликопротеини 2b и 3а в обвивката на тромбоцитите
*патогенеза- тромбоцитите не взаимодействат с фибриноген и не се агрегират
*Симптоми: петехии, кървене от носа, кървене от матката ( може да бъде смъртоносен!)

Наследствена тромбоцитопатия
С НАРУШАВАНЕ НА РЕАКЦИЯТА НА ГРАНУЛИТЕ
наследяване - автозомно рецесивно
причина - нарушена активност на циклоксигеназата, ниска активност на контрактилния белтък
патогенеза - липса на агрегация при взаимодействие с колаген, липса на освобождаване на гранули
Симптоми:

Наследствена тромбоцитопатия
С НАРУШЕНИЕ И ОСВОБОЖДАВАНЕ НА СЪДЪРЖАНИЕТО НА ГРАНУЛИТЕ
Болест на Herjman Pudlak (AR)
* причина - нарушаване на натрупването на плътни гранули (ADP, адреналин, серотонин, Са2 +)
* патогенеза - няма агрегация в взаимодействието с колаген, не се отделя съдържанието на гранулите
* Симптоми: петехии, кървене от носа, кървене от матката

Наследствена тромбоцитопатия
С НАМАЛЯВАНЕ НА АГРЕГАЦИЯТА НА АДЕЗИЯТА И ПЛАСТИЛАТА
Синдром на Von Willebrand-Jurgens (AR)
причина - Дефицит на фактор на Willebrand
патогенеза - нарушената адхезия на тромбоцитите поради дефицит на фактор 8
Болест на Бърнард Сул (AR)
причина - липса на гликопротеин 1 върху тромбоцитите
патогенеза - взаимодействието на тромбоцитите с фактор von Willebrand, f. 5, f. 11
Знаци на - капилярно кървене ( особено опасни по време на пубертета или раждането)

Наследствена тромбоцитопатия
НЕФИЦИАЛНОСТ И НАМАЛЕНА НАСТРОЙКА f.3
Тромбоцитопатия Bowe и Овен
причина - дефицит f.3 тромбоцити
патогенеза - няма взаимодействие между тромбоцитите и прокоагулантите
Симптоми: петехии, кървене от носа, кървене от матката

Наследствена тромбоцитопатия
Тромбоцитопатия, комбинирана с други наследствени аномалии
Синдром на Whiskott-Aldridge
- причина - в тромбоцитите има малко плътни гранули (ADP, серотонин, адреналин, Ca2 +), алфа гранули (бета-тромбоглобулин, фибриноген, фибронектин, растежен фактор)
- патогенеза - намалена адхезия и агрегация на тромбоцитите, освобождаването на гранули е нарушено
- Симптоми:хеморагичният синдром настъпва рано, може да има фатално кървене

Придобита тромбоцитопатия (етиология)
1. левкемия- малко гранули в тромбоцитите, дължащи се на ускорено зреене, намалена адхезия и агрегация
2. НатрупайтеIg M - увреждане на рецепторите от имунни комплекси, нарушаване на взаимодействието на тромбоцитите с прокоагуланти (имунни заболявания)
3. хиповитаминоза Б12 - разрушаване на освобождаването на гранулите
4. Ефекти на медикамента

Лекарствена тромбоцитопатия
* И инхибитори на синтеза на тромбоксан А2
стероидни противовъзпалителни лекарства
- нестероидни противовъзпалителни средства (аспирин блокира тромбоцитната агрегация за 4-6 дни)
* Обучаващи стимулатори cAMP
-papaverin
- еуфилин
- анаболни стероиди
* Ca йон антагонисти
-verapamil
-korinfar

VAZOPATIYA
Хеморагична диатеза, дължаща се на функционален и морфологичен дефицит на съдовата стена
- вродени
- придобит

КОРОНА ВАСОПАТИЯ
Бол. Ранду-Ослер (хеморагична телангиектазия)
Бол. Fabry (дифузен ангиокер-том на багажника)
Наследствена тромбоцитопенична микроангитоматоза

КОРОНА ВАСОПАТИЯ
причина - наследствено нарушение на развитието на съединителната тъкан, вкл. съдов суандотелиум
особеност
- фокално съдово изтъняване
- разширяването на лумена на микроелементите
- малки колагенови влакна в суандотела
- плавателните съдове са лесно ранени
- лоша адхезия и агрегация на тромбоцитите поради липса на колагенни влакна
**Знаци на - назално, белодробно-бронхиално и стомашно-чревно кървене (има фатален край)

ПРИДОБИВАНА ВАСОПАТИЯ
1. И diopaticheskaya (Сарком на Kaposi)
- етиология - неизвестна
2. застоял (дерматит Klotza, дерматит Favra Rakusho)
- етиология - хронична сърдечна недостатъчност, локална венозна недостатъчност
3. дистрофията на
Стероидна пурпура - хиперфункция на надбъбречните жлези, лечение с кортикостероиди - инхибират синтеза на колаген
Скачане - недостиг на Vit.S
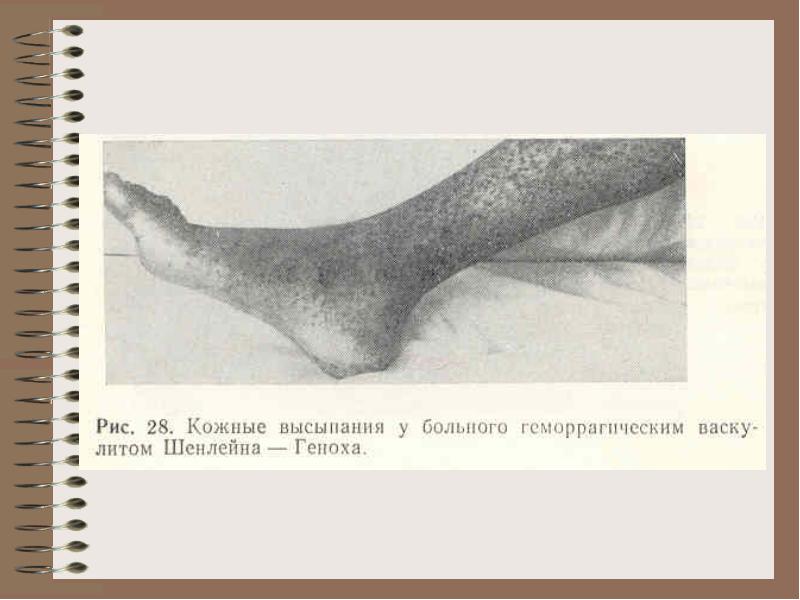
Bol.Shenlein-Genokha - съдови увреждания от имунни комплекси
4. неврогенен
Клинични признаци - кожни форми на кървене

коагулопатия
Хеморагична диатеза, която се появява в резултат на патологията на коагулационната система на хемостазата
** наследствен
** придобити

Наследствена коагулопатия
Генетично причинено коагулационно нарушение, дължащо се на дефицит или молекулярна аномалия на вещества, отговорни за хемостазата на коагулацията

Наследствена коагулопатия
КЛАСИРАНЕ
1. Коагулопатия поради изолирано нарушение на вътрешния механизъм на образуване на протромбиназна активност (хемофилия А, В, С, Willebrand b., Дефицит на Hageman)
2. Коагулопатия поради изолирано нарушение на външния механизъм на образуване на протромбиназна активност (хипопроконвертинемия - дефицит от 7 л)
3. Комбинираното нарушение на външния и вътрешния механизъм на образуване на протромбиназна активност (парахемофилия - недостиг от 5 lb., b.Steuart-Prouer - дефицит от 10 lb.)
4. Нарушаване на крайния стадий на коагулация на кръвта (афибриногенемия)

СТАТИСТИКА
Сред всички форми на коагулопатия страдат:
Хемофилия А 68 - 78%
B , Willebrand 9 - 18%
Хемофилия В 6 - 13%
Хемофилия С, парахемофилия и хипопроконвертинемия 1 - 2%
Останалите форми - клинична казурия

Хемофилия А
Хеморагична диатеза поради наследствен дефицит на прокоагулантната част на фактор 8
Фактор 8 (протеин с високо молекулно тегло)
1. Грокопротеин прокоагулант (VIII: К)
2. Гликопротеин, осъществяващ адхезията на тромбоцитите (VIII: FV)
3. Гликопротеин, активиращ адхезията на тромбоцитите под въздействието на ристомицин (VIII: Rkoff)
4. Антигенен маркер VIII: К (VIII: K AG)
5. Антигенен маркер VIII: Rkof (VIII: Rkof AG)
Дейност VIII: К и VIII: PV намалява с намаляваща мултимерна структура и само 8 фактора

Хемофилия А
* Ей tiologiya - генна аномалия в хромозомата X, която контролира синтеза прокоагулантна част f. 8 (Viii: k)
** III - мъже (46, XhY)
** видове
- Хемофилия А + (антиген-позитивна форма - аномална е синтезирана VIII: К), 8-10% страдат
- Хемофилия А- (негативна антиген-не синтезирана VIII: К), 90-92% страдат
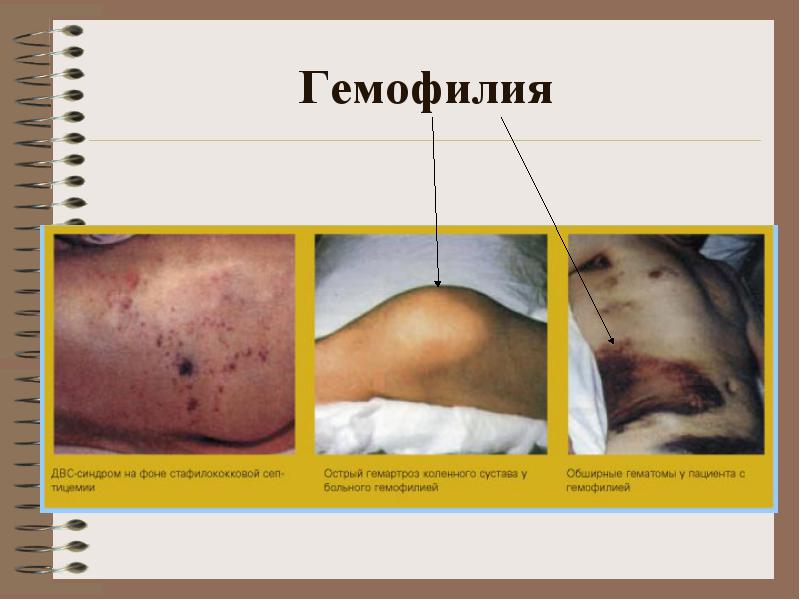
**** клиника: кръвоизливи в големи стави, хематоми (подкожно, интрамускулно), тежко и продължително посттравматично кървене. Възможно кървене в коремните органи, стомашно-чревно кървене

хемофилия
хемофилия
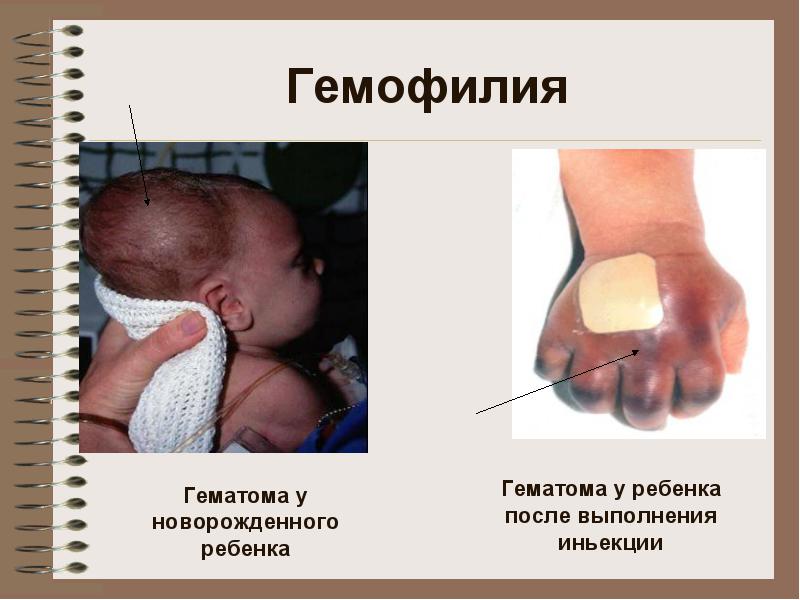
Хемофилия Б
етиология - геномна аномалия в хромозомата X, която контролира синтеза на f. 9
Болни - мъже (46, XhY)
- жени (46, XhXh), (45, Xh O)
*** Изгледи
- Хемофилия В + (синтезирана е антигенна положителна форма - аномална) е. 9)
- Хемофилия В- (антиген-отрицателна форма - не е синтезирана е. 9)
клиника: кръвоизливи в големи стави, хематоми (подкожно, интрамускулно), тежко и продължително посттравматично кървене. Възможно кървене в коремните органи, стомашно-чревно кървене

ПОЛУЧАВАНА КОУГАЛОПАТИКА
особеност - полидефицитен
етиология
1. Имунно инхибиране на прокоагуланти (конфликт на резус)
2. Липса на вит. К-зависими коагулационни фактори (7, 10, 9, 2)
а) увреден синтез в червата (дисбактериоза, диария)
б) нарушение на усвояването на вит. К (дефицит на жлъчка)
в) тежко увреждане на черния дроб
3. Предозиране на хепарин

хиперкоакулационна
УВЕЛИЧАВА КАПАЦИТЕТ НА КРЪВТА, ЗА ДА СЪЩЕСТВУВА БУТИКАТА В КОРАБИТЕ
тромбоза
DIC

ДИК-СИНДРОМ (СИНДРОМ НА ОТКАЗАНА ВЪВЕДАКУЛАРНА КОЛАГАЦИЯ НА КРЪВ)
КЛАСИРАНЕ
* Според клиничния курс
1) остри (мигновени форми се характеризират с тежък курс)
2) хроничен
* По разпространение
1) локализиран
2) генерализирана

етиология
Инфекции, септични условия
шок (със септична смъртност от 100%)
Хирургични интервенции, изгаряния
Всички терминални условия, сърдечен арест
Остра интраваскуларна хемолиза
Патология на акушерството (20-25%)
Хемобластоза (с левкемия - 33-45%)
Разрушителни процеси в паренхимни органи
Алергични реакции

Етапи на DIC
1) Хиперкоагулация (образуване на множество кръвни съсиреци, дължащи се на активиране на коагулационната система)
2) Консумирана коагулопатия (изчерпване на коагулиращата система, прекомерно използване на тромбоцитите за образуване на кръвни съсиреци)
3) Хипокоагулация (понижаване на активността на коагуланти, активиране на антикоагуланти, активиране на фибринолиза)
4) Завършване (възстановяване, усложнения, смърт)

Патогенеза на DIC
1) хипертромбинемия (тромбопластинът влиза в кръвта в големи количества от увредени тъкани и спомага за образуването на тромбин). При инфекциите, активираните макрофагови моноцити синтезират своите коагуланти (f.7, f.10, f.9, f.2)

Патогенеза на DIC
2) Масивна агрегация на тромбоцитите (причинява развитие на консумация на тромбоцитопения и усложнени от кръвоизливи)
3) Травма и хемолиза на еритроцитите (това води до много ADP, което увеличава адхезията и агрегацията на тромбоцитите)

Патогенеза на DIC
4) "Хуморна протеаза експлозия" (при активиране на прокоагуланти, антикоагуланти, фибринолитици, протеини на системата каликреин-кинин, системата на комплемента в кръвта, се натрупват много протеинови разпадни продукти, които са много токсични и увреждат кръвоносните съдове и тъканите)

Патогенеза на DIC
5) Изчерпване на системата за фибрино-лизинг
(допринася за тромбоза)
6) Изчерпване на коагулационните фактори в кръвта
(причиняват развитие на кръвоизливи)

Клиника на ДИК
1. Шоко за хемокоагулация
причината
* нарушения на микроциркулацията (причиняват развитието на тъканна хипоксия)
* натрупване на токсични продукти от протеолиза
проявления
* понижаване на кръвното налягане
* понижаване на централното венозно налягане
* кървене (предизвиква хеморагичен шок)

Клиника на ДИК
2. Хемостатични нарушения
а) хиперкоагулация
Основната проява е тромбоза.
Кръвта коагулира in vitro
б) hypocoagulation
Основното проявление е кървене
(в същото време системата на фибринолизата е изчерпана)

Клиника на ДИК
3. тромбоцитопения
Това се дължи на образуването на голям брой кръвни съсиреци в съдовете (консумация на тромбоцитопения)

Тази група включва генетично определени хипокоагулации, характеризиращи се с дефицит, както и с молекулярни аномалии на коагулационни фактори.
По този начин 83-90% от всички наследствени нарушения на кръвосъсирването са 2 вида фактор на дефицит на фактор VTII хемофилия А (70-78%) и болестта на фон Вилебранд (9-18%); други 6-13% са свързани с дефицит на фактор IX (хемофилия В). По този начин дефицитът само на два коагулационни фактора - VIII и IX - представлява около 96-98% от всички наследствени коагулопатии. Дефицитът на факторите VII и V се регистрира в 0.5-1.5%, фактор X - в 0.3-0.5% от случаите.
Не всички нарушения в системата за коагулация на кръвта са придружени от кървене: тя може да отсъства или да е лека.
Хемофилия А. Това заболяване е най-честата коагулопатия, която се основава на дефицит на фактор VІІІ (антихемофилен глобулин) и е единственият сред тях с рецесивно X-хромозомно наследство.
Разнообразието от форми на патологията на фактор VІІІ отразява сложността на структурата му. В кръвта фактор VIII циркулира под формата на протеинов комплекс, състоящ се от редица подобни субединици.
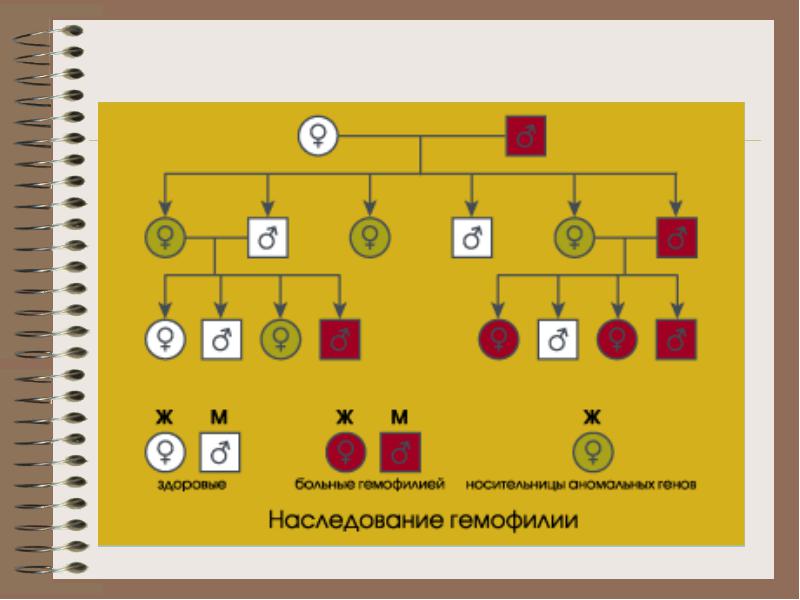
наследяване. Хемофилият ген, разположен в хромозомата X, се наследява от болен човек от всичките му дъщери, които по-късно неизбежно носят болестта, докато синовете на пациента остават здрави (поради факта, че получават Х хромозомата от здрава майка).
Също така трябва да се отбележи, че женски носител на хемофилия има възможност в 50% от случаите да ражда здрав син и половината от дъщерите стават носители на гена на хемофилия.
Женските носители по принцип не страдат от кървене, тъй като втората нормална хромозома X осигурява синтеза на фактор VІІІ, който в повечето случаи е достатъчен, за да осигури хемостаза.
Въпреки това, процентът на фактор VІІІ варира в много големи граници (60-250%). В това отношение, при някои предаватели нивото на фактор VІІІ в плазмата може да бъде 11-20%, което създава риск от кървене от наранявания, операции и раждане. Лекарят трябва да помни за тази опасност по време на хирургични интервенции при майките, сестрите и особено дъщерите на пациентите с хемофилия. Преди операцията и преди раждането те трябва да проверят нивото на фактор VІІІ в плазмата и, при скорости под 25%, да предложат профилактично криопреципитат при 7-10 U / kg на ден.
Откриването на генния носител на хемофилия се улеснява от подробно изследване на фамилната хеморагична история във всички кръвни роднини на майката на пациента.
Наследственият генезис се установява при хемофилия А в 70-75% от случаите, а при хемофилия В - при 90-91%. Генът на хемофилия А несъмнено често мутира, тъй като броят на пациентите не е намалял в продължение на много векове, въпреки че доскоро значителна част от тях са починали преди достигане на детеродна възраст, което е довело до естествения спад на анормалните Х хромозоми.
Симптоми на нарушения на коагулационната хемостаза
Тежестта на кървенето зависи от дефицита на фактор VІІІ в плазмата, чието съдържание в различни хемофилни семейства е генетично програмирано.
Нивото на факторите с ясен антихемофилен ефект (VIII или IX), вариращо от 0 до 1%, причинява изключително тежък ход на разглежданата патология, нивото на факторите от 1 до 2% причинява тежки, от 2 до 5% умерени и над 5% лесен ход на заболяването. В последния случай съществува вероятност от кървене, което представлява сериозна опасност за живота на пациента, което е от особено значение при провеждане на различни хирургични интервенции или в случай на нараняване.
Клиничната картина на хемофилия е доминирана от кръвоизливи в големите стави на крайниците, дълбоки подкожни, между мускулни и интрамускулни хематоми, тежко и продължително кървене с наранявания, хематурия (появата на кръв в урината). Други кръвоизливи се наблюдават по-рядко, включително тежки и опасни, като ретроперитонеални хематоми, кръвоизливи в коремните органи, стомашно-чревни кръвоизливи и вътречерепни кръвоизливи.
Има ясна еволюционна еволюция на проявите на болестта. При раждането могат да се наблюдават повече или по-малко разширени цефалматоми (кръвоизлив под перитостта на костите на черепа), подкожни и интрадермални кръвоизливи, късо кървене от пъпна връв. Понякога заболяването се открива по време на първото мускулно инжектиране, което може да причини голям, животозастрашаващ междумускулен хематом. Честито често е придружено от не много тежко кървене.
През първите години от живота често има кървене от лигавиците на устната кухина, което се свързва с нараняване на различни остри предмети. Когато детето се научи да ходи, падането и натъртванията често се съпътстват от обилно кървене от носа и хематоми по главата, кръвоизливи в окото, както и след орбитални хематоми, което може да доведе до загуба на зрение. Детето започна да пълзи, типично кървене в областта на бедрата.
След това се стига до предни кръвоизливи в големите стави на крайниците. Остри кръвоизливи в ставите изглеждат по-ранни, по-тежката хемофилия. Първите кръвоизливи предразполагат към повтаряне на същите стави. При всеки пациент с особена устойчивост и честота се засягат кръвоносните съдове на съединението I - III. Това се дължи на морфологично преструктуриране и вторични възпалителни промени в тъканите на ставата.
Установено е, че синовиалната мембрана е основният и евентуално единственият източник на кръвоизлив в ставата, тъй като след пълна синьоктомия (отстраняване на синовиалната мембрана) такива кръвоизливи са повтарящи се и не се повтарят. Най-често засегнатите стави на коляното, последвани от глезена и лакътя, а след това със значителна хълбока. Кръвоизливи в малките стави на ръцете и краката (по-малко от 1% от всички лезии) и междузвездните стави са относително рядко наблюдавани. В зависимост от възрастта и тежестта на заболяването, всеки пациент е засегнат от ставите I - II до VIII - XII.
Клинично важно е да се разграничат остри кръвоизливи в ставите (първични и повтарящи се), хронична хеморагично деструктивна остеоартроза (артропатия), вторичен имунен ревматоиден синдром като усложнение на основния процес.
Остра хемартроза - внезапният вид (често след малка травма) или рязко увеличаване на болката в ставата. Кожата на ставата е червена и гореща на допир. Болката бързо (в рамките на няколко часа) се облекчава след първата трансфузия на криопреципитат или антихемофилна плазма и почти веднага изчезва, като едновременно с това се отделя кръвта от ставата. Ако синдромът на болката с това лечение не се елиминира, трябва да се потърси допълнителна патология - вътрешно-ставна фрактура, разкъсване на кондила, задържане на тъканта.
Остеоартрозата се разделя на етапи въз основа на клинични и радиологични данни. При класификацията се разграничават 4 стадия на увреждане на ставите.
В първия или по-ранния стадий обемът на ставата (с разширение на пространството на ставата) в резултат на кръвоизлив може да се увеличи. В "студения" период функцията на ставата не се нарушава, но чрез радиография, уплътняването и удебеляването на ставната капсула могат да бъдат открити поради инфилтрация с хемоидерин.
В стадий II се проявяват типични промени в секвенцията на подкарпауса на епифизите - модели на ръба, образуване на единични овални малки клетъчни разрушения и кисти. Остеопорозата е по-изразена, съединението се запазва, но може да бъде умерено стеснено.
В стадий III, ставата е рязко уголемена, деформирана, има неравномерна и неравномерна структура и се определя изразено мускулно изхабяване. Мобилността на засегнатите стави е повече или по-малко ограничена, поради както увреждането на самата връзка, така и промените в мускулите и сухожилията. Радиографски, ставите са удебелени, рязко деформирани, ставните повърхности са сплескани, епифизите са увеличени поради нарастването на костната тъкан, диафизата е намалена, съединението е стеснено. Остеопорозата се проявява, вътреартикуларните фрактури се появяват лесно. В бедрената кост, кървене-подобно или тунелно-подобно разрушаване на костната субстанция в областта на междуспиналната фиша е типично за хемофилия. Пателата е частично унищожена. Вътре-ставния хрущял е разрушен, подвижните, често разбити фрагменти от тези хрущяли, често вложени в стари организирани кръвни съсиреци, се намират в ставната кухина. Има различни видове подкладация и изместване на костите.
В стадий IV функцията на ставата е почти напълно изгубена, пространството на ставите е стеснено, лошо визуализирано на рентгеновата снимка и често е обрасло с съединителна тъкан. Склерозата на перинеалните части на костта се изразява в комбинация с образуването на пукнатини и формирането на кисти в епифизите. Възможни патологични вътреракуларни фрактури. Костната анкилоза е изключително рядка и всъщност никога не е наблюдавана, освен ако не е извършено в миналото погрешно лечение (при продължително обездвижване на крайниците).
С възрастта тежестта и разпространението на ставните лезии постоянно напредват и се влошават от появата на периартикуларни хематоми.
Вторичният ревматоиден синдром (Barkagan синдром - Egorova), първоначално описан от авторите през 1969 г., е често срещана форма на увреждане на ставите при пациенти с хемофилия. В много случаи се вижда, защото е наслоен от предишни кръвоизливи в ставите и деструктивни процеси в ставите, присъщи на хемофилията. Внимателното изследване на пациентите улеснява диагностицирането на вторичен ревматоиден синдром, което е от съществено значение за по-нататъшното правилно лечение. Този синдром е придружен от хроничен възпалителен процес (често симетричен) в малките стави на ръцете и краката, които преди това не са били засегнати от кръвоизливи, с последващата им типична деформация, болка в големите стави, които не спират и често се влошават след плазмени трансфузии и инжекции с криопреципитат. Също така, този синдром се проявява с изразена сутрешна скованост в ставите, постоянна прогресия на ставния процес от допир с пресни кръвоизливи, появата или рязкото увеличаване на лабораторните признаци на възпалителния процес, включително имунологични, с повишаване на серумните глобулини, сиаловите киселини, фибриногена, повишаване на концентрацията на циркулиращи имунни комплекси и, в някои случаи, титър на ревматоиден фактор. При мнозинството от пациентите синдромът се появява на възраст 10-14 години, до 20-годишна възраст честотата му достига 5,9%, а с 30 години - до 13%.
С възрастта разпространението и сериозността на всички лезии на ставите непрекъснато се развиват, което води до увреждане, принуждавайки пациентите да използват патерици, инвалидни колички и други устройства.
Прогресия на ставното увреждане зависи от честотата на остро кървене в ставите, бързина и полезността на тяхното лечение (много важно за началото на преливане на кръв), качество ортопедични грижи за пациента, подходящо използване на физическа терапия, физиотерапия и спа влияе кариера избор и редица други обстоятелства. Понастоящем всички тези въпроси са изключително важни, тъй като продължителността на живота на пациентите с хемофилия, дължаща се на успеха на лечебната терапия, се е увеличила драстично.
Следните видове обширни и напрегнати хематоми са доста трудни и опасни за пациента: подкожно, мускулно, субфаскално и ретроперитонеално. Постепенно се увеличават, те могат да достигнат огромни размери, да съдържат 0,5-3 литра кръв и повече, да доведат до развитие на анемия при пациентите, да причинят компресия (компресия) и разрушаване (унищожаване) на околните тъкани и съдовете, които ги хранят, некроза. Например, ретроперитонеалните хематоми често разрушават големи участъци от тазовите кости (диаметърът на зоната на разрушаване е до 15 см или повече), хематомите по краката и ръцете разрушават тубуларните кости, петата на костите. Смъртта на костната тъкан също причинява кръвоизливи под периоста. Това разрушаване на костите при рентгенографията е подобно на разрушаването на тумора (например при остеосаркоми). Хематомите често се калцифицират и понякога водят до образуване на нови кости (остеонегенеза). Те могат да затворят ставите и да ги имобилизират напълно.
Много хематоми, оказващи натиск върху нервните шини или мускулите, причиняват парализа, увредена подвижност, чувствителност, бързо прогресивна мускулна атрофия. При кръвотечение в областта на мускулите на iliopsoas, особено гъвкави са движенията на бедрото на бедрото. Особено внимание се обръща на тези хематоми, които могат да причинят развитие на стеноза на горните дихателни пътища. Такива хематоми включват хематоми на меките тъкани на субмандибуларния регион, хематоми на шията, фаринкса и фаринкса.
14-30% от всички пациенти с хемофилия развиват обилно и продължително бъбречно кървене, което представлява сериозна заплаха за живота на пациента и е трудно за лечение. Такова кървене може да възникне както спонтанно, така и във връзка с увреждания на лумбалната област, свързана с пиелонефрит, и вероятно поради повишена екскреция на калций в урината поради разрушаване на костната тъкан при пациенти с хемофилия. Аналгетици (ацетилсалицилова киселина и т.н.), изобилие от кръвопреливане и плазма, водещо до развитие на вторична тромбоцитопатия поради допълнителен отрицателен ефект върху бъбреците, могат да допринесат за появата или подобряването на такова кървене. Бъбречно кръвоизлив често предхожда от дълго microhematuria (малък брой червени кръвни клетки в урината) и който се записва в интервалите между епизоди macrohematuria (голям брой червени кръвни клетки в урината, забележим на окото).
Появата на кръв в урината често се съпровожда от тежки дисурични събития, припадъци от бъбречна колика, поради образуването на кръвни съсиреци в уринарния тракт. Тези явления са особено интензивни и изразени в лечението на пациенти, когато временно се възстанови нормалната хемостаза. Прекратяването на хематурията често се предхожда от бъбречна колика и често - временното отсъствие на урина с азотемия.
Бъбречно кървене податливи на подновено, че през годините може да доведе до сериозни дегенеративни разрушаване промени в този орган, вторична амилоидоза инфекция и смърт от уремични (вкарване метаболитни продукти в изходяща скорост на урина в кръвта).
Голямото кървене от стомашно-чревния тракт при пациенти с хемофилия може да се появи спонтанно, въпреки че в повечето случаи те се провокират чрез приемане на ацетилсалицилова киселина, бутадион и други лекарства. Вторият източник на кървене са клинично изразени или "скрити" язви на стомаха или дванадесетопръстника, както и ерозивен гастрит от различен произход. Въпреки това, понякога се наблюдава дифузно капилярно кървене без никакви разрушителни промени в лигавицата. Тези диапедемични кръвоизливи, при които чревната стена се накисва дълго с кръв, бързо води до анемична кома, остра съдова недостатъчност и смърт.
Кръвоизливът в мезентериума, както и в големия и малкия оментиум, често създават фалшиво впечатление за развитието на пациента на остра хирургична патология на коремните органи, като остър апендицит, чревна обструкция, която е особено изразена в случай на кръвоизлив под серозната мембрана в чревната стена. Единствената насока в такива ситуации може да бъде бързата ефикасност на интензивната заместителна терапия. Незабавното начало на такава терапия се препоръчва във всеки случай - както за елиминиране на кървенето, така и за подготовка на пациента за операция. След това всичко се определя от резултата от лечението. Ако след инжектирането на концентрат на фактор VІІІ (или IX) синдромът на болката и други признаци на остра коремна кожа бързо намалеят, пациентът може да продължи да бъде наблюдаван, докато продължава интензивната заместваща терапия (неусложнена вътрешна хеморагия). Ако ефектът от заместителната терапия не е достатъчен, тогава е необходима хирургична интервенция.
Хеморагиите в мозъка и гръбначния мозък и техните мембрани при хемофилия почти винаги се свързват или с наранявания, или с употребата на лекарства, които нарушават хемостатичната функция на тромбоцитите. Между момента на нараняване и развитието на кръвоизлив може да има светъл период от 1-2 часа до ден.
Характерният симптом, който отличава хемофилията от друга патология, е продължителното кървене в случай на нараняване и операция. Разкъсаните рани са много по-опасни от линейните разкъсвания. Кървенето често не се случва веднага след нараняване, но след 1-5 часа
Тонсилектомията (отстраняване на сливиците) за хемофилия е много по-опасна от коремна хирургия.
Извличането на зъбите, особено коренните, често е придружено от няколко дни анемизиращо кървене не само от дупки в зъбите, но и от хематоми, образувани на мястото на тъканна инфилтрация с новокаин. Тези хематоми причиняват разрушаване на челюстта. При хемофилия зъбите трябва да се отстранят на фона на действието на антихемофилни лекарства под обща анестезия. Премахването на няколко зъба се извършва най-добре едновременно.
Някои от усложненията на хемофилията се дължат на загуба на кръв, компресия и разрушаване на хематомни тъкани и хематомна инфекция. Голяма група от усложнения се свързват и с имунни нарушения. Най-опасната от тях е откриването в кръвта на пациенти с голям брой антитела срещу коагулация с фактор VІІІ (или IX), модифициращи хемофилия в така наречената инхибиторна форма, при която основният метод на лечение - трансфузионна терапия - почти губи своята ефективност. Нещо повече, повтарящото се приложение на антихемофилни лекарства често води до бързо увеличаване на броя на тези антитела при пациенти, в резултат на което трансфузионната терапия, която първоначално даде някакъв ефект, скоро става безполезна.
Честотата на инхибиторната форма на хемофилия варира от 1 до 20%, по-често от 5 до 15%. При тежки форми на хемофилия инхибиторите се появяват в кръвта на пациентите несравнимо по-често, отколкото в белите дробове и при тези над 12-годишна възраст - много по-често, отколкото в по-ранна възраст. При инхибиторни форми хемостатичната функция на тромбоцитите е значително понижена, хеморагиите в ставите и кръвта в урината стават по-чести и увреждането на ставите е значително по-високо.
Сред другите имуноалергични разстройства понякога се наблюдават тромбоцитопения, понякога се комбинира с левкопения, автоимунна хемолитична анемия с положителен тест на Coombs, най-еозинофилия, бъбречна амилоидоза.
Диагностика на нарушения на коагулационната хемостаза
Хемофилията се диагностицира при всички пациенти с кръвоизлив от тип хематом и увреждане на опорно-двигателния апарат, както и при продължително кървене по време на операция. За примерен диагноза е от решаващо значение за намаляване на интензитета на откриване на коагулацията (съсирването) на кръвни проби в обща като време на съсирване, активираното парциално тромбопластиново време и тест autokoagulyatsionnom при нормално параметри тромбин и протромбиново време.
За да се определи кои от коагулационните фактори са в недостиг, те прибягват до помощта за корекционни тестове, използващи теста за генериране на тромбопластин или теста за автокоагулация.
Типът хемофилия също може да бъде идентифициран чрез "тестовете за смесване": към плазмата на пациента, който се изследва в различни епруветки, се добавят плазмени проби, в които липсва един от коагулационните фактори (VIII, IX или XI). Липсата на нормализиране на коагулацията в една от епруветките показва дефицит на същия фактор и в двете смесени плазми, т.е. недостатъчност на пациента.
Диагнозата на хемофилия завършва с определянето на дефицита на фактора в количествен смисъл, което е важно за правилната оценка на тежестта на заболяването и заместващата терапия.
Лечение на нарушения на коагулационната хемостаза
Основният метод за лечение и профилактика на хемофилно кървене на всяко място и от всякакъв произход е интравенозното прилагане на достатъчно дози кръвни препарати, съдържащи фактор VIII. Фактор VIII е променлив и практически не се запазва в консервираната кръв, естествената и суха плазма. Само директни кръвопреливания от донор на пациент с хемофилия, както и интравенозни инфузии на кръвни продукти с консервиран фактор VІІІ (антихемофилна плазма, криопреципитат, концентрат на фактор VIII с различно пречистване) са подходящи за заместващо лечение.
Директните дарения от донора се прибягват само когато лекарят няма други антихемофилни лекарства. Грешна грешка е кръвопреливането от майката на пациента, тъй като тя е носителят на заболяването и нивото на фактор VІІІ е рязко намалено.
Поради краткия полуживот на фактор VІІІ в кръвта на пациента (около 6-8 часа) кръвните трансфузии, като трансфузиите на антихемофилна плазма, трябва да се повтарят най-малко три пъти дневно. За да се спре масивното кървене и надеждно да се обхванат различни хирургични интервенции, когато нивото на антихемофилния фактор трябва да се поддържа над 30-40%, такива кръвопреливания и кръвопреливания са неподходящи. Въпреки че времето на съсирване и времето за прекалцификация (насищане с калций) се нормализира при пациенти с хемофилия с повишаване на концентрацията на фактор VIII до 3-4%, това ниво не е достатъчно, за да се предотврати кървенето по време на операциите. Следователно, по време на лечението и предоперативната подготовка, трябва да се фокусира само върху количественото определяне на фактор VІІІ (или върху автокоагулограма), но не и върху показателите за общото време на съсирване, изпитването на протромбиновото потребление и други методи с нисък праг на чувствителност.
Равен обем антихемофилна плазма е приблизително 3-4 пъти по-ефективен от свежата консервирана кръв. При единични дози от 10-15 ml / kg и дневно 30-50 ml / kg, разделени на 3 части (първата доза е 1,5 пъти повече от 2 последователни), антихемофилната плазма ви позволява да поддържате накратко 10-15% ниво на фактор VIII , Основната опасност от това лечение е, че пациентът претоварва кръвообращението на пациента, което може да доведе до развитие на белодробен оток. Използване антихемофилен плазма в концентрирана форма не променя положението, тъй като високата концентрация на инжектира албумин (протеин) предизвиква интензивно движение на течност от тъканите в кръвния поток, при което обем кръв се увеличава по същия начин, както в преливане на нормална плазма разреждане. Концентрираната суха плазма антихемовил има само предимството, че фактор С е по-концентриран в нея и в малък обем се инжектира по-бързо в кръвта на пациента. Сухата анти-хемофилна плазма преди употреба се разрежда с дестилирана вода до 1 / 3-1 / 2 от първоначалния обем. Лечението с антихемофилна плазма е достатъчно за облекчаване на повечето остри кръвоизливи в ставите (с изключение на най-тежките), профилактиката и лечението на незначително кървене.
Най-надеждният и ефективен хемофилизиращ фактор VIII се концентрира. Криопреципитатът остава най-достъпният от тях - плазмените протеини, извлечени чрез охлаждане (крио-утаяване), при които фактор VIII, фибриноген и фактор XIII, но недостатъчен албумин и някои други протеини са достатъчни. Ниското съдържание на албумин в лекарството ви позволява да влезете в кръвообращението на пациентите в много големи количества и да увеличите концентрацията на фактор VIII до 100% или повече, без страх от кръвообращение и белодробен оток. Основният недостатък на криопреципитата е неговата нередност в дейността.
Криопреципитатът трябва да се съхранява при -20 ° C, което затруднява транспортирането. Когато размразяването на лекарството бързо губи своята активност. Тези недостатъци са лишени от суха криопреципитация и съвременни концентрати на фактор VIII. Те могат да се съхраняват в конвенционален хладилник и да се използват на полето.
Количеството на фактор VІІІ, който се съдържа в 1 ml "осреднена" донорна плазма, т.е. плазма със 100% съдържание на антихемофилен глобулин, се приема като единица активност на антихемофилно лекарство.
За задържане на кръвоизливи в ставите и незначително кървене, включително предотвратяването им при извличане на зъбите, обикновено е достатъчно да се повиши нивото на фактор VIII до 15-20%. По-опасното вътрешно и външно кървене, както и развитието на хематоми в меките тъкани изискват поддържане на нивото на фактор VIII над 30-40%, при което криопреципитатът или други концентрати на фактор VIII се прилагат при 20-30 U / kg; за големи операции и наранявания, хематурия и гастроинтестинално кървене, дозата на криопреципитат се повишава до 40-60 U / kg, а в някои случаи и повече.
В същото време прекомерните инжекции на криопреципитат са нежелани, тъй като създават висока концентрация на фибриноген в кръвта, в резултат на което се нарушава микроциркулацията в органите и съществува опасност от тромбоза и DIC.
Честотата на прилагане на антихемофилни лекарства се определя от степента, до която при всяко приложение е възможно да се повиши концентрацията на фактор VІІІ в плазмата. Така че, ако концентрацията на фактора се увеличи до 40%, след 6-8 часа ще падне до 20% и при първоначално увеличение до 120%, нивото от 20% ще бъде достигнато само за един ден. Модерните концентрирани препарати на фактор VІІІ (криопреципитат и т.н.) могат да бъдат ограничени до 1-2 интравенозни инжекции на ден. Достатъчен ефект от заместващата терапия се постига, само ако са изпълнени следните условия: всички антихемофилни лекарства се прилагат интравенозно само в струя в възможно най-концентрирана форма и възможно най-бързо след дезактивирането им без смесване с други инфузионни разтвори. Една от основните причини за неуспеха на заместващата терапия е инжектирането на кръвни продукти, които не повишават нивото на фактор VІІІ в плазмата.
Докато стабилното кървене спира, трябва да се избягва въвеждането на кръвни заместители и кръвопреливания (кръвни продукти), които не съдържат антихемофилни фактори, тъй като това води до разреждане на фактор VIII и намаляване на неговата концентрация.
Ранното отстраняване (аспирация) на кръвта, която се излива в ставата, не само незабавно потиска синдрома на болката, предотвратява допълнително кръвосъсирване в ставата, но също така намалява риска от развитие и бърза прогресия на остеоартрита. За предотвратяване и облекчаване на вторични възпалителни промени след аспирация в кръвта, лекарят предписва въвеждането на 40-60 mg хидро-тизон в ставата. Поддържащата трансфузионна терапия, проведена през първите 36 дни, предотвратява по-нататъшно кървене и ви позволява да започнете по-рано класове по физиотерапия, което допринася за по-бързо и пълно възстановяване на функцията на засегнатия крайник, предотвратява мускулната атрофия.
Движението в засегнатата става трябва да се развива на етапи: през първите 5-7 дни след отстраняването на обездвижващата превръзка се извършват активни движения както в засегнатата става, така и в други стави на крайниците, като постепенно се увеличава честотата и продължителността на упражненията. По-късно, от 6-ия до 9-ия ден, преминават към упражнения, използвайки велоергометри, педални порти за ръце и еластични пръчки. И само на 11-13-ия ден, с цел да се елиминира остатъчната скованост и да се ограничи максималното огъване или неокачествяването, упражненията за пасивно упражнение се извършват внимателно под контрола на антихемофилни плазмени трансфузии или малки дози криопреципитат.
Едновременно с това, от 5-7-ия ден се предписват физиотерапевтични ефекти - хидрокортизонна електрофореза, анодна галванизация.
В случай на кръвоизливи в меките тъкани се изисква по-интензивно лечение, отколкото при кръвоизливи в ставите, при терапия с антихемофилни лекарства. При анемизирането на пациента се предписват допълнителни трансфузии на червени кръвни клетки. Ако се появят признаци на инфекция с хематом, веднага се предписват широкоспектърни антибиотици. Всички интрамускулни инжекции за хемофилия са противопоказани, тъй като могат да причинят обширни хематоми и псевдотумори. Пеницилин и неговите полусинтетични контрацептиви също са нежелателни, защото причиняват дисфункция на тромбоцитите при високи дози и повишават кръвоизливите.
Ранната и интензивна анти-хемофилна терапия допринася за бързото развитие на хематоми. Хематомните пробиви и аспирацията на кръвта трябва да се избягват. Продължете трансфузионната терапия от 5-7 до 14 дни. Обвитите хематоми се отстраняват, ако е възможно, хирургически заедно с капсула под капака на интензивната грижа с концентрации на антихемофилни фактори.
В случай на кръвотечение от носа, лекарят не трябва да прибягва до тесни тампонади, особено в гърба, тъй като веднага след отстраняването на тампоните кървенето при такива пациенти почти винаги се възобновява с още по-голяма сила.
За да се спре носното кървене възможно най-бързо, е необходимо да се приложи антихемофилна плазма, както и антихемофилни лекарства в комбинация с напояване на носната лигавица с аминокапронова киселина, тромбин или адроксон.
Бъбречните кръвоизливи, при които трансфекциите на антихемофилна плазма и ниските дози криопреципитат са неефективни, представляват сериозна опасност за пациентите. Препоръчваните средни дози антихемофилни лекарства (30-40 U / kg) не винаги спират кървенето или ги спират за максимум 1-2 дни. Повишава ефективността на употребата на антихемофилни лекарства преднизон (20-30 mg / ден за възрастни пациенти).
За облекчаване на стомашночревно кървене трябва да се използват големи дози концентрати от антихемофилни фактори заедно с аминокапронова киселина, дози до 0,2 g / kg.
Трябва да се отбележи, че употребата на преднизолон за кървене в стомашно-чревния тракт трябва да се избягва, използването на преднизолон е най-опасно за язвите както на стомаха, така и на дванадесетопръстника.
Трябва да се има предвид, че кървенето от стомаха често се предизвиква от приемането във връзка с болка в ставите, зъбните или главоболие ацетилсалицилова киселина, Brufen, индометацин, бутазолидонов. При пациенти с хемофилия дори единична доза ацетилсалицилова киселина може да причини стомашно кървене.
При профилактиката и лечението на хроничен остеоартрит и други наранявания на опорно-двигателния апарат трябва да се имат предвид различни начини за предпазване на ставите и предотвратяване на наранявания на крайниците. За да направите това, са зашити гумени щитове на коляното, глезените и лактите, всички спортове, свързани със скачане, падане и набиване (включително колоездене и мотоциклетизъм) са забранени. Важна роля играе най-ранното възможно и пълно лечение на остри кръвоизливи в мускулите и ставите, интензивно целогодишно терапевтично упражнение. За тази цел те се състоят от комплекси от атравматични упражнения във вода, от меки подложки и уреди за упражнения - велоергометри, ръчни порти. Класовете трябва да започнат в предучилищна или по-млада училищна възраст, т.е. преди хронична остеоартроза, увреждане на двигателната способност и други тежки заболявания на развитата мускулно-скелетна система.
Цялостното лечение се допълва с физиотерапевтични (високочестотни токове, електрофореза на глюкокортикостероидите) и балнеологични методи на лечение, които включват: калолечение, стъпаловидни бани и бани с радон. При чести и продължителни кръвоизливи в същите стави, избраните методи са лъчетерапията и синьоктомията (отстраняване на синовиалната мембрана на ставата).
Радиотерапията се провежда в единична доза от 25-50 R (за остър кръвоизлив) до 50-100 R за хроничен остеоартрит. Седмите се повтарят след 1-2 дни, като общата доза варира от 400 до 1000 R. При деца под 14-годишна възраст е необходима известна предпазливост поради възможността за увреждане на зоните на растеж на костите и следователно общата доза не трябва да надвишава 400 R. През последните години, и вътрешна експозиция чрез инжектиране на радиоактивни изотопи в ставите.
Синокектомията, извършена чрез единичен разрез, е много ефективен метод за лечение на хемофилни лезии на ставите, предотвратяване на тежък остеоартрит. Този вид лечение елиминира последващите кръвоизливи в действащата става, осигурява запазването на нормалната конфигурация и функция. Този ефект се проявява със сравнително ранна операция - с артроза от І - ІІ степен и с лезии от ІІІ - ІV клас, синьоктомията като правило вече не е подходяща. Подобно на всички други операции, синьоктомията се извършва с използване на криопреципитат или други концентрати на антихемофилни фактори.
Други ортопедични процедури често се представят ahilloplastiku удължаваха кости, за да се възстанови пространството на ставата, в тежки случаи - със сгъстен фуги в нормално положение. Неоценима услуга, докато предоставянето устройства Волкова - Hovhannisyan, Ilizarov и други, осигурява корекция бързо и надеждно, без да е изключително опасен за пациенти с продължително обездвижване на крайниците. Възстановяване на ставното пространство без използването на тези устройства по принцип е почти невъзможно.
С достатъчно криопреципитат заместителна терапия (през първите 7-8 дни - 30-40 U / (кг х ден), а след това - половината количество) при пациенти, предвидени доста надежден хемостаза; кървене и кръвоизлив в местата на спиците не се наблюдават.
Съвременните методи за заместителна терапия и използването на ортопедични устройства коренно промениха прогнозата на костни фрактури при пациенти с хемофилия. Не много отдавна, такива фрактури не оздравяват, често усложнява от фалшиви ставите и дори да доведат до загуба на крайник, а след това под влиянието на големи дози криопреципитатно, а сближаването, както и добри устройства за закрепване на кости е осигурена чрез заздравяване на фрактура в обичайното време бе споменато по-горе.
За изключителни терапевтични предизвикателства включват борбата срещу остеопороза, кисти и вътрекостно псевдотумор които нямат склонност към osumkovaniyu. Тези процеси дават сериозни усложнения, а понякога са принудени да прибягват до ампутация.
Лечение на усложнена хемофилия. Най-опасни е откриването в кръвта на пациенти с хемофилия голям брой антитела срещу фактор VIII, които определят инхибиторна трансформация хемофилия форма. Инхибиторът може да инактивиране на много голямо количество прилага фактор VIII от външната страна, и следователно първично лечение - заместването преливане терапия - са неефективни или стане напълно неефективно.
В процеса на преливане терапия (с 4-6-ти ден) антитяло титър може да се повиши.
Ако е необходимо заместителна терапия по здравословни причини, е временно не може да се преодолее ефекта на прилагане на антитяло на огромни количества на фактор VIII концентрат (500-1000 U / кг), или плазмафереза (отстраняване на пациент с няколко литра плазма го заменя с прясна антихемофилен) заедно с фактор VIII инжекции megadoses ,
По-обещаващо е използването на така нареченото байпас лечение в инхибиторната форма на хемофилия А - приложението на концентратите IX, X и II. Прилагането им в средни дози осигурява на половината от пациентите с инхибиторна хемофилия да спрат кръвотечението. Въпреки това, тромбогенността на тези лекарства, тяхната способност да провокират развитието на DIC и тромбозата, особено при едновременното приложение на аминокапронова киселина и други хемостатици, е известна. Такива разстройства могат също да се развият по време на байпас лечение на инхибиторна форма на хемофилия. Така например са описани случаи на инфаркт на миокарда при млади пациенти с хемофилия при многократна употреба на концентрационните фактори на протромбиновия комплекс. Според редица автори, в случай на инхибиторна хемофилия, не обикновени, но така наречените активирани препарати от комплекс на протромбин или фактор IX са по-ефективни. Те обаче са 10 или повече пъти по-скъпи от неактивираните концентрати на същите тези фактори. За да се намали рискът от развитие на DIC и тромбоза, се препоръчва въвеждането на тези фактори с антитромбин III или с предварително дълбоко замразена плазма заедно с малки дози на свиване.
Данните за ефекта на преднизолон върху количеството антитела в кръвта са противоречиви, но повечето автори все още отбелязват, че такова лечение рядко е ефективно при пациенти с хемофилия. Имуносупресорите (азатиоприн и други) често намаляват количеството антитела, но употребата им е опасна поради развитието на тромбоцитопения, която при хемофилия може значително да влоши хеморагичните феномени.
Ако пациентите с инхибиторна форма на хемофилия нямат положителна динамика, тогава по време на заместваща терапия, преди хирургични интервенции, винаги е необходимо внимателно да се провери дали посоченият инхибитор е налице в плазмата.
При екзацербация на вторичен ревматоиден синдром, както и по време на курсове за интензивна заместителна терапия, особено ако той не отслабва, но увеличава болката в ставите, преднизонът дава добър ефект (20-40 mg на ден за един месец с последващо постепенно намаляване на дозата до минимум).
Изключително важно за предотвратяването на кървенето е да се сведе до минимум рискът от наранявания, разфасовки и т.н. от ранна детска възраст. Изключването от употреба на играчките (включително метал и пластмаса), както и нестабилните и тежки предмети е лесно. Мебелите трябва да са със заоблени ръбове, изпъкнали ръбове, обвити с памук или каучук от пяна, подът покрит с килим. Комуникацията и играенето на пациенти с момичета, а не момчета, е за предпочитане.
За пациента е важно правилният избор на професия и място на работа. В най-тежките случаи единственият ефективен метод за облекчаване на заболяването е системното, веднъж на всеки 10 дни, интравенозно приложение на криопреципитат или друг концентрат на фактор VIII, който е наличен. Единична доза от лекарството за такава превенция е 400-800 IU.
От голямо значение за предотвратяването на тежки увреждания на опорно-двигателния апарат е възможно най-ранното приложение на препарати от фактор VІІІ за натъртвания и други наранявания, както и за проявяване на остра ставна болка, което предполага, че е започнало изтичане на кръв. Непосредственото въвеждане на концентрации на антихемофилни фактори (специален екип за спешна помощ или хемофилен център или обучени родители на пациента) отпада от самото начало на формиране или обостряне на кръвоизливи, предотвратява разрушителните промени в ставата. Спешната първа помощ е основен елемент от физическата рехабилитация на пациентите и предотвратяването на тежки и необратими промени в ставите, костите и мускулите. Драстично намалява броя на хоспитализациите, средната годишна продължителност на престоя в болницата, не откъсва децата от училище.
С интензификацията на заместващата трансфузионна терапия броят на хората, заразени със серумен хепатит, се увеличава, тежките реакции към въвеждането на хеморагии се увеличават и възникват редица други имунни заболявания.
Генната профилактика на хемофилия все още не е развита. Определянето на пола чрез изследване на секс хроматина и кариотипа на амниотични клетки, получено чрез метода на амниоцентезата, дава възможност за своевременно прекъсване на бременността, но не показва дали фетусът е носител на хемофилен ген. Бременността се запазва, ако плодът е мъж, тъй като всички синове на пациентите се раждат здрави и прекъснати, ако плодът е женски, тъй като всички дъщери на пациенти с хемофилия са носители на болестта.
Жените - носители на хемофилия, с вероятност за раждане на пациента с 50% (ако плода е от мъжки пол) или Платците на хемофилия (ако има женски ембрион), раждането на момичета носи само риска от семейството на хемофилици с първото поколение на втория, и в същото времето се увеличава общия брой носители на заболяването.
Министерството на здравеопазването на Руската федерация одобри лекарството Revolide (Eltrombopag) за употреба при деца. Ново лекарство се показва на пациенти, страдащи от хронична имунна тромбоцитопения (идиопатична тромбоцитопенична пурпура, ITP), рядко заболяване на кръвната система.
03.03.2017
Канадски учени от университета в Отава възнамеряват да направят революция в реставрационната медицина. В един от последните експерименти, те успяха да развият човешко ухо от обикновена ябълка.
27.02.2017
Специалисти от Първия медицински университет "Павлов" в Санкт Петербург създават наночастици, с помощта на които е възможно да се диагностицират състоянията на инфаркт и префарциране на пациента. Също така в перспективата на научните изследвания, наночастиците ще бъдат използвани ...
Медицински изделия
Почти 5% от всички злокачествени тумори са саркоми. Те се отличават с висока агресивност, бързо разпространение по хематогенния път и склонност към релапс след лечение. Някои саркоми се развиват през годините, без да показват нищо ...
Вирусите не само се задържат във въздуха, но също така могат да паднат върху перилата, седалките и други повърхности, като същевременно поддържат своята дейност. Следователно, на пътувания или на обществени места е желателно не само да се изключи комуникацията с други хора, но и да се избягва ...
За да върнете доброто виждане и да кажете сбогом на очилата и контактните лещи завинаги е мечтата на много хора. Сега тя може да стане реалност бързо и безопасно. Новите характеристики на корекцията на лазерното виждане отваря напълно безконтактната техника Femto-LASIK.
Козметичните продукти, предназначени да се грижат за кожата и косата ни, всъщност не са толкова безопасни, колкото мислим.
Комплексът от механизми, поддържащи кръвта в течно състояние, без коагулация в кухината на съда или инфилтрация през съдовата стена, се нарича хемостаза. Тъй като патологичните състояния, свързани с кръвосъсирването, се разглеждат в следващата лекция, трябва да се обмислят и други промени, свързани с нарушена хемостаза.
Кървене (кръвоизлив от гръцката Haima -. Кръв и реин - поток) се нарича кръвта в съдовата леглото или сърцето на околната среда (външна кървене) или в телесни кухини, кухи органи лумен (вътрешно кървене). Примери за външно кървене са метрорагия (матката), мелена (чревни) и вътрешна - hemopericardium, хемоторакс, hemoperitoneum и hemarthrosis (в перикардната кухина, плеврата, коремна или съвместно съответно).
В зависимост от източника на кървене се разделя на артериална, венозна, артериална-венозен (смесен), капилярна, паренхимната (капилярен на паренхимните органи) и сърце.
Особено вид кръвоизлив е кървене в които кръвта extravascularly акумулира в тъканите. Има четири типа:
Хематом - хеморагия с нарушена цялост тъкан и се образува кухина;
Хеморагичен импрегниране (инфилтрация) - кръвоизлив запазване интактна тъкан;
Екхимози (синини) - кървене в кожата на равнинна, подкожна тъкан, лигавиците;
Петехии - установят кръвоизливи по кожата, лигавиците и серозни мембрани, вътрешните органи.
Множество малки червени петна от кръвоизливи, сливащ се заедно в по-голям размер, наречени хеморагична пурпура и синини до 2 см в диаметър - екхимоза.
Механизми на кървене или кръвоизлив включват:
Разликата (haemorragia на rhexin), произтичащи от увреждане или некроза немодифициран съд (сърдечна руптура на инфаркт на миокарда), възпаление (сифилитичен mezaortit с разкъсване на аортата), засегнатата съдова аневризма;
Корозия (haemorragia на diabrosin), или arrosive кървене, което се развива в разрушаването на възпалението на съдовата стена (по-гноен), злокачествен тумор, некроза (случаен некроза кървене туберкулозен кухина), излагане на химикали (стомашен сок може да доведе до кървене от стомашни язви), покълване хорионбиопсията съдова фалопиевите тръби с извънматочна бременност;
Диапедеза (haemorragia на diapedesin от гръцката диаметър -. Чрез, pedao - скокове), при което на изхода на кръв чрез увеличаване на съдовата пропускливост, обикновено непокътнати малки кръвоносни съдове в тежка хипоксия, интоксикация, инфекция, различни коагулопатии, хеморагичен диатеза. Сравнително често diapedetic кръвоизлив разработен за хипертонична криза, системни васкулити, левкемия, хемофилия, уремия.
Склонност към спонтанно кървене или кръвоизлив в отговор на дори малки щети е наречен хеморагичен диатеза. Това състояние е свързано с качествено или количествено тромбоцитите променя недостатъчно коагулация, патологична нестабилност или повишен съдов пермеабилитет както наследствени и придобити.
Основните причини за кървене (кръвоизлив) са:
1. Подобрен съдова чупливост наблюдава при своите вродени дефекти, инфекции и интоксикации, хипо- и бери-бери, стероидна терапия;
2. Дефекти на тромбоцитите. Те включват тромбоцитопения от всякакъв произход, наследствено или придобито отслабване адхезия (болест на фон Вилебранд, Bernard-Soulier, наследствена хеморагична диатеза и т.н.), отслабена от агрегацията на тромбоцитите или намаляване на секрецията;
3. вроден дефицит на коагулационни фактори (хемофилия А за фактор VIII, хемофилия В от Фактор IX, болест на фон Вилебранд, други фактори на кръвосъсирването) или повече придобита произход (чернодробни заболявания, дефицит на витамин К, някои имунни заболявания);
4. Излишък интравазална коагулация, като дисеминирана интравазална коагулация - (. Видите следната лекция) DIC.
Изход кръвоизливи може да е изгодно (резорбция проникнала извън кръв, организация, капсулиране, образование "ръждясали" кисти) и неблагоприятната (инфекция присъединяване нагнояване).
Стойността на кървенето се дължи на неговия вид, тежест и продължителност. Например, инфаркт на инфаркт на миокарда с hemopericardium за образуване на бързо води до смърт на пациента, въпреки че общият брой на поточно кръв е обикновено не повече от 100-200, с артериална кървенето може да се развие масивна загуба на кръв и остра анемия с фатални последици. Продължителен леко кървене от хронична язва на стомаха или дванадесетопръстника причинява хроничен хеморагичен анемия. Значение кръвоизлив зависи преди всичко от неговата локализация, и то само на неговия размер. Дори и малък кръвоизлив в мозъка може да доведе до загуба на жизнено важни центрове, мозъчен оток и смърт на пациента, докато дори и без усложнения масивен кръвоизлив в подкожната тъкан не представлява риск за живота.
Плазморагията е излизане от лумена на съда с кръвна плазма с импрегниране на околните тъкани (плазмено накисване), дължащо се на повишена съдова пропускливост. Plasmorrhages настъпва трансендотелиална поради ултрафилтрация (плазма добив през порите на базалната мембрана на ендотела чрез увеличаване на хидростатично или осмотично налягане), дифузия (причинена от градиент на плазмени компоненти в лумена и от съда), microvesicular транспорт (mikropinotsitoz или tsitopemzis срещащи се дължи на активността на системите за ензим ендотелни) , Възможно е също така и освобождаване на вътрешно-ендотелиална плазма. По този начин плазморагията се определя от увреждане на васкуларната стена (главно нейната интима) и промяната в кръвните константи. Морфологичен проучване микроваскуларни стена сгъсти, става хомогенна, а електрон микроскопско изследване на набъбналите ендотелните клетки имат голям брой микровезикули, fenestrae и образуване тунел, появата на междуклетъчните пропуски, разхлабване на интимата мазе мембрана. Натрупването на плазмени компоненти води до увреждане на клетките и междуклетъчното вещество в съдовата стена и периваскуларните тъкани, в края на което се развива хиалиноза, а в тежки случаи - фибриноидна некроза.
Шокът е тежко патологично състояние, характеризиращо се с циркулаторен колапс (остра циркулационна недостатъчност) след суперструйно излагане на хемостаза. Представени са хиповолемични, сърдечни, септични и съдови видове шок.
Хиповолемичен шок се причинява от бързо намаляване на обема на циркулиращата кръв с 20% или повече, което се отбелязва при остра загуба на кръв и дехидратация. По този начин загубата на течности и електролити е възможна при продължителни изгаряния (поради освобождаването на плазма от увредена микроваскулатура), с тежко повръщане, обилна диария.
Сърдечният удар развива в отговор на намаляване на обема на инсулт при поражение на сърцето се наблюдава при инфаркт на миокарда, тежка миокардит, остра митрална или аортна регургитация, протезна клапа тромбоза, разкъсване на интервентрикуларната преграда, hemotamponade сърцето риза. Очевидният спад на кръвното налягане води до значително намаляване на кръвоснабдяването на тъканите, подобно на хиповомичните промени.
Септичен (токсичен-инфекциозен) шок се случва в присъствието на инфекция, причинена от грам-отрицателни (Е. коли, Proteus, Klebsiella, и т.н.) по-малко Грам-положителни (staphylo-, стрептококи, пневмококи) микрофлора. Секретирани токсини (главно ендотоксин) Активиране на системата на комплемента, коагулация, фибринолиза, както и тромбоцитите и неутрофилите. В резултат на това стимулира образуването на азотен оксид (силен вазодилататор), тумор некрозис фактор, интерлевкин причинява остра циркулаторна недостатъчност.
Съдова (преразпределение) може да бъде неврогенен шок (травматична, болка, увреждане на гръбначния мозък като усложнение от анестезия) или анафилактичен индуцирани общи реакции на свръхчувствителност. Поради изразена вазодилатация, повишена пропускливост на капилярите и артериовенозна нулиране преразпределение обем интраваскуларна кръв, придружено от значително намаляване на общото периферно съдово съпротивление.
Шокът в развитието му преминава през три етапа:
1. непрогресиращо (рано) етап на удар се характеризира с понижаване на кръвното налягане и сърдечна обем продукция, като се поддържа относително нормално кръвоснабдяване на жизненоважни органи. Това се дължи на компенсаторни вазоконстрикция на кръвоносните съдове, особено на кожата и червата. С изчерпването на адаптивните механизми шокът преминава в следващия етап;
2. прогресивни различни етап шок клинични симптоми, дълбоко колапс, причинени от намалена кръв пълнене всички органи и тъкани (тъкан хипоперфузионни поради увеличаване артериална дилатация Keying), развитието на метаболитни и заболявания на кръвообращението. 3. необратимо етап шок има ясно изразена липса на кръвообращението на нивото на микроваскулатурата в нарушение на целостта на съдовата стена, бързо нараства мултиорганна недостатъчност, завършва със смърт на пациента.
Морфологичното изследване показва генерализирани дистрофични и некротични промени, явления на синдрома на DIC (петехиални кръвоизливи, стазис, тромби в микроваскулатурата). Освен това, поради особеностите на структурата и функционирането на различните органи във всяка една от тях, възникват особени промени - шокови органи. По този начин, развитието на некротична нефроза (некроза на епитела с туморни тръби) е характерно за шоков бъбрек. Шокиращият белодроб се проявява чрез огнища на ателектаза, серозен хеморагичен едем, понякога със загуба на фибринови влакна (хиалин мембрани). Исхемичната енцефалопатия се появява в мозъка, която се проявява чрез оток, точкови кръвоизливи и огнища на некроза. В сърцето се наблюдават малки, най-вече субендокардиални огнища на кръвоизлив и миокардна некроза, мастна дистрофия на кардиомиоцити със симптоми на тяхното отдръпване. В кортикалния слой на надбъбречните жлези се наблюдава намаляване до пълното изчезване на липидите, използвани за синтеза на стероидни хормони. В стомашно-чревния тракт се откриват кръвоизливи, ерозии и остри язви в лигавицата. Шокиращият черен дроб се отличава от мастната дистрофия на хепатоцитите и в някои случаи дори от тяхната центролобуларна некроза.
Прогнозата на шока зависи от вида, тежестта, стадия на започване на лечението, наличието на усложнения. Понастоящем при тежък кардиогенен или септичен шок смъртността достига 50% или повече.
Ключови понятия за нарушена хемостаза:
1. Хемостатични нарушения, коагулопатия (коагулопатия, коагуло- гръцки патос - страдание, заболяване) - нарушена функция на системите за коагулация и антикоагулация на кръвта.
2. Хиперкоагулиращо тромботично състояние- състояние, придружено от патологичен процес на повишено кръвно съсирване, дължащо се на повишена тромбоцитна агрегация, активиране на плазмени и тъканни коагулационни фактори с образуване на тромбоцитни и фибринови съсиреци.
3. Хипокоагулиращо хеморагично състояние- състояние, придружено от патологичен процес за намаляване на съсирването на кръвта, дължащо се на понижаване на тромбоцитната агрегация, инактивиране на коагулационните фактори на плазмата и тъканите с появата на кървене и кървене.
4. DIC (тромботично хеморагично състояние) - дисеминирана интраваскуларна коагулация на кръвта - типичен патологичен процес хемостатични нарушения, произтичащи от последователно срещащи съсирване реакции хиперкоагулация (образуване на кръвни съсиреци разпространени в микроциркулацията васкулатура) и антикоагуланти (изчерпване тромбогенни фактори и подобряване на фибринолизата), придружен от масивно кървене, тежка кръвосъсирване шок и остра дистрофия на вътрешните органи.
При кои заболявания има нарушение на хемостазата:
Хемостаза - сложен процес, който предотвратява или спира притока на кръв от лумена, предвижда появата на фибрин пакет, необходим за възстановяване на целостта на тъканите, както и най-накрая премахва фибрин, когато нуждата от нея изчезва. Четири основни физиологични механизма са включени в този процес.
Използване на кръв хемостатично система изпълнява своята важна функция - поддържане течно състояние на кръвта, протичащ в кръвоносните съдове, и кръвосъсирването от счупване на съдовата стена и по този начин, спиране на кървенето и поддържане на кръвен обем и състав. Системата на хемостазата е многокомпонентна. Тя включва тромбоцити и други кръвни клетки, съдова стена екстраваскуларно тъкан, биологично активни вещества (тромбоцит-съдова хемостаза), плазма, тъкан коагулационни фактори (коагулация хемостаза), разположени тясно с антикоагулант, фибринолитична и каликреин-кинин системи. Нарушението на някое от тези компоненти води до патологично хемостаза.
Класификация на нарушенията на хемостазата. Патология хемостаза е класифицирана от първична лезия на различните компоненти в тромбоцитите-съдови разстройства на хемостаза и коагулация хемостаза. Според етиологията на тези заболявания могат да бъдат придобити и наследствено, и от посоката на промени разделени на понижаване на съсирването на кръвта (hypocoagulation) и повишено съсирване на кръвта (хиперкоагулация), който може да бъде местен (тромбоза) и генерализирано (DIC).
Намаляване на коагулацията на кръвта
Намаляването на кръвосъсирването изглежда прекомерно кървене (хеморагичен синдром) - rebleeding, кръвоизлив осъществява както спонтанно и с леки наранявания.
Тромбоцитите-съдови хемостаза е нарушена в количествени и качествени промени на тромбоцитите (тромбоцитопения и thrombocytopathy) и лезии на съдовата стена.
Тромбоцитопенията се нарича намаляване на броя на тромбоцитите в кръвта под нормата (180-320 G / l или 180-320x109 / l). Въпреки това, спонтанното кървене се случва само когато броят им спадне под 30 g / l. При тромбоцитопатията се разбира качеството на малоценност и дисфункция на тромбоцитите с нормално или намалено съдържание.
Причини за ниска коагулация на кръвта. Причината за тромбоцитопения имунни отговори често се променят антигенна структура на тромбоцитите под действието на вируси, лекарства, антитромбоцитни антитела форма (с хронична лимфоцитна левкемия, идиопатична тромбоцитопения), тромбоцитите несъвместимост между майката и фетални антигени. В допълнение, разработване тромбоцитопения се дължи на заболявания на костния мозък МЕГАКАРИОЦИТИ йонизиращи лъчения, химически или изместват си туморни метастази, левкемични инфилтрати. Намалена thrombocytopoiesis могат да бъдат причинени от недостиг на фолиева киселина и цианокобаламин, наследствен дефект на тромбоцитите формация (включително при дефицит trombotsitopoetinov). Тромбоцитопенията се проявява в резултат на механично увреждане на тромбоцитите със спленомегалия, изкуствени сърдечни клапи, както и повишена консумация на тромбоцити с локална и генерализирана вътресъдова коагулация на кръвта.
Етиологичните фактори, които причиняват тромбоцитопатия, включват действието на токсични вещества и лекарства (алкохол, ацетилсалицилова киселина), йонизиращо лъчение, ендогенни метаболити (с уремия, чернодробна цироза); дефицит на цианокобаламин, хормонални разстройства (хипотиреоидизъм). Наблюдаваните генетични дефекти мембранна структура и биохимичен състав на тромбоцитите (trombostenina дефицит, фактор 3, АТР, ADP, G-6-PDG, мембранни рецептори за фактори, V, VIII, XI и др.).
При хеморагичен vazopatiyah лезия на съдовата стена, което води до разрушаване на тромбоцитите-съдови хемостаза и кървене, се дължи на повишена проницаемост на стената на кръвоносен съд и неговото разграждане в нарушение на синтеза на колаген (за хранителен дефицит аскорбинова киселина, наследствени дефекти в синтеза на колаген) чрез действието на биологично активни вещества ( алергия), радиотоксини (радиационна болест), имунен хеморагичен васкулит, намаляване на ангиотрофната функция на тромбоцитите по време на тромбоцитите Отваряне и thrombocytopathy, унищожаване на левкемична инфилтрация на съдовата стена. Една от причините за кървенето е намаляването на производството на ендотелиална васкуларна стена на фактор von Willebrand - голям молекулен компонент на кръвта на коагулационния фактор VIII (наследствена болест на фон Вилебранд). Този фактор се натрупва в тромбоцитите и се освобождава, когато те се дегранулират.
Необходимо е за нормална адхезия на тромбоцитите към колагенната стена и без него не се образува тромбом на тромбоцитите. хеморагичен синдром наблюдава по време на амплификация пероксидация на мембранните фосфолипиди, в резултат на ендотела се синтезира и секретира излишък мощни инхибитори на тромбоцитната агрегация - простациклин. В допълнение, нарушеното неврогенно и хуморално регулиране на васкуларния тонус води до намаляване на кръвоносната съдова хемостаза, което води до невъзможност за блокиране на малките съдове с тромбоцитен тромб.
Патогенеза с ниска коагулация на кръвта. Има четири основни механизма на тромбоцитопения: намаляване на производството, увеличаване на разрушаването, повишено потребление (тромбоза), преразпределение на тромбоцитите.
Прекъсване на хемостазата и развитие на кървене по време на тромбоцитопения поради следните механизми:
- повишаване на микроваскуларната пропускливост на еритроцитите и другите кръвни съставки (диапедемичен кръвоизлив) и васкуларната чупливост, дължаща се на дистрофия на стената, когато функцията на ангиотрофния тромбоцит е изключена;
- намаляване на функцията на лепило-агрегация на тромбоцитите;
- реакция освобождаване нарушение на тромбоцитите на кръвта фактор на кръвосъсирването, ADP, серотонин, адреналин, antigeparinovogo фактор, което води до недостатъчно образуване на образуването на тромбоцити тромби, не съдов спазъм и забавяне коагулация;
- намаляване на придърпването на съсиреци в резултат на намаляване на активността на контрактилния протеин на тромбоцитите - тромбостенин (тромбоцитен фактор 8).
При патогенезата на тромбоцитопатията могат да се разграничат два основни механизма на тяхното появяване: производството на патологични тромбоцити в костния мозък и унищожаването на тромбоцитите във всички части на кръвната система. Патогенезата на тромбоцито-васкуларната хемостаза с тромбоцитопатия е същата като при тромбоцитопения, тъй като тя се свързва с дезактивирането на тромбоцитните функции.
Нарушаването на хемостазата на коагулацията, което води до развитие на кървене, може да бъде причинено от следните фактори:
- Придобито и наследствено намаляване или изкривяване на синтеза на плазмени и тромбоцитни коагулационни фактори и компоненти на системата каликреин-кинин;
- инхибиране или повишено потребление на тези фактори;
- повишаване на ендогенните антикоагуланти;
- активиране на фибринолитичната система;
- Предозиране на антикоагуланти, фибринолитични и дефибриниращи лекарства. Всичко това е в основата на нарушението на една от трите фази на коагулация на кръвта и отдръпване на съсирек или тяхната комбинирана промяна.
Предизвиква нарушение на първата фаза на кръвосъсирването - образуване на тромбопластин - е продукти за намаляване на фактори (IX, X) в патологията на черния дроб, образуването на антитела към някои фактори (VIII, IX) при заболявания, патогенезата на която има автоимунен компонент (левкемия, колаген) или предозирането на такъв универсален антикоагулант като хепарин. Има генетични дефекти в синтеза на фактори VIII, IX и XI, чийто дефицит е в основата на развитието на хемофилия (съответно, последователността на тези фактори е хемофилия А, В и С).
Нарушаването на втората фаза на кръвосъсирването - тромбин - настъпва не само за чернодробни заболявания, но също така и в хипо- и бери-бери К при понижено също синтез в черния дроб на фактори II, V, VII, включени в тази фаза (с обструктивна жълтеница, ентерит, богат резекция на тънките черва, медицинска дисбактериоза). Появата на инхибитори на имунната фактори V, VII (например, при лечението на стрептомицин сулфат), повишена им бъбречна екскреция, наследствена недостатъчност (Фактор V когато paragemofilii) или компоненти антикоагулация система инактивиране - антитромбин, хепарин (с анафилактичен шок, предозиране хепарин).
Хеморагичен диатеза свързан с трета фаза нарушена коагулация - фазата на образуване на фибрин случва с намаляване на синтез фибриноген в заразената чернодробна патологичен процес, светлина или в резултат на наследствен хипо-, afibrinogenemia и дефицит fibrinstabiliziruyuschego фактор (фактор XIII). По-често обаче, нарушението на третата фаза е следствие от увеличена фибринолиза в случай на нараняване (операция) на белите дробове, матката, панкреаса; изгаря, шок. Това се дължи на повишено кръвно въвеждане на плазминогенен активатор (плазминоген) - тъкан, микробен fibrinokinaz, левко- и еритроцитни активатори, компоненти на каликреин-кинин система и комплекси допълнение система хепарин с фибриноген, плазминоген и адреналин (тези комплекси предоставят неензимно фибринолиза от В. . Кудряшов).
Патогенеза. Основната връзката в патогенезата на хеморагичен диатеза, който се развива в нарушение на всяка от фазите на кръвосъсирването, е хронична загуба на кръв и нейните последици, както и структурни и функционални промени в мястото на кръвоизлив (в ставите, вътрешните органи, кожата и други тъкани).
Повишена коагулация на кръвта
Увеличаването на коагулацията на кръвта се проявява чрез локална (тромбоза) или генерализирана вътресъдова кръвосъсирване, която се основава на нарушение на тромбоцитната съдова и коагулационна хемостаза.
Хиперкоагулацията може да се дължи на:
- повишаване на функционалната активност на системата за коагулация на кръвта вследствие на повишен прием на прокоагуланти и активатори на кръвосъсирването в кръвта;
- повишаване на съдържанието на тромбоцити;
- намаляване на антитромботичните свойства на съдовата стена;
- намаляване на активността на кръвната антикоагулантна система;
- отслабване на фибринолизата.
Генерализирана (разпространявана) интраваскуларна коагулация (DIC) - тежко увреждане на хемостаза, което се случва, когато излишък незабавни кръвни procoagulants и активатори на коагулация, водещи до образуването на няколко микротромби в съдовете на микроваскулатурата, и след това hypocoagulation развитие, тромбоцитопения и кръвоизлив в резултат "консумация" на факторите на коагулационната система и увеличаване на функционалната активност на системата за антикоагулация и фибринолиза на кръвта, последвано от изчерпване на всички t EX системи.
Етиология. Разнообразието и неспецифичността на DIC се дължи на разнообразието от причинно-следствени фактори за неговото възникване. Те включват предимно общи инфекции и септични условия, всички видове шок, травматичен хирургия, гинекологична патология (преждевременно отделяне, ръчно преместване на плацентата), остра интраваскуларна хемолиза, уремия в бъбречна недостатъчност, всички крайни състояния.
Патогенеза. Основната връзката в патогенезата на генерализирано хиперкоагулация дисбаланс между каликреин-кинин, коагулация, антикоагулация и фибринолитичната система кръв, когато влезе в кръвния поток на голям брой прокоагулантната и активатори. Това води до нарушаване на кръвта като важна функция като запазване на нормалното си състояние на агрегиране, в резултат на фаза хиперкоагулация на кръвни съсиреци в кръвоносните съдове и спира разпространението му с развитието на тежки дегенеративни и функционални нарушения на органи и тъкани, често са несъвместими с живота. В следващата фаза на хипокоагулация, изтъняването на кръвта и загубата на способност за съсирване и агрегиране на тромбоцитите предизвикват кървене, което е слабо податливо на терапевтична корекция. При благоприятния изход третият идва - фазата на възстановяване, при което хемостазата се нормализира.
 Английска азбука с транскрипция
Английска азбука с транскрипция Изборът на най-добрата микс за слаби и недоносени бебета
Изборът на най-добрата микс за слаби и недоносени бебета Астрономическите данни на Сатурн
Астрономическите данни на Сатурн