Kršenje hemostaze. Povećana sposobnost krvi za stvaranje ugrušaka u krvnim žilama. Ca ion antagonisti
Sustav hemostaze izvanredno je dostignuće evolucije, koja neprekidno održava ravnotežu između dva višesmjerna procesa: najbrže stvaranje ugruška (tromba) kako bi se spriječio gubitak krvi kao odgovor na oštećenje žila uz održavanje tekućeg stanja nakupljanja krvi u cirkulaciji. Rješenje ovog teškog problema pružaju složene interakcije vaskularnog endotela, kaskada koagulacije plazme, antikoagulacijski mehanizmi, fibrinolitički sustav, trombociti i leukociti. Reološke karakteristike kretanja krvi kroz žile različitog promjera, posebno viskoznost u sustavu mikrocirkulacije, od velike su važnosti.
U medicini kritičnih stanja često se razvijaju poremećaji hemostaze, stupanj njihove ozbiljnosti ovisi o deregulirajućem učinku na homeostazu štetnih čimbenika - traume, infekcije, operacije, lijekova, kao i o kompenzacijskim sposobnostima kardiovaskularnog i dišnog sustava. Dešifriranje vodeće uloge poremećaja hemostaze, posebno diseminirane intravaskularne koagulacije (DIC), u patogenezi najkritičnijih stanja koja zahtijevaju intenzivnu njegu, i pojavljivanje u liječnikovom arsenalu učinkovitih ciljanih lijekova za njezinu korekciju su odlika obilježja suvremene medicinske prakse.
Klinički se poremećaji hemostaze češće manifestiraju krvarenjem, rjeđe trombozom, ali često postoji istodobna manifestacija patoloških krvarenja i mikrotrombija.
Fiziologija normalne hemostaze
Oštećenje stijenke krvne žile uzrokuje trenutno vazokonstrikciju i same oštećene žile i susjednih kapilara i arteriola, što dovodi do početnog usporavanja protoka krvi u zoni oštećenja. Nadalje, interakcija nekoliko funkcionalnih komponenata dovodi do stvaranja primarnog trombocitnog čepa (ugruška) koji se brzo stabilizira fibrinskim filamentima. U normalnim uvjetima, ovaj postupak prokomagulacije ograničen je vremenom i mjestom, a nadziraju ga iste funkcionalne komponente. To uključuje trombocite, kaskadu koagulacije plazme, prirodne antikoagulanse, sustav fibrinolize i endotelne stanice.
Kada dođe do oštećenja endotela, trombociti dođu u kontakt sa sundendotelnim slojem kolagena, trombociti se lijepe (priliježu) na kolagen, formiraju se granule trombocita s oslobađanjem serotonina, lizosomalnih enzima, fibrinogena i IV faktora trombocita i stimulira se sinteza. Aktivirani trombociti se agregiraju i formiraju primarni trombocitni čep (primarna hemostaza). Kvantitativne i kvalitativne patološke promjene trombocita očituju se krvarenjem i krvarenjem. Vrijeme krvarenja je optimalni screening test za procjenu funkcionalne održivosti trombocita.
Kaskada koagulacije odgovorna je za stvaranje stabilnog fibrinskog tromba. Čimbenici koji čine to su navedeni u tablici. 2-10.
Tablica 2-10. Faktori koagulacije Faktor 1 Fibrinogenski faktor II Protrombinski faktor III Tkivo tromboplastin (tkivni faktor) Faktor IV Kalcijev faktor V Acelerin Faktor VII Prokonvertin Faktor VIII Antihemofilični faktor IX Božićni faktor Faktor X Faktor Stuart Faktor XI Faktor prekida plazme Kromplastistin Kromatlastik faktor
Sinteza većine faktora koagulacije događa se u jetri. Faktor VIII, osim jetre, djelomično sintetizira i megakariociti i endotelne stanice. Čimbenici II, VII, IX i X vitamina K ovisni su, tj. Za njihovu sintezu hepatocitima potreban je vitamin K, a shema kaskade koagulacije koagulacije prikazana je na Sl. 2-8.
Početak kaskade koagulacije je interakcija faktora VII s faktorom tkiva (III) u zoni oštećenja (vanjski put zgrušavanja). Nastali kompleks aktiviranog faktora VII s faktorom tkiva aktivira faktore IX i X, što dovodi do stvaranja trombina. Trombin pretvara fibrinogen u fibrin aktiviranjem faktora XIII i trombocita. Djelovanje trombina kontrolira prirodni protein koji se aktivira antikoagulansom C. Alternativa vanjskom putu koagulacije je ona unutarnja, počevši od aktiviranja faktora XII kolagenom zbog kontakta krvi s stranom površinom. Faktor XNA aktivira faktor X1a, tada su vanjski i unutarnji putevi koagulacije identični.
Unutarnji put vanjski put
(kontaktni faktor) (oštećenje tkiva)
RSH
PXA
Rua
RHSha
RHSH
Sl. 2-8. Šema kaskade koagulacije.
Screening testovi - protrombinsko vrijeme, aktivirano parcijalno tromboplastinsko vrijeme (APTT) i trombinsko vrijeme - omogućuju nam prosudbu stanja jedinica koagulacijske hemostaze. Kongenitalne ili stečene oštećenja kaskade koagulacije uzrokuju krvarenja u mozgu, zglobovima, mekim tkivima i mišićima i krvarenje u probavnom sustavu.
Prirodni antikoagulansi predstavljeni su s dva glavna faktora - antitrombinom III i vitaminima ovisnim o vitaminu K i 5. Antitrombin III inhibira trombin i faktor Xa, sudjeluje u inaktivaciji faktora 1Xa, X1a, XIA. U interakciji s heparinom, antitrombin III značajno pojačava njegov antikoagulantni učinak. Aktivirani protein C u kombinaciji s proteinom 5 ima antikoagulantni učinak na enzime koji inhibiraju Wa i Usha faktore (važni kofaktori procesa prokoagulanse). Uz to, protein C pojačava fibrinolizu inhibiranjem tkivnog aktivatora plazminogena, olakšavajući prelazak plazminogena u plazmin. Protein C igra važnu ulogu u patogenezi
DIC sindrom. Manjak antitrombina III, proteina C i proteina 5 (češće stečenih nego kongenitalni) popraćen je velikom učestalošću trombotskih komplikacija.
Fibrinoliza (poput koagulacije) je normalan odgovor na oštećenje vaskularne stijenke. Tkivni plazminogeni aktivator (1-RA), koji nastaju od endotelnih stanica kao odgovor na njihovo oštećenje ili stimulaciju trombinom, pretvara plazminogen u plazmin. Plazmin uništava fibrin i fibrinogen, tvoreći različite produkte razgradnje fibrina. Istodobno, inhibitor aktivatora plazminogena (PA1-1, formiran od hepatocita i endotelnih stanica i PA1-2, formiran u placenti i makrofazima) cirkulira u neaktivnom obliku u plazmi. Njihov fiziološki značaj leži u kontroli fibrinolize i sprječavanju njezina prelaska u patološki stadij. Terapeutski inhibitori fibrinolize su traneksamska kiselina i aminokapronska kiselina. Suprotno tome, streptokinaza je fibrinolitički lijek koji povećava stvaranje plazmina.
U normalnim uvjetima, endotelne stanice odgovorne su za antitrombotsku interakciju između krvi i tkiva, održavajući tekuće stanje u krvi. Proizvode antikoagulanse poput glikozaminoglikana, heparin sulfata, trombomodulina (aktiviraju antitrombin III i protein C), dušičnog oksida i prostaglandina (inhibiraju agregaciju trombocita i potiču vazodilataciju), aktivatora plazminogena u tkivu, pokretajući fibrinolizu. Ali endotelne stanice sposobne su stvoriti von Willebrandov faktor i tkivni faktor, koji pokreću kaskadu koagulacije, kao odgovor na stimulaciju bakterijskim endotoksinima. Ova svojstva moraju se uzeti u obzir prilikom provođenja terapije za hemostatske poremećaje.
Laboratorijski pregled na poremećaje hemostaze
Testovi za procjenu primarne hemostaze, koji se hitno izvode u uvjetima intenzivne njege, određuju vrijeme krvarenja i broj trombocita. Skupljanje i adhezija trombocita, sadržaj von Willebrand faktora istražuju se u specijaliziranim laboratorijima za koagulologiju.
Proces koagulacijske hemostaze može se procijeniti testovima kao što su APTT, protrombinsko vrijeme i trombinsko vrijeme, koji daju sažetu procjenu nekih faktora koagulacije. Odvojeno određivanje faktora koagulacije moguće je samo u specijaliziranim laboratorijima.
Screening antikoagulacijski sustav može se provesti određivanjem koncentracije antitrombina III; ostali testovi inhibicije koagulacije traju dugo, provode se u specijaliziranom laboratoriju.
O stanju fibrinolitičkog sustava može se prosuditi ispitivanjem količine produkata razgradnje fibrinogena, fibrinskih monomera, B-dimera, kao i korištenjem posebnih studija sadržaja aktivatora i inhibitora fibrinolize u plazmi.
Normalne vrijednosti pokazatelja koagulacije date su u tablici. 2-11.
Tablica 2-11. Indeksi zgrušavanja krvi Norma ispitivanja Norma APTT 27,4-40,3 s Protrombinsko vrijeme 12,3-16,1 s Kontrola trombinskog vremena ± 3 s Fibrinogen 1,7-3,1 g / l P-dimera Kraj tablice. 2-11 Faktori koagulacije II, V, VII, VIII, IX, X, XI, XII 50-150% Antitrombin III 80-120% Aktivirani protein C 73-121% Protein 3: ukupno 55-125% besplatno 21-53% Von Willebrand faktor (antigen) 50-150%
Vrijeme krvarenja odgovara vremenu potrebnom za stvaranje trombocita. Može se produljiti trombocitopenijom, disfunkcijom trombocita i von Willebrandovom bolešću, ali nikad se ne produžuje s koagulološkim poremećajima (na primjer, hemofilijom).
Broj trombocita treba biti uključen u obvezni laboratorijski pregled pacijenata u jedinicama intenzivne njege. Treba imati na umu da se broj trombocita može smanjiti u prvim danima menstruacije.
APTT odražava ukupni sadržaj svih čimbenika unutarnjeg puta koagulacije, od aktiviranja faktora XII do stvaranja topljivog fibrina, osim faktora VII i XIII. Produljenje APTT-a odražava povećanu sklonost krvarenjima i može ukazivati na nedostatak jednog ili više čimbenika unutarnje veze hemostaze (na primjer, VIII s hemofilijom ili von Willebrandovom bolešću). Produljuje APTT terapiju natrijevim heparinom ili varfarinom. Poremećaji primarne hemostaze APTT se ne odražavaju.
Protrombinsko vrijeme karakterizira proces stvaranja ugrušaka. Određuje zbroj faktora koagulacije I, II, V, VII i X koji čine vanjski put te produljuje s nedostatkom jednog ili više njih. Ovaj se pokazatelj često koristi za kontrolu terapije neizravnim antikoagulansima (varfarin) - antagonistima vitamina K, koji u skladu s tim ne djeluju na fibrinogen i faktor V. Još je informativnije u ovu svrhu proučavanje kompleksa protrombina koji određuje samo zbroj faktora II, VII i X (za sintezu ovih faktorima potreban vitamin K). Kako bi se usporedili rezultati ispitivanja različitih laboratorija koji koriste različite ispitne sustave, pokazatelji protrombinskog vremena i protrombinskog kompleksa preračunavaju se u međunarodni normalizirani omjer (INR). U zdravih pojedinaca INR iznosi oko 1. Kad se liječi varfarinom, manjkom vitamina K, zatajenjem jetre ili izoliranim nedostatkom jednog od faktora (obično VII), INR bi trebao biti između 2 i 3.
Trombinsko vrijeme testira posljednju fazu stvaranja tromba. Njegovo produljenje može ukazivati na fibrinogenopeniju manju od 1 g / l ili na disfibrinogenemiju. Terapija natrijevim heparinom također produžuje trombinsko vrijeme.
Nizak sadržaj fibrinogena može biti posljedica smanjene proizvodnje ili povećane potrošnje. Visok sadržaj fibrinogena pokazatelj je akutnog upalnog stanja, posebno jetre, gdje dolazi do njegove sinteze. Povećanje koncentracije produkata lize fibrinogena (proizvodi degradacije fibrina, B-dimer) uz smanjenje njegove količine ukazuje na razvoj DIC-a.
Manjak antitrombina III (najmoćniji prirodni proteolitički antikoagulant u plazmi) često služi kao manifestacija akutnog masivnog gubitka krvi, neadekvatno nadoknađenog (bez transfuzije svježe smrznute plazme (FFP)) ili DIC-a povezane sa sepsom. Mnogo rjeđe, smanjenje količine antitrombina III događa se kao manifestacija nasljedne bolesti autosomno dominantne prirode. Upotreba probirnih testova za diferencijalnu dijagnozu stečenih hemoragičnih sindroma ili bolesti, čija je glavna klinička manifestacija patologija hemostatskog sustava, prikazana je u tablici. 2-12.
Tablica 2-12. Ispitivanje hemostaze kod određenih bolesti i sindroma.Hemofilijski test. Bolest
Von Willebrand akutni
dIC
sindrom bolesti
heparinska jetra
trombociti natrijevog varfarina Normalna stopa Snižena stopa Normalna stopa Normalna stopa fibrinogena Normalna stopa Snižena stopa Normalna stopa Protrombina
vrijeme Norma Norma produžena produžena norma Norma produžena APTT produljena norma ili produljena Norma ili produljena Norma ili produljena produljena trombinska vremena Norma izdužena norma ili produljena izdužena norma
Međutim, navedeni klasični testovi za praćenje hemostaze, nažalost, ne daju cjelovitu, cjelovitu sliku njegovog stanja, odražavajući interakciju brojnih čimbenika. U intenzivnoj njezi često je potrebno znati stanje pacijentovog sustava koagulacije krvi u vrijeme ispitivanja, kako u svrhu izbora lijekova ili sredstava za korekciju transfuzije, tako i zbog procjene ispravnosti terapije za ispravljanje poremećaja hemostaze. Metoda tromboelastografije omogućava vam brzo i pouzdano dobivanje podataka koji karakteriziraju i opće stanje hemostaze, kao i stanje njegovih pojedinačnih veza tijekom njihovih patoloških promjena.
Metoda tromboelastografije temelji se na mjerenju fizičkih parametara ugruška (tromba) u procesu njegovog stvaranja. Od trenutka koagulacije do kraja i kasnije lize, promjena gustoće gomile bilježi se pomoću elektromehaničkog pretvarača, koji se u modernim modelima tromboelastografa prenosi na računalni zaslon. Postoje sljedeći glavni parametri tromboelastografije (Sl. 2-9):
K (min) - vrijeme od početka koagulacije do stvaranja prvih vlakana fibrina;
K (min) - vrijeme promjene amplitude koagulacije, njenog rasta ili usporavanja;
K + K - korelira s vremenom zgrušavanja krvi, jednakim normi od 6-8 minuta;
kut a - odražava brzinu zgrušavanja krvi, proces polimerizacije fibrina;
MA (mm) - najveća amplituda krivulje, koja karakterizira snagu i krutost formiranog ugruška, koji uglavnom ovise o funkciji i broju trombocita, a u manjoj mjeri i o koncentraciji fibrina u krvi;
EPY, LUZO (%) - procjena stupnja fibrinolize.
Kao što se vidi iz smokve. 2-9, u slučaju hiperkoagulabilnog sindroma, vremenski pokazatelji KiK se skraćuju, kut a i MA povećavaju. Suprotno tome, sa statusom hipokoagulacije povećava se KiK, smanjuje se kut a i MA. Pored općih karakteristika stanja hemostaze, prema podacima tromboelastografije moguće je i prosuditi kršenja njegovih pojedinačnih veza. Dakle, s predoziranjem natrijevog heparina, svi pokazatelji tromboelastograma - K, K, a, MA - bit će izduženi i smanjeni; s trombocitopenijom, K će ostati u granicama normale, ali K će biti izdužen sa smanjenim MA; s pojačanom fibrinolizom # nenormalno, ali MA je oštro i trajno smanjeno EPY i LUZO; s trombocitopatijom i disfunkcijom trombocita
početak
Sl. 2-9. Opcije tromboelastograma: A - normalno; B - hiperkoagulacija; B - hipokoagulacija.
K izduženi, kut a i MA smanjeni. Mogućnost opetovanog izvođenja tromboelastografije, grafičko snimanje istih, minimalno vrijeme provedeno na istraživanju s vrlo malom količinom krvi koja je potrebna za njegovu primjenu, čine tromboelastograf jednim od bitnih svojstava laboratorijske opreme ekspresne laboratorije jedinica intenzivne njege.
Intenzivna terapija zasebnih oblika poremećaja sustava hemostaze
U medicini kritičnih stanja, kompletna koagulološka studija često se ne može provesti zbog ozbiljnosti pacijentovog stanja, nedostatka vremena i hitnosti kirurške intervencije. Treba napomenuti da se sumnja na krvarenje zbog sistemske hemostaze u ogromnoj većini slučajeva može isključiti ako pacijent ima hematokrit\u003e 30%, broj trombocita\u003e 100x109 / l, koncentraciju fibrinogena\u003e 1,5 g / l i, međutim, APTT i vrijeme protrombina koje ne prelazi gornje granice normalnih vrijednosti za najviše 3-5 s. S takvim pokazateljima moguće je sigurno izvesti invazivne postupke (kateterizacija punkcije središnje vene ili arterije). Istodobno, krvarenje s ovim pokazateljima može ukazivati na kiruršku lokalnu hemostazu (obično nakon operacije) ili razvoj akutnog DIC-a.
Uobičajeni su sistemski poremećaji hemostaze koji zahtijevaju intenzivnu njegu. 2-13.
Tablica 2-13. Poremećaji hemostaze u kritičnim stanjima Dijagnoza Hemostazna patologija Bolesti jetre Smanjenje svih faktora koagulacije osim VII i faktora von Willebranda Smanjivanje koncentracije proteina C i 5 Smanjenje broja trombocita i njihova disfunkcija DIC korištenjem AIK disfunkcije trombocita Smanjenje broja trombocita Smanjenje koncentracije fibrinogena Smanjenje Glumci II, V, VII, X, XI ICE sindrom TBI, sindrom sudara Povećana koncentracija proizvoda razgradnje fibrina ICE sindrom Masivna transfuzija Smanjeni sadržaj faktora V i VII ICE sindrom Warfarin Smanjeni sadržaj faktora II, VII, IX, X Smanjena koncentracija Protein C i 5 heparin natrijeva trombocitopenija Smanjeni faktor Xa trombolitik
terapija Povećanje koncentracije fibrinogena i razgradnih produkata razgradnje DIC sindrom Smanjivanje sadržaja fibrinogena Smanjenje broja fibrinogena Smanjenje broja trombocita Smanjenje proteina C i 5 Smanjenje koncentracije antitrombina III Smanjenje faktora V, VIII, IX, XI Povećanje koncentracije proizvoda razgradnje fibrina
Minimalni dovoljan sadržaj čimbenika koagulacije plazme u krvotoku, neophodan za osiguravanje hemostaze tijekom kirurških intervencija, prikazan je u tablici. 2-14.
Minimalni dovoljan sadržaj trombocita je 80-100x109 / L.
Tablica 2-14. Minimalni sadržaj faktora koagulacije potreban za kiruršku faktor hemostaze Razina hemostatike,% normalna Fibrinogen 50-100 Protrombin 40-50 Faktor V 10-30 Faktor VII 10-20 Faktor VIII 30-70 Willebrand faktor 20-50
Kraj tablice. 2-14 Faktor IX 20-60 Faktor X 10-20 Faktor XI 20-80 Faktor XIII 10
Primarni poremećaji hemostaze
Trombocitopenija (vidjeti poglavlje 9), von Willebrandova bolest i disfunkcija trombocita odnose se na hemoragičnu dijatezu uzrokovanu primarnom hemostazom. Tipični simptomi su hemoragični osipi na koži ili sluznici, pojava modrica, petehije s minimalnom izloženošću. Intenzivna terapija nužna je za lokalno krvarenje, posebno često s nosnim i menoragijama.
Najčešće se bilježi trombocitopenija zbog oštećenja koštane srži (aplastična anemija, hemoblastoze, metastaze karcinoma). Rjeđe su bolesnici s hemoragičnom trombocitopeničnom dijatezom zbog urođenih uzroka (Wiskott-Aldrich-ov sindrom, May-Hegglin-ova anomalija) ili oštećenja zračenjem, nedostatka željeza, vitamina B12 i kroničnog alkoholizma rjeđi u praksi liječnika intenzivne njege.
Idiopatska trombocitopenična purpura najčešći je oblik autoimune trombocitopenije, za koju je karakteristično da skraćuje život trombocita zbog povećane potrošnje. Funkcija trombocita ne pati. Kada se pojavi krvarenje ili radi njihove prevencije, propisani su glukokortikoidi. Primjena visokih doza intravenskog imunoglobulina je učinkovita. Često, posebno kada se pojave komplikacije glukokortikoidne terapije (Itsenko-Cushingov sindrom, hiperglikemija) ili recidiv krvarenja ili pribjegavaju splenektomiji. Na dan operacije i u neposrednom postoperativnom razdoblju nastavlja se liječenje glukokortikoidima, njegovo povlačenje treba biti postupno (smanjenje doze za 2,5-5 mg prednizolona dnevno). Transfuzije trombocita ne smatraju se sredstvom izbora, osim u izuzetno rijetkim slučajevima (neučinkovitost konzervativne terapije i potreba za sprječavanjem pojačanog krvarenja tijekom operacije).
Imuni sukob služi i kao osnova za trombocitopeniju uzrokovanu heparinom. Pacijentovo tijelo, kao odgovor na primjenu natrijevog heparina, počinje stvarati 1C protutijela, koja se vežu na Pc receptore trombocita, pridonoseći skraćenju njihovog života. Učestalost pojave takvog sukoba je
5% ljudi koji primaju natrij heparin. Trombocitopenija se razvija sporo, lokalno krvarenje je rijetko, transfuzija trombocita nije potrebna. Uz ukidanje natrijevog heparina, broj trombocita se obnavlja u roku od 2-5 dana.
Mnogi lijekovi koji se koriste u intenzivnoj njezi mogu uzrokovati disfunkciju trombocita, ali oni su obično klinički beznačajni. Samo nekoliko može izazvati krvarenje.
Acetilsalicilna kiselina blokira agregaciju trombocita, inhibicija se nastavlja tijekom života trombocita u cirkulaciji (7-10 dana), pa čak i jedna doza acetilsalicilne kiseline može prilično dugo blokirati osnovnu funkciju primarne hemostaze. Ako je u takvoj situaciji potrebno izvesti operacije, prikazan je recept desmopresina koji privremeno (na tri sata) uklanja produženje vremena krvarenja. Ponovno imenovanje desmopresina produžava njegovo djelovanje.
NSAID blokiraju sintezu tromboksana A2 - važnog medijatora agregacije trombocita. Njihovo djelovanje se može neutralizirati i propisivanjem desmopresina.
Otopine dekstrana smanjuju koncentraciju faktora VIII u plazmi, von Willebrand-ovog faktora, inhibiraju funkciju trombocita, produžujući vrijeme krvarenja. Unatoč dobrom djelovanju supstitucije volumena, transfuzija dekstrana u akutnom masovnom gubitku krvi ili u prisutnosti inicijalno intenzivne hemostaze (hemofilije, bolesti krvnog sustava, bolesti jetre itd.) Sada bi trebala biti svedena na minimum.
Klopidogrel, tiklopidin, kao i moderni inhibitori receptora za trombocite CPP / Sha (abciximab), koji se koriste u bolesnika s koronarnom srčanom bolešću (CHD) koji su pretrpjeli moždani udar ili infarkt miokarda, uzrokuju disfunkciju trombocita i povećavaju rizik od hemoragičnih komplikacija. U gotovo svim slučajevima primjena desmopresina pomaže u tim slučajevima, s izuzetkom situacije s primjenom inhibitora CPNH / Sha. U potonjem slučaju može biti potrebna transfuzija trombocita.
Von Willebrandova bolest je hemoragična dijateza naslijeđena od autosomno dominantnog tipa, uzrokovana oštećenjem ili nedostatkom von Willebrandovog faktora u plazmi. Faktor von Willebranda ima dvije glavne funkcije. Neophodan je za stvaranje trombocitnog čepa i štiti faktor VIII od cijepanja u plazmi. Postoje tri glavne vrste von Willebrandove bolesti (tablica 2-15).
Tablica 2-15. Willebrandova bolest: vrste i terapija Willebrandov faktor Terapija Kvantitativni nedostatak Desmopressin u većini slučajeva Kvalitativni nedostatak Desmopressin u blagim slučajevima; koncentrati faktora VIII koji sadrže von Willebrandov faktor; krioprecipitat Ukupna odsutnost koncentrata faktora VIII koji sadrže von Willebrandov faktor, krioprecipitat
Epidemiološke studije su pokazale da učestalost Willebrandove bolesti ne prelazi 1% u populaciji, ali se obično rjeđe dijagnosticira. Bolest prevladava kod žena s menorrhagijom. U svih bolesnika s krvarenjem treba utvrditi količinu von Willebrandovog faktora u krvi.
Prva vrsta bolesti je najčešća, čini 70-80% svih osoba koje pate od von Willebrandove bolesti. U ovom obliku bolesti smanjuje se broj normalno funkcionirajućih Willebrandovog faktora. Sklonost krvarenju obično se izražava umjereno, ali postoje i teške manifestacije.
Drugi tip karakterizira kvalitativna mana Willebrandovog faktora, uslijed mutacije u genu ovog faktora.
Treći tip karakterizira odsutnost von Willebrandovog faktora i smanjenje koncentracije faktora VIII u plazmi. Dijagnoza se obično temelji na laboratorijskim testovima, uglavnom na određivanju koncentracije i funkcije von Willebrandovog faktora i aktivnosti faktora VIII.
Terapija je usmjerena na normalizaciju triju parametara - sadržaja von Willebrandovih faktora i VIII, vremena krvarenja. To se postiže davanjem desmopresina, koji potiče endogenu hemostazu, i primjenom koncentrata faktora VIII koji sadrži von Willebrandov faktor. Desmopresin je učinkovit kod prvog, rjeđe kod drugog tipa von Willebrandove bolesti, a kod trećeg tipa nije učinkovit. Kada se daje intravenski, učinak je praktično karminantan, s potrebom za nastavkom liječenja, ponavljane doze se primjenjuju nakon 8-12 sati. U drugoj i trećoj vrsti von Willebrandove bolesti i u nedostatku učinka primjene desmopresina, u prvom se tipu terapija provodi koncentratima faktora VIII koji sadrže Willebrandov faktor. Čisti koncentrati faktora VIII se ne koriste jer faktor VIII ima vrlo kratak poluživot u nedostatku von Willebrandovog faktora. Svi koncentrati faktora VIII koji sadrže von Willebrand faktor dobiveni su iz plazme, stoga se moraju koristiti koncentrati koji su prošli virusnu inaktivaciju kako bi se izbjegla transfuzijska infekcija virusnim infekcijama. Virusna nesigurnost krioprecipitata ograničava njegovu uporabu u liječenju von Willebrandove bolesti. Ponekad, posebno s izraženim krvarenjem sluznice, pribjegavaju imenovanju inhibitora fibrinolize - primjeni traneksaminske kiseline.
Antikoagulansi, disaggregati, transfuzije dekstrana kontraindicirani su osobama s von Willebrandovom bolešću. Ne smiju im se davati intramuskularne injekcije, jer je rizik od intramuskularnih hematoma velik.
Kršenja kaskade koagulacije
Kod bolesti uzrokovanih patologijom kaskade koagulacije, nastajanje fibrina u konačnici je oslabljeno. S prirođenom prirodom bolesti ne postoji niti jedan faktor koagulacije u plazmi, dok kod stečenih bolesti postoji nekoliko nedostataka (na primjer, sekundarna hemostaza zbog bolesti jetre, nedostatak vitamina K, uporaba antikoagulansa).
Hemofilija AIV
Hemofilija je prirođena bolest sustava koagulacije, naslijeđena recesivnom vrstom spola i uzrokovana nedostatkom faktora VIII (hemofilija A) ili faktora IX (hemofilija B). Klinički su ta dva oblika bolesti identična, razlikuju se samo u istraživanju koncentracije svakog faktora u krvi.
Učestalost hemofilije A je jedna na 5 000 novorođenih dječaka, hemofilija B - jedna u 30 000 novorođenih dječaka. Prema tome, 80% bolesnika s hemofilijom ima hemofiliju A, 20% hemofiliju B.
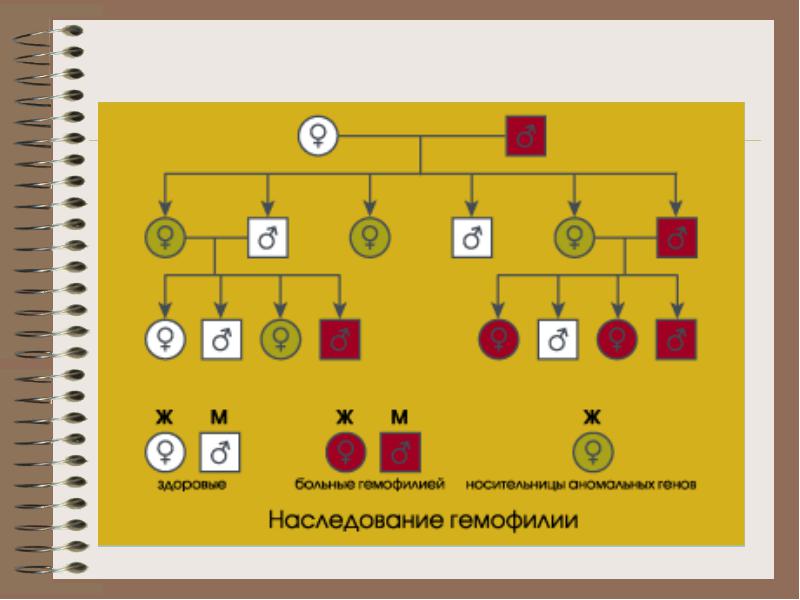
Geni faktora VIII i IX povezani su sa ženskim X kromosomom, tako da hemofilija pogađa samo muškarce, a žene postaju nositeljice. Kod ženskih nosača rizik od rođenja dječaka s hemofilijom je 25%, a kod djevojčice nositeljice također 25%. Kod muškaraca s hemofilijom kćer će uvijek biti nositelj, a sin će uvijek biti zdrav.
Kliničke manifestacije hemofilije ovise o koncentraciji faktora VIII ili IX u krvi. Njihova se aktivnost utvrđuje u međunarodnim jedinicama (IU). Normalna aktivnost faktora VIII ili IX iznosi oko 1 IU u 1 ml plazme. Postoje tri stupnja ozbiljnosti hemofilije (tablica 2-16).
Tabela 2-16. Jačina hemofilije Težina koncentracija faktora VIII, t / t Koncentracija faktora IX, IU / dl Blaga hemofilija A 5-25 100 Umjerena hemofilija A 1-4 100 Teška hemofilija A Intenzivna terapija obično je potrebna pacijentima s teškom hemofilijom, u kojem se mogu pojaviti spontana krvarenja i krvarenja u bilo kojim organima i tkivima, koji se ponavljaju. Krvarenja u zglobovima dovode do razvoja hemofilične artropatije, u mišićima - mogu izazvati sindrom kompresije, u mekim tkivima - stvaranje pseudotumara, koji se inkapsulira i, polako povećavajući kao rezultat opetovanih krvarenja, istiskuje okolna tkiva. Intrakranijalno krvarenje jedan je od najčešćih uzroka smrti bolesnika s hemofilijom.
Blagi oblik hemofilije često se ne prepoznaje do zrele dobi dječaka, kad se prvi put može otkriti je li potrebno izvesti bilo kakvu operaciju. Teška hemofilija obično se dijagnosticira kada dječaci napune 1-2 godine kada počnu hodati. Prvi znakovi mogu biti krvarenja u zglobovima, potkožni hematomi zbog djetinjastih poteškoća ili intramuskularnih injekcija. U koagulogramu se primjećuje produljenje APTTV-a kod normalnih brzina protrombinskog i trombinskog vremena, kao i vremena krvarenja. Dijagnoza se potvrđuje proučavanjem koncentracije faktora VIII, IX i Willebranda.
Za liječenje koriste se koncentrati faktora VIII ili IX, dobiveni iz donatorske plazme ili pomoću genske tehnologije. Suvremeni koncentrati faktora koagulacije sigurni su za virus i vrlo su učinkoviti. Za izračunavanje doze koncentrata faktora pretpostavlja se da krv primatelja ne treba zadržati barem 50% na dan operacije i tijekom
14 dana postoperativnog razdoblja. Obično se količina IU faktora VIII ili IX potrebna za jednu primjenu izračunava na sljedeći način:
volumen krvi (ml) = 7% tjelesne težine (kg); na primjer, 7% od 70 kg = 4900 ml;
volumen plazme (ml) = 60% volumena krvi (ml); 60% od 4900 ml = 2940 ml;
količina ME faktora VIII = 50% volumena plazme (ml); odnosno u našem primjeru 1470 IU.
Mnoštvo intravenskih primjena koncentrata faktora VIII - svaki
h, za faktor IX - svakih 12 sati
Otprilike 30% bolesnika s hemofilijom A u procesu liječenja koncentratima faktora VIII u krvi pojavljuju se antitijela koja blokiraju aktivnost prokoagulanta lijeka i zato se nazivaju inhibitorima. U hemofiliji B učestalost pojave inhibitora je manja. Titar inhibitora mjeri se u jedinicama Bethesde (BU). Jedna BU jednaka je količini inhibitora, koji inhibira 50% jedne jedinice faktora VIII, unesene u testni sustav. Povećanjem doze faktora može se prevladati niski titar BU (5-10 BU), međutim visok titar BU (preko 10 BU) onemogućuje hemostatski učinak, jer će cjelokupna količina ubrizgavanog lijeka biti blokirana antitijelima. Za uklanjanje antitijela preporučuje se plazmafereza (ne zamjenjujte uklonjenu plazmu donora FFP-a, jer sadrži faktor VIII), primjenu glukokortikoida. U novije vrijeme, rekombinantno aktivirani faktor VII i aktivirani koncentrat protrombinskog kompleksa postali su široko korišteni u takvim situacijama. Pri liječenju takvih bolesnika savjetovanje koagulologa je obavezno.
DEFICIJENCIJSKI FAKTOR VII
Faktor koagulacije VII, vezanjem na tkivni faktor, aktivira se i postaje polazna poluga od koje započinje proces koagulacije. Vrlo rijetko se dijagnosticira genetska varijanta urođenog nedostatka faktora VII. Klinički se očituje stvaranjem modrica s manjim ozljedama, produljenim nevezanim krvarenjima iz nosa i maternice. S ozbiljnim nedostatkom faktora VII (manjim od 1%) može doći do krvarenja, kao kod hemofilije, hemarthrosis, retroperitonealnih hematoma i intracerebralnih krvarenja. Istodobno, APTTV ostaje unutar normalnog raspona, ali se protrombinsko vrijeme i INR povećavaju. Za konačnu dijagnozu potrebno je proučiti aktivnost faktora VII u krvi.
Stečeni nedostatak faktora VII razvija se kod bolesti jetre, liječenja varfarinom, nedostatka vitamina K. Istovremeno će se u krvi smanjiti koncentracija ostalih faktora zgrušavanja ovisnih o vitaminu K - II, IX, X.
Terapija je supstitutivna. Kao izvor faktora VII koristi se FFP transfuzija, propisan je koncentrat protrombinskog kompleksa. Nedavno se u liječnikovom arsenalu pojavio rekombinantni aktivirani faktor VII, koji se dokazao u liječenju nedostatka faktora VII i u liječenju inhibicijskih oblika hemofilije i trombocitopeničnog krvarenja. Da bi se postigla hemostaza, potrebno je povećati koncentraciju faktora VII u pacijentovoj krvi na 15-20%. Preporučena doza rekombinantno aktiviranog faktora VII je 90-120 mg / kg intravenski svaka
3 sata za zaustavljanje krvarenja. Potrebno je laboratorijsko nadgledanje radi praćenja učinkovitosti i prilagođavanja doze, kao i uklanjanja mogućeg rizika od tromboembolijskih komplikacija.
OSTALI KONGENITALNI UČINCI PLASMANNIH FAKTORA
Manjak faktora XI (hemofilija C) je urođena hemoragična dijateza, koja je izražene etničke prirode i dijagnosticirana je uglavnom kod Židova i Armena. Ponavljano krvarenje različite lokalizacije (nazalno, menoragija, postporođajna, posttraumatska) nastaje kada je sadržaj faktora XI manji od 10%. APTTV produženo, protrombinsko vrijeme u granicama normale. Ako je nemoguće provjeriti laboratorijski nedostatak faktora XI u laboratorijskim uvjetima s pojačanim krvarenjem, potrebno je propisati transfuziju donora FFP-a. Namjena antifibrinolitikova (traneksamična i aminokapronska kiselina) je neučinkovita, a kontraindicirana je kod hematurije.
Afibrinogenemija je vrlo rijetka hemoragična dijateza, koja se očituje čestim spontanim teškim krvarenjima. Kada je hipofibrinogenemija, spontano krvarenje pojavljuje se samo u koncentraciji fibrinogena manjoj od 0,5 g / l. APTT i protrombinsko vrijeme značajno su produljeni. Dijagnoza se potvrđuje laboratorijskim ispitivanjem sadržaja fibrinogena. Terapija - transfuzija FFP-a, krioprecipitat ili koncentrat fibrinogena.
Disfibrinogenemija je heterogena skupina nasljednih bolesti s disfunkcijom fibrinogena. Ponekad se ova disfunkcija očituje otpornošću fibrin ugruška na fibrinolizu, češće - preosjetljivost na fibrinolizu. U prvom slučaju postoji tendencija povećane tromboze, u drugom - krvarenju. Liječenje nakon provjere dijagnoze (uz sudjelovanje koagulologa) - transfuzija FFP, rjeđe - imenovanje gena fibrino.
Izolirani urođeni nedostatak protrombina, faktori V, X,
XII, XIII u praksi liječnika intenzivne njege izuzetno je rijedak. Ti poremećaji nemaju određenu kliničku sliku, njihova dijagnoza zahtijeva ne samo probirne studije koagulograma, već i specifične analize koncentracije specifičnih faktora koagulacije. Kada se otkrije etiološki uzrok krvarenja, FFP se prelije.
ANTIFOSFOLIPIDNI SINDROM I ANTIKOAGULANTI RADA
Krvarenje sluznice u kombinaciji s manifestacijama venske ili arterijske tromboze na pozadini trombocitopenije s istodobnim otkrivanjem u krvi antifosfolipidnih antitijela i / ili lupusnog antikoagulansa karakterizira antifosfolipidni sindrom i njegov teški oblik - katastrofalni antifosfolipidni sindrom. Ovaj se sindrom pojavljuje kod sistemskog eritematoznog lupusa, kolagenoze, raka, infekcija i trudnoće. Mnogi su slučajevi katastrofalnog antifosfolipidnog sindroma idiopatske prirode. Temelj ovog sindroma je stvaranje autoantitijela usmjerenih protiv fosfolipida, posebno kardiolipina. Potonji tvori kompleks s proteinom (32-glikoprotein-1 (p2-CPl), koji je dio protrombina. Iz tog razloga, plazma bolesnika s katastrofalnim antifosfolipidnim sindromom ima antikoagulacijsko djelovanje, a o sadržaju lupusnog antikoagulansa može se prosuditi o stupnju ove aktivnosti. U slučaju antifosfolipidnog sindroma, svi testovi ovisni o protrombinu će se produžiti, dok, unatoč produljenju APTT i UIGO, vrijeme koagulacije t U1UO nije poremećeno, što određuje visoki rizik od tromboze u slučaju antifosfolipidnog si Dre.
Terapija za katastrofalni antifosfolipidni sindrom je složena. Protiv pozadine plazmafereze propisan je UFG, prednizon. Uz neučinkovitost provode pulsnu terapiju metilprednizolonom. Uklonjena plazma nadoknađuje FFP donora. Često, s potpunom trombozom mezenteričnih žila, potrebno je pribjeći kirurškoj intervenciji, što značajno pogoršava prognozu.
KRIVA ŽIVOTA
Sveobuhvatni poremećaj hemostatske ravnoteže uslijed smanjenja sinteze mnogih faktora zgrušavanja i inhibitora jetrenih bolesti prati razvoj patološkog krvarenja. To smanjuje broj i funkcije trombocita, povećava fibrinolizu, produžuje vrijeme protrombina, povećava INR. Često splenomegalija koja se primjećuje kod ciroze jetre pogoršava trombocitopeniju. U slučaju jakog krvarenja ili kirurške intervencije, propisana je FFP transfuzija, primjena rekombinantnog aktiviranog faktora VII, protrombinskog kompleksa. Traneksaminska kiselina i desmopresin djeluju kratko.
Diseminirana intravaskularna koagulacija
DIC je potpuni prekid interakcije svih sustava hemostatske ravnoteže, koji određuju njegovu ravnotežu, što uključuje endotelne stanice, hemostazu trombocita (primarnu) hemostazu, koagulacijski sustav plazme i fibrinolizu. Za ICE je karakteristična istodobna prisutnost krvarenja i mikrotromboze, što dovodi do brzog razvoja organa i PON. Dešifriranjem fenomena ICE-a (u kojem su djela MS Machabeli i ZS Barkagana igrali vodeću ulogu u našoj zemlji) objasnio je mnoge naizgled različite fenomene koji prate takva formalno različita kritična stanja kao što su sepsa, masivni gubitak krvi, opekotine i ugrizi zmija. , komplikacija trudnoće itd.
U praksi intenzivne njege ICD se najčešće razvija na pozadini sepse, masovnog gubitka krvi (posebno u akušerstvu), ozljeda, karcinoma i hematoloških bolesti.
MEHANIZAM ETIOLOGIJE I RAZVOJA
Razvoj ICE-a može biti posljedica različitih uzroka i stanja, kako je prikazano u nastavku. Češće ICE poprima karakter akutnog (munje) tijeka, rjeđe se opaža kronični tijek.
Uzroci DIC-a:
Šok (hipovolemija i hipoksija) bilo koje etiologije.
Infekcija.
Sepsa.
Bakterijska.
Virusni.
Gljivične.
ozljeda
Burns.
Crash sindrom
-CHMT.
Masna embolija.
Velike operacije.
Komplikacije u trudnoći i porodu
Teška eklampsija.
Aplantacija placente.
Fetalna smrt fetusa.
Embolija amnionske tekućine.
NENR sindrom.
anafilaksija
uvreda
Akutna intravaskularna hemoliza
Vaskularna protetika
Zmija ugrize
neoplazme
Adenokarcinom.
Hematoloških zloćudnih bolesti.
Bolest jetre
Ciroza.
Akutni fulminantni hepatitis.
Patološka aktivacija veza sustava hemostaze može biti uzrokovana različitim čimbenicima. Aktivacija endotelnih stanica endotoksinom kod infekcija, trovanja, acidoze i hipoksemije popraćena je pojavom tkivnog faktora na površini njihove membrane. Sustav koagulacije plazme aktivira se oslobađanjem tkivnog faktora kao posljedica traume, sepse, komplikacija trudnoće, blastemije s hemoblastozom.
Sustavna aktivacija koagulacije dovodi do stvaranja u krvotoku prevelike količine cirkulirajućeg trombina, što uzrokuje generalizirano stvaranje fibrina, aktiviranje i potrošnju faktora VIII i V, kao i aktiviranje trombocita. Kao rezultat toga, pokreće se proces masivne mikrotrombogeneze u sustavu mikrocirkulacije, što dovodi do razvoja PON i pogoršava oštećenja endotelnih stanica. S druge strane, generalizirana tvorba fibrina aktivira fibrinolitički sustav, fibrinolitički aktivatori se aktivno oslobađaju iz aktiviranih endotelnih stanica, trombocita i leukocita.
Takva masivna sistemska aktivacija hemostaze dovodi do brze potrošnje svih faktora zgrušavanja, trombocita i inhibitora. Potrošnja trombocita u ICE može ići vrlo brzo, njihova proizvodnja koštane srži nema vremena za nadoknađivanje cirkulacijskog bazena trombocita. Uz to, cirkulirajući trombociti postaju funkcionalno oštećeni kao rezultat izloženosti produktima razgradnje fibrina. Kod bolesti jetre smanjena sinteza proteina uslijed zatajenja jetre doprinosi produbljivanju deficita koagulacijskih faktora i njihovih inhibitora. Uz to, važno je patološko uništavanje faktora koagulacije bakterijskim proteazama u sepsi, enzimima gušterače kod pankreasne nekroze ili blizu fetalne tekućine u emboliji amnionske tekućine. Rezultat ovih procesa je krvarenje zbog trombocitopenije, hiperfibrinolize i nedostatka faktora zgrušavanja.
KLINIČKE MANIFESTACIJE
Spektar kliničkih manifestacija DIC-a ovisi i o uzroku, koji ga je uzrokovao (DIC je uvijek sekundarni, to nije nozološki oblik, nego sindrom uvijek povezan s velikom bolešću) i uvjetima povezanim s njegovim razvojem. U akutnom toku DIC-a, njegove manifestacije mogu biti znakovi PON, što ukazuje na oštećenje CNS-a, bubrežnu, jetrenu, plućnu disfunkciju. Karakteristične su metabolička acidoza, proteinurija, hipoksija, hipotenzija i groznica. Hemoragični simptomi uključuju petehije i ekhimozu na koži, spontano krvarenje sluznice, krvarenje s mjesta ubrizgavanja i kirurške rane, u težim slučajevima - intracerebralne hemoragije. Mikrotromboza uzrokuje ishemijska oštećenja unutarnjih organa, uglavnom mozga, pluća, bubrega i jetre. Tromboza posuda dermisa i subderma popraćena je akrocijanozom, mogućim razvojem gangrene prstiju ili stopala. Ishemijski znakovi DIC-a očituju se neurološkim oštećenjem svijesti (letargija, brza iscrpljenost i monosilbilnost u odgovorima na pitanja), hipoksemijom i hipoksijom s oštećenom frekvencijom i respiratornim ritmom, oligurijom ili anurijom, hipoalbuminemijom i hipoprotrombinemijom.
DIJAGNOZA
Primarna dijagnoza DIC-a u potpunosti se temelji na kliničkoj slici, uključujući hemoragične i ishemijske znakove. Razlikuju se hiper- i hipokoagulacijske faze akutnog DIC-a, a hiperkoagulativnu fazu DIC-a treba razlikovati od kroničnog hiperkoagulacijskog sindroma (statusa), koji se u osnovi razlikuje od DIC-a u pogledu patogenetskih i kliničkih i laboratorijskih podataka.
Hiperkoagulativni sindrom - povećana spremnost krvi za zgrušavanje, kompenzirana mehanizmima protiv zgrušavanja. Kada nema niti lokalni ili diseminirani krvni ugrušci u vaskularnom sustavu, nema kliničkih manifestacija tromboze. Ali u laboratorijskim podacima primjećuje se skraćenje APTT-a, protrombinsko vrijeme, povećana aktivnost trombocita, smanjena fibrinoliza, brzo stvaranje ugruška u epruveti.
Hiperkoagulacijska faza DIC-a često je prolazna, a liječnik je ne može dijagnosticirati. Pojavljuju se klinički znakovi ishemije organa. Svi laboratorijski znakovi hiperkoagulacije (APTT, protrombin, aktivacija trombocita) su izraženi, ali istodobno se pojavljuju prvi početni znakovi potrošnje faktora koagulacije - količina trombocita, koncentracija antitrombina III, protein C nije oštro smanjena. ali je labav i nestabilan. Važan simptom je često brza tromboza igle ili katetera tijekom intravenske punkcije.
Hipokoagulacijsku fazu DIC-a karakteriziraju znakovi difuzne hemoragične dijateze (petehijalno-ehhimsko krvarenje) i laboratorijski biljezi potrošnje faktora koagulacije sustava hemostaze - produljenje vremena krvarenja, APTT, protrombinsko vrijeme, značajno smanjenje broja trombocita i njihovih invaliditeta. koncentracije fibrinogena, faktor VIII, pojava B-dimera.
TRETMAN
Osnova terapije ICE-a je olakšanje početnog patološkog procesa koji ga je započeo. Međutim, etiološka terapija ovih bolesti (antibiotici za sepsu, kemoterapija ili operacija na tumorima, plazmafereza za akutnu intravaskularnu hemolizu itd.) Daje učinak tek nakon određenog vremenskog razdoblja. Zato su istodobne terapijske mjere toliko važne za osiguravanje obnove i održavanja BCC-a, odgovarajuće oksigenacije, korekcije hipotenzije kako bi se poboljšala mikrocirkulacija.
Istodobno, kritično stanje pacijenta, pogoršano manifestacijama DIC-a, zahtijeva brzu transfuzijsku korekciju poremećaja u hemostatskom sustavu.
U terapiji hiperkoagulacijske faze DIC-a, kada postoje kliničke manifestacije ishemije organa uslijed mikrotromboze, propisan je natrijev heparin. Natrij heparin inhibira aktivnost trombina, smanjujući tako stvaranje fibrina. Obično se propisuje 8-10 MEDKHH) uz kontinuirano intravenozno davanje raspršivača ljekovitih tvari (infusomat). Treba imati na umu da natrijev heparin djeluje učinkovito pod uvjetom da u krvnoj plazmi postoji dovoljna količina antitrombina III. Njegovim smanjenjem potrebno je transfuzirati FFP (10 ml / kg) ili propisivati komercijalne pripravke antitrombina III (do 3000 IU / dan). Kriterij za djelotvornost terapije natrijevim heparinom bit će smanjenje koncentracije produkata razgradnje fibrina i B-dimera, porast sadržaja fibrinogena, skraćenje protrombinskog vremena. Upotreba heparina niske molekularne težine u ovoj situaciji je nepraktična zbog njihove neučinkovitosti i nemogućnosti praćenja. U liječenju DIC-sindroma septičke etiologije, dobro se preporučila aktivirani protein C, koji kao antikoagulans inhibira aktiviranje faktora V i VIII i smanjuje stvaranje trombina.
Mnogo češće liječnik intenzivne njege susreće se s hipokoagulacijskom fazom DIC-a, u transfuzijskoj terapiji kojoj vodeća uloga pripada nedostatak faktora koagulacije. DIC je složeno kršenje hemostatskog sustava, stoga "prva violina" u njegovom liječenju svira transfuzijom FFP - složenog transfuzijskog medija u kojem optimalni set sadrži sve potrebne faktore koagulacije. Svrha transfuzije FFP je povećati koncentraciju fibrinogena iznad 1-1,5 g / l. Terapijska doza smatra se FFP transfuzijom brzinom od 15-20 ml / kg. U nedostatku hemostaze, moguće je ponovno uvesti FFP pod laboratorijskim nadzorom koncentracije faktora koagulacije. Ponekad je potrebno dodati antitrombin III preparate za transfuziju FFP-a, posebno ako je njegova koncentracija u krvi manja od 70%. Uz prijetnju cirkulacijskog preopterećenja kako bi se smanjio volumen pribjegavao transfuziji krioprecipitata (jedna doza na 10 kg tjelesne težine). Uporaba plazmafereze u liječenju DIC-a usmjerena je kako na terapiju osnovne bolesti (na primjer, akutna intravaskularna hemoliza zbog transfuzije crvenih krvnih stanica koja je nespojiva s antigenima sustava ABO), tako i na sprječavanje cirkulacijskog preopterećenja kada su potrebne velike količine plazme.
Transfuzija trombocita u DIC-u indicirana je samo s razvojem krvarenja i smanjenjem njihovog broja manjim od 50x109 / l. Svrha transfuzije trombocita je prekoračiti tu vrijednost, za koju je u pravilu potrebna jedna jedinica koncentrata trombocita (55-70x109) na 10 kg tjelesne težine po transfuziji. Uz izraženu potrošnju trombocita, potrebne su ponovljene transfuzije svaka 24 sata.
Transfuzija crvenih krvnih stanica prikazana je samo iz zdravstvenih razloga s provjerenim znakovima hipoksemije i hipoksije tkiva zbog nedostatka crvenih krvnih stanica u krvotoku.
Važno je zapamtiti da neki pacijenti s laboratorijskim znakovima DIC-a nemaju kliničke manifestacije tromboze ili sklonost krvarenjima. Takvim pacijentima nije potrebna transfuzijska korekcija hemostaze, trebaju provesti terapiju za osnovnu bolest.
POPIS LITERATURE ^
Praktična transfuziologija / Ed. vojnik Kozinets. - M .: Praktična medicina, 2005. - 544 str.
Shevchenko Yu.L., Shabalin V.N., Zarivchatsky MF, Selivanov E.A. Vodič za opću i kliničku transfuziologiju. - SPb .: Foliant, 2003. - 608 str.
KN ^ aags! T., Tahapega U.R.K., Voyzhs! K. e * a1. RNagtasoktellls $ o ^ gesotp: aPu ^ es! ^ asShg VII t 1gayita rayep ^ t1 \\\\ zeuege YYes11p§ // Sp1. Saga. - 2006. - Wo1. 10. - P. 104.
MagIposhIg II., Kepe * S., 5e§a1 E. e1 a1. KesoshPap !; asPua ^ es! Gus ^ og VII bf prisvajajući ltoggagaga sopt1t 1t; hod //]. Tgaita. - 2001. - Wo1. 51. - P. 431-438.
Utsep!:] .B., Ko $$ am1: K., Cui V. e * a1. Kesottepsa1: Yup $ op 1bе i $ e o! "Hesottap! Asy-ua * es1 ^ as1; og VII az a af" ipsuye 1; gea1: tep1; Gogta $$ 1ue Yess 11p§ - a Ëeorep regresresIue // Cn. (Sag. - 2006. - Wo1. 10. - str. 120
Pacijent s skorbutom ima krvarenje desni i petehije na koži. Što uzrokuje poremećaje hemostaze kod ove bolesti?
A. @ Kršenje sinteze kolagena
B. Trombocitopenija
C. Višak antikoagulansa
D. Aktivacija fibrinolize
E. Manjak prokoagulansa
Dječak s hemoragičnim sindromom nema antihemofilni globulin A u krvi (faktor VIII). Kakav je mehanizam neuspjeha hemokoagulacije u ovog pacijenta?
@ Unutrašnji mehanizam nastanka protrombinaze
Konverzija fibrinogena u fibrin
Vanjski mehanizam nastanka protrombinaze
Pretvorba protrombina u trombin
Uvlačenje krvnog ugruška
Muškarac koji je dvije godine bolovao od kronične mijeloidne leukemije, primljen je u bolnicu u stanju akutnog zatajenja bubrega. Što bi mogao biti uzrok akutnog zatajenja bubrega u ovog pacijenta?
@DIC - sindrom
limfopenija
neutropenija
trombocitopenija
Nedovoljna aktivnost bilo koagulacijskih faktora uzrokuje razvoj hemoragičnog sindroma u bolesnika s hipovitaminozom K?
X, IX, VII, II
Von Willebrand faktor
Pacijent koji je sustavno konzumirao acetilsalicilnu kiselinu razvio je krvarenje. S padom aktivnosti kojih enzima trombocita je povezan razvoj trombocitopatije u ovom slučaju?
@ Ciklo-oksigenaza
lipoksigenzaza
peroksidaze
Citokrom oksidaza
Glukoza - 6 - fosfat dehidrogenaza
Djevojka periodično ima krvarenje iz nosa, na koži postoje mali hemoragični osipi. Pregledom je utvrđeno: vrijeme krvarenja - 10 minuta, smanjena sposobnost lijepljenja trombocita i niska aktivnost f. VIII (VIII: C). Koja je bolest kod djeteta?
@ Bolest Von Willebranda
Hemofilija A
Hemofilija B
Nasljedna disfibrinogenemija
trombocitopenija
Nakon što je patila od angine, 5-godišnja djevojčica ima petehijalni osip na koži torza i ekstremiteta, krvari iz desni. Pregledom je utvrđeno smanjenje broja trombocita u krvi. Na kojoj se razini trombocitopenije (g / l) pojavljuju njeni klinički znakovi?
Koja bi mogla biti glavna veza u patogenezi trombofilije u bolesnika koji pati od tromboflebitisa donjih ekstremiteta?
@ Nedostatak antikoagulansa
trombocitopenija
thrombocytopathy
Manjak prokoagulansa
U svrhu dijagnosticiranja promjene u sustavu hemokoagulacije propisano je ispitivanje razine produkata razgradnje fibrina u krvi?
thrombocytopathy
trombocitopenija
Vazopatija hemoragična
Pacijentu je dijagnosticirana genetska oštećenja membranskog receptora za von Willebrandov faktor - glikoprotein (GP) Ib, koji je odgovoran za početnu fazu adhezije trombocita na kolagen. Kako se zove ova bolest?
@ Bernard - Soulier
Von Willebrand
Addison - Birmera
Wilson - Konovalova
Glanzmana - Negeli
Pacijentu je dijagnosticiran nasljedni defekt GP IIb - IIIa - membranski receptor koji omogućava vezu fibrina s membranom trombocita i potreban je za njihovu agregaciju. O kojoj bolesti govorimo?
@Glancman - Negeli
Von Willebrand
Addison - Birmera
Wilson - Konovalova
Bernard - Soulier
U djeteta s kombiniranom imunodeficijencijom, testom krvi utvrđeno je smanjenje adhezije trombocita na kolagen, njihova agregacija, slabljenje koagulacije krvi i povlačenje ugruška u krvi. Pod kojim imunodeficijencijom se primjećuju slične promjene?
@ Whiskott - Aldrich
Švicarskog tipa
Di - Georgie
Nezelofa
Bolesnoj djevojci dijagnosticirana je Glantsmannova trombasthenija. Koje poremećaje u sustavu hemostaze se događaju u ovom slučaju?
@Disaggregacijska trombocitopatija
Apsolutna trombocitopenija
Disadesivna trombocitopatija
Nedostatak trombocitopatije
Distegranulacijska trombocitopatija
Članovi ekspedicije koji su bili na sjeveru žale se na gingivalno krvarenje i petehijalne krvarenja na koži. Iz anamneze se zna - u prehrani nije bilo dovoljno askorbinske kiseline, a to je dovelo do krhkosti vaskularne stijenke. Koja je patogeneza vazopatije?
@ Dysplastic
upalni
metaplastičnim
dystrophic
imun
Kod pacijenta nakon duže operacije na gušterači, postoperativna rana dugo je krvarila. Prema koagulogramu utvrđeno je značajno povećanje razine plazmina. Koja je patogeneza koagulopatije promatrana u ovom slučaju?
@ Fibrinopatija
Protrombinazopatiya
Tromboplastinopatiya
Trombinopatiya
Vazopatiya
Pacijentu se dijagnosticira genetska oštećenja faktora V koja postaje neosjetljiva na inaktivaciju antitrombotskim kompleksom trombomodulin - protein C, koji smanjuje sposobnost vaskularne stijenke da ograniči stvaranje fibrina. Koja će se patologija zgrušavanja krvi pojaviti s ovom anomalijom?
'trombofiliju
trombocitopenija
thrombocytopathy
Hemoragični sindrom
Kompleks mehanizama koji podržavaju krv u tekućem stanju, bez koagulacije u lumenu posude ili istjecanja kroz vaskularni zid nazvan je hemostazom. Budući da su patološka stanja povezana s koagulacijom krvi obrađena u sljedećem predavanju, ovdje treba razmotriti i druge promjene povezane s oštećenom hemostazom.
Krvarenje (krvarenje, od grč. Haima - krv i rak - protok) je protok krvi izvan vaskularnog kreveta ili srca u okoliš (vanjsko krvarenje) ili u tjelesnu šupljinu, lumen šupljeg organa (unutarnje krvarenje). Primjeri vanjskog krvarenja su metroragija (maternica), melena (crijevna) i unutarnja krvarenja - hemopericardium, hemotoraks, hemoperitoneum i hemarthrosis (u šupljinu perikarda, pleure, trbušne šupljine ili zgloba, respektivno).
Ovisno o izvoru krvarenja, dijele se na arterijska, venska, arterijsko-venska (mješovita), kapilarna, parenhimska (kapilara iz parenhimskih organa) i srčana.
Posebna vrsta krvarenja je hemoragija u kojoj se krv nakuplja ekstravaskularno u tkivima. Postoje četiri vrste:
Hematoma - krvarenje s oštećenom cjelovitošću tkiva i stvaranjem šupljine;
Hemoragično namakanje (infiltracija) - krvarenje uz očuvanje integriteta tkiva;
Modrica (modrica) - planarno krvarenje u koži, potkožnom tkivu, sluznici;
Petechiae - ukazuju na krvarenja na koži, sluznici i seroznim membranama, unutarnjim organima.
Višestruka petehijalna krvarenja, koja se spajaju u veće, nazivaju se hemoragična purpura, a modrica promjera do 2 cm naziva se ekhimoza.
Mehanizmi razvoja i krvarenja i krvarenja uključuju:
Ruptura (hemoragija po reksinu) koja je posljedica ozljeda nepromijenjene žile ili nekroze (ruptura srca kod infarkta miokarda), upale (sifilitični mesaortitis s rupturom aorte), aneurizma zahvaćene vaskularne stijenke;
Koroziju (haemorragia po diabrosin) ili arrosive krvarenja koji se razvija u uništavanju upale krvožilne stijenke (više gnojni), malignog tumora nekroze (kazeozne nekroze krvarenje tuberkulozan šupljine), izloženost kemikalijama (želučani sok može uzrokovati krvarenja čireva na želucu), klijanje viliji korionskih žila maternične cijevi u izvanmateričnoj trudnoći;
Dijapedesis (hemoragija per diapedesin, s grč. Dia - kroz, pedao - skakanje), karakterizirana krvnim ishodom zbog povećane propusnosti vaskula, u pravilu, netaknutim žilama mikrovaskulacije u teškoj hipoksiji, intoksikaciji, infekciji, različitim koagulopatijama, hemoragijskoj dijatezi. Relativno često se krvarenja u diapedi razvijaju u hipertenzivnoj krizi, sistemskom vaskulitisu, leukemiji, hemofiliji, uremiji.
Sklonost spontanom krvarenju ili krvarenju kao odgovor na čak i manje oštećenje nazvana je hemoragična dijateza. Ovo je stanje povezano s kvalitativnim ili kvantitativnim promjenama trombocita, nedostatkom hemokoagulacije, patološkom krhkošću ili povećanom propusnošću vaskularnog zida, nasljednim i stečenim.
Glavni uzroci krvarenja (krvarenja) su:
1. Povećana krhkost vaskularnog zida primjećena je kod njegovih urođenih oštećenja, infekcija i intoksikacija, hipo- i beriberija, terapije steroidima;
2. Oštećenja trombocita. Tu spadaju trombocitopenija bilo kojeg podrijetla, nasljedna ili stečena slabljenja adhezije (von Willebrandova bolest, Bernard-Soulier, nasljedna hemoragijska dijateza itd.), Oslabljena agregacija ili smanjenje izlučivanja trombocita;
3. Nedovoljnost urođenih faktora koagulacije (hemofilija A faktorom VIII, hemofilija B faktorom IX, von Willebrandova bolest, ostali faktori zgrušavanja krvi) ili češće stečenog porijekla (s bolestima jetre, nedostatkom vitamina K, nekim imunološkim lezijama);
4. Prekomjerna intravaskularna koagulacija, na primjer, u diseminiranoj intravaskularnoj koagulaciji krvi - DIC (vidjeti sljedeće predavanje).
Ishod krvarenja može biti povoljan (resorpcija strujeće krvi, organizacija, inkapsulacija, stvaranje "zahrđale" ciste) i nepovoljan (suppuration kada je infekcija priključena).
Vrijednost krvarenja je zbog njegovog izgleda, ozbiljnosti i trajanja. Dakle, ruptura srca u infarktu miokarda s stvaranjem hemopericardija brzo dovodi do smrti pacijenta, iako ukupna količina krvarenja obično nije veća od 100-200 g. Uz arterijsko krvarenje može se razviti masivan gubitak krvi i akutna anemija sa smrtnim ishodom. Dugotrajno manje krvarenje iz kroničnih čira na želucu ili dvanaesniku uzrokuje kroničnu posthemoragičnu anemiju. Vrijednost krvarenja ovisi, prije svega, o njegovoj lokalizaciji, a tek potom o veličini. Čak i mala krvarenja u mozgu mogu prouzročiti oštećenje vitalnih centara, oticanje mozga i smrt pacijenta, dok čak i masivna nekomplicirana krvarenja u potkožnom tkivu ne predstavljaju opasnost za život.
Plazmoragija je izlaz iz lumena krvne žile s impregnacijom okolnih tkiva (natapanje plazmom) zbog povećane vaskularne propusnosti. Plazmoragija se pojavljuje transendotelno zbog ultrafiltracije (izlazak plazme kroz pore bazalne membrane endotela uslijed povećanja hidrostatskog ili osmotskog tlaka), difuzije (zbog gradijenta komponenti plazme u lumenu i van posude), mikrovezikularnog transporta (mikropinocitoza ili citotemisitisa) koji nastaju kao rezultat aktivnosti aktivnosti. , Moguće je i inter-endotelno oslobađanje plazme. Dakle, plazmoragija se određuje oštećenjem vaskularnog zida (prvenstveno njegove intime) i promjenom konstanta krvi. Morfološka studija vaskularne stijenke mikrocirkulacijskog sloja zadebljava se, postaje homogena, a tijekom elektronskog mikroskopskog pregleda u natečenim endotelnim stanicama uočava se veliki broj mikrovestikula, stvaranje fenestra i tunela, pojava međućelijskih pukotina, labavljenje intimne bazne membrane. Akumulacija komponenti plazme dovodi do oštećenja stanica i međućelijske tvari u vaskularnom zidu i perivaskularnom tkivu, na kraju kojih se razvija hialinoza, a u težim slučajevima - fibrinoidna nekroza.
Šok je teško patološko stanje karakterizirano kolapsom cirkulacije (akutno zatajenje cirkulacije) nakon supermočne izloženosti hemostazi. Razlikuju se hipovolemični, srčani, septički i vaskularni tipovi šoka.
Hipovolemički šok uzrokovan je brzim smanjenjem volumena cirkulirajuće krvi za 20% ili više, što se primjećuje u akutnom gubitku krvi i dehidraciji. Dakle, gubitak tekućine i elektrolita moguć je s velikim opeklinama (zbog oslobađanja plazme iz oštećene mikrovaskulature), s jakim povraćanjem, obilnom proljevom.
Srčani šok razvija se kao odgovor na smanjenje volumena moždanog udara sa srčanim lezijama, opažen je kod infarkta miokarda, teškog miokarditisa, akutne mitralne ili aortne insuficijencije, tromboze protetskih zalistaka, rupture interventrikularnog septuma, hemo tampona srčane košulje. Izražen pad krvnog tlaka dovodi do značajnog smanjenja opskrbe krvlju u tkivima, slično hipovoemijskim promjenama.
Septički (toksično-infektivni) šok nastaje kada postoji infekcija uzrokovana gram-negativnom (E. coli, Proteus, Klebsiella, itd.) Rjeđe gram-pozitivnom (stafilo-, strepto-, pneumokoki) mikroflorom. Izlučeni toksini (prije svega endotoksini) aktiviraju sustav komplementa, koagulaciju, fibrinolizu, kao i trombocite i neutrofile. Kao rezultat, potiče se stvaranje dušičnog oksida (moćan vazodilatator), faktora nekroze tumora a i interleukina, koji izazivaju akutno zatajenje cirkulacije.
Vaskularni (redistributivni) šok može biti neurogen (traumatičan, bolan, s oštećenjem leđne moždine, kao komplikacija anestezije) ili anafilaktički, uzrokovan generaliziranim reakcijama preosjetljivosti. Zbog izražene vazodilatacije, povećane propusnosti kapilara i arteriovenskog pražnjenja, intravaskularni volumen krvi se redistribuira, praćen značajnim padom ukupnog perifernog vaskularnog otpora.
Šok u svom razvoju prolazi kroz tri faze:
1. Neprogresivni (rani) stadij šoka karakterizira pad krvnog tlaka i srčanog izlaza uz održavanje vitalnih organa s relativno normalnom opskrbom krvlju. To je zbog kompenzacijskog vazokonstrikcije žila, posebno kože i crijeva. Iscrpljivanjem adaptivnih mehanizama šok prelazi u sljedeću fazu;
2. Progresivni stadij šoka karakteriziran je izraženim kliničkim simptomima, dubokim kolapsom zbog slabe opskrbe krvlju svih organa i tkiva (hipoperfuzija tkiva zbog povećanja dilatacije arterija), razvojem metaboličkih i krvožilnih poremećaja. 3. U nepovratnom stupnju šoka postoji izražena cirkulatorna insuficijencija na razini mikrovaskularne kršenja s kršenjem integriteta vaskularne stijenke, brzo povećanje multiorganskog zatajenja, što rezultira smrću pacijenta.
Morfološki pregled pokazuje generalizirane distrofične i nekrotične promjene, pojave DIC sindroma (petehijalna krvarenja, stasis, krvni ugrušci u mikrovaskulaturi). Osim toga, zbog osobitosti strukture i funkcioniranja različitih organa, u svakom od njih nastaju osebujne promjene - šok organa. Dakle, razvoj nekrotične nefroze (nekroza epitela zglobnih tubula) karakterističan je za šok bubrega. Šokna pluća očituju se žarištem atelektaze, seroznim hemoragičnim edemom, ponekad gubitkom fibrinskih filamenata (hijalinskih membrana). U mozgu se javlja ishemična encefalopatija koja se očituje edemom, punktatnim krvarenjima i žarištima nekroze. U srcu se opažaju mala, uglavnom subendokardna žarišta krvarenja i nekroze miokarda, masna degeneracija kardiomiocita s znakovima njihove povučenosti. U kortikalnom sloju nadbubrežne žlijezde dolazi do potpunog nestanka lipida koji se koriste za sintezu steroidnih hormona. U gastrointestinalnom traktu otkrivaju se krvarenja, erozije i akutni čirevi na sluznici. Šok jetre razlikuje se masnom distrofijom hepatocita, a u nekim slučajevima čak i centrolobularnom nekrozom.
Prognoza šoka ovisi o njegovoj vrsti, ozbiljnosti, fazi u kojoj se započinje liječenje, prisutnosti komplikacija. Trenutno, s teškim kardiogenim ili septičkim šokom, smrtnost doseže 50% ili više.
Hemostatski poremećaji
Kompleks faktora i mehanizama koji osiguravaju optimalno agregacijsko stanje krvi.
Za procjenu sustava koagulacije krvi izvode se testovi:
Vrijeme, trajanje krvarenja. Ubodite prst i ispupčenu kap umočenu u komad papira. Norma - 45-180 sekundi.
Vrijeme ugruška prema Lee-Whiteu. Uzmite u epruvetu i pomičite se do pojave fibrinskih filamenata. Norma - 6-9 minuta.
Kao odgovor na oštećenje krvožilnog sustava dolazi do spazma vaskularne stijenke. Trombociti sežu u oštećenu posudu, lijepe se na stijenku žila (prianjanje). Trombociti trombocita su zalijepljeni zajedno i formirani. Ti mehanizmi su vaskularna hemostaza trombocita.
Fazna koagulacija.
Koagulacijska hemostaza. Njegova aktivacija može se dogoditi na 2 načina:
Mehanizam je unutarnji, aktivira se uz pomoć kolagena, proteaze ili adrenalina, ti čimbenici dovode do činjenice da: XII faktor Hageman se, kad se aktivira, pretvara u aktivni protein (skupina aminokiselina propada i to je aktivni oblik)) XIIa a XI IX VIII - nužno uz sudjelovanje Ca ionov iona u stvaranju aktivne protrombinaze (tromboplastina).
Mehanizam - vanjski - oštećenje tkiva. Tkivni tromboplastin (III) doprinosi prijelazu faktora VII u aktivni oblik, a rezultat toga je stvaranje aktivne protrombinaze.
U prvoj fazi sudjeluju koagulacija krvi - 7, 8, 9 faktora koagulacije.
Zgrušavanje krvi
Aktivna protrombinaza (trombokinaza) pretvara se u trombin. Ima dvije podfaze:
Stvaranje enzimske doze trombina.
Pod djelovanjem vatrene doze trombina, prokonvertin (VII) prelazi u konvertitin (VIIa). Convertin vraća postupak koagulacije u 1. fazi
Proaccelyrin (V) prelazi u Accelerin (Va) - ubrzava koagulaciju krvi.
Stvaranje rezultirajuće doze trombina. Radite protrombin, proaccelin, proconvertin.
Trombin djeluje na fibrin, formirajući fibrinogen. Polimerizacija i stabilizacija. Fibrinogen - fibrinomnomer - fibrin oligomeri - fibrinpolimeri.
Faza - fibrinoliza.
XII XIIa plazminogen - plazmin (glavni faktor fibrinolitičkog sustava) fibrin se raspada na produkte razgradnje fibrina (proizvodi fibrinolize aktiviraju koagulaciju faze 1).
Sustav hemostaze.
Hemoragična dijateza.
Podijeljeni su prema štetnoj komponenti hemostaze:
Vazopatii:
nasljedna:
telangiektazija ili Randyus-Oslerova bolest - autosomno dominantno nasljeđe, to jest, nedostatak u strukturi vaskularne stijenke, postaje tanji i nastaju vrećaste ektaze. Lokalizacija: usne, gornji torzo, lice, vlasište, sluznica, šupljine. Ti razređeni zidovi su dobro ozlijeđeni. Pacijent ima kroničnu anemiju nedostatka željeza zbog kroničnog gubitka krvi.
stečena:
Hipovitaminoza C (skorbut), PP - neophodna za polimerizaciju vaskularne stijenke - pacijent ima petehije, vaskulitis. Na simetričnoj koži.
Hemoragični vaskulitis (Schönlein-Genochova bolest):
Uzorci otpora vaskularne stijenke: Konchalovsky (pritisak u manžetu se vrši pritisak na određenu vrijednost, tada se broji broj petehija), tronožac (nakon nanošenja manžeta prilikom mjerenja krvnog tlaka, gledanja na kožu - doći će do krvarenja), štipanja (štipanja kože).
thrombocytopathia:
trombocitopenija:
Verlgofova bolest (trombocitopenična purpura) nasljeđuje se autosomno dominantno. Manifestira se u obliku modrica, a cvatu - koža leoparda.
Sposobnost slezene da proizvodi inhibitor trombocitopoeze (faktor slezine) nasljeđuje se. Ovaj faktor inhibira povlačenje trombocita iz megakariocita u koštanoj srži, povećava se broj megakariocitova i ima malo smisla iz njih.
Liječiti: uklanjanje slezene.
Stečeno: NA TELEFONU FOTO!
Mijelotoksični učinci:
Egzogeni čimbenici: fizikalni (ionizirajuće zračenje), kemijski (citostatici, antibiotici, rafinirani proizvodi), biološki (virusi, toksini mikroorganizama).
endogenog:
Supstanca normalnih klica formiranja krvi.
Autoimuna trombocitopenija.
Rezultat - nazalno, gingivalno krvarenje, maternica, modrice.
Za razlikovanje postoji biološka analiza, bolesnikov serum ubrizgava se životinji. Faktor slezene nema specifičnost vrsta, stoga izaziva trombocitopeniju kod životinje.
Trombociti - kršenje funkcionalnih svojstava trombocita:
Nasljedna: Glantsmanova bolest, Willebrandova bolest (složena hemoragična dijateza, jer endotel obično stvara Willebrandov faktor, komponenta 8 faktora, a izobličena sinteza ovog faktora se nasljeđuje. Willebrandeov faktor je faktor koagulacije).
stečena:
Transfuzija velikih doza krvi, plazme, prokoagulantnih koncentrata.
Mijelom, Waldenstromova bolest (povećana u vrhuncu normalnih i abnormalnih proteina).
DVSS (povećani PDF - proizvodi degradacije fibrina)
Ljekovite - NSAID
Hipovitaminoza C, B 12.
Mehanizam trombocitoze:
Kršenje sinteze i nakupljanja u granulocitima biološki aktivnih tvari trombocita,
Kršenje degranulacije i oslobađanje faktora trombocita u krvnoj plazmi.
Dijagnoza trombocitopenije i astenije:
Broj trombocita: 180-400 * 10 9 / l.
Vrijeme sakupljanja trombocita: 14-18 sekundi
Postotak stanica koje su se pridružile agregaciji je više od 90.
Produljenje vremena i smanjenje stanica koje su ušle - trombocistin.
Konchalovskyov pozitivan test - trombociti određuju trofičnost vaskularnog endotela, emitiraju faktore rasta neophodne za endoteliocite. Ako su trombociti mali - oštećenja, povećava se krhkost žila.
Koagulopatija - poremećaj koagulacijske hemostaze:
Nasljedna. U fazama koagulacije:
Poremećaji faze koagulacije I:
Hemofilija A (80% sech hemofilia) je nedostatak faktora VIII.
Hemofilija B (10%) je nedostatak faktora IX.
Hemofilija C (5%) - nedostatak faktora XI.
Mehanizam nasljeđivanja hemofilije: hemofilija A je defekt X kromosoma. Zdrav otac, majka - nositelj: zdrav sin, zdrava kći, kći noseća, sin koji boluje od hemofilije. Bolest se manifestira odmah nakon rođenja, novorođenče može imati različita krvarenja (cefalhematoma). Svaka ozljeda dovodi do stvaranja hematoma (vrsta krvarenja). Možda je nastajanje hemarthrosis.
H i hemofilija B i C može se javiti i kod muškaraca i kod žena.
Dijagnoza kršenja koagulacije faze I:
Vrijeme aktiviranja plazme rekcifikacije (AVR) 40-60s.
Djelomično aktivirano vrijeme tromboplastina (APTT) 33-45 sec.
Poremećaji faze II:
Nasljedna (parahemofilija): hipoprothrombinemija, hipoprokonvertinemija, hipoproakcelerinemija.
Stečeno: zatajenje jetre, aholija, hipovitaminoza K.
Za procjenu stanja faze II procjenjujemo protrombinski indeks (PTI) od 85-110%.
Faza III poremećaj:
Nasljedne: hipofibrinogenemija, afibrinogenemija, disfibrinogenemija.
Stečena kao rezultat smanjenja sinteze ili povećane potrošnje (posebno kod DVSS): hipofibrinogenemija, afibrinogenemija.

PATOFIZIOLOGIJA HEMOSTASISNOG SUSTAVA
Vrijednost hemostatskog sustava
1. Očuvanje krvi u tekućem stanju (adekvatan omjer aktivnosti sustava koagulacije i antikoagulacije)
2. Spriječiti i zaustaviti krvarenje (održavanje konstantnog volumena cirkulirajuće krvi)

VRSTE HEMOSTASISA
Vaskularna krvnih
(Početno)
- ZAUSTAVLJANJE Krvarenja u MICRO brodovima
koagulacija
(Sekundarna)
FORMIRANJE FIBRINSKIH KUPCA

KOMPONENTE HEMOSTASTIČKOG SUSTAVA
* VASKULARNI ZID
* trombociti (monociti, eritrociti)
* PLASMA SUSTAVI:
- PROKOAGULYANTY
- ANTIKOAGULANTI
- FIBRINOLITIČKA
- KALLIKREIN-KININOVAYA

KLASIFIKACIJA POREMEĆAJA HEMOSTAZE
ZA ETIOLOGIJU
- HEREDITARNA
- OSVOJENO
ZA MEHANIZAM RAZVOJA
- VASKULARNI POREMEĆAJI
hemostaza
- RASPOREDI KOAGULATORNE HEMOSTASIJE
ZA SMJERU PROMJENE
- HIPOKOAGULACIJA
- HIPERCOAGULACIJA

gipokoagulyatsii
Smanjena sposobnost zgrušavanja krvi sa tendencijom ponovnog krvarenja i krvarenja (spontano ili nakon manjih ozljeda)

etiologija
1. THROMBOCYTOPIA
2. trombocitopatije
3. VASOPATIJA
4. COAGULOPATHY

trombocitopenija
Patološko stanje karakterizirano smanjenjem broja trombocita u krvi. (manje od 150 · 109 / l)

HEREDITARNA THROMBOCYTOPENIA
U pravilu, istodobno ga prate nenormalni defekti trombocita

POBOLJENE THROMBOCYTOPENIA (KLASIFIKACIJA POD MEHANIZmom RAZVOJA)
OŠTEĆENJE PLATELETA
- imunološki kompleksi
- mehanička trauma (splenomegalija, hemangiom)
PLOČENO FORMIRANJE PLATELETA
(aplastična anemija, kemijska i radijacijska oštećenja crvene koštane srži, zamjena hematopoetskog tkiva tumorima)
POVEĆANA UPOTREBA PLATELETA
(tromboza, DIC)

IMUNI THROMBOCYTOPIA
GETEROIMMUNNAYA
* Javlja se češće u djeca
** razlog - promjene u antigenskoj strukturi trombocita (tijekom propadanja rubeole, malih boginja, adenovirusnih virusa; hapteni koji potiču od lijeka - kinidin, sulfonamidi, rifampicin; cjepiva)
***Povoljan tečaj (ako se otkloni uzrok, dolazi do potpunog oporavka)

IMUNI THROMBOCYTOPIA
autoimuna
Javlja se češće u odrasli
razlog - nedostatak imunološke tolerancije na antigene vlastitih trombocita
Provokativni čimbenici: lijekovi, virusi, bakterije

Autoimuna trombocitopenija
BOLEST VERLOGOPA
(autoimuna kronična trombocitopenična purpura)
* Na površini trombocita Ig G povećava se 10 puta
* Glavno mjesto sinteze Ig G je slezena
* Princip liječenja:
- splenektomija
- kortikosteroidi
- imunosupresivi
* Ne postoji potpuno izlječenje.

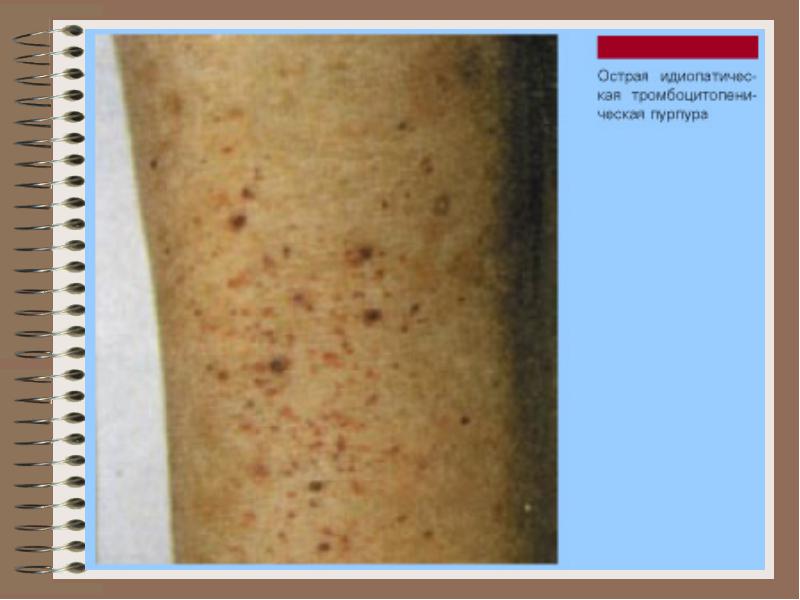
thrombocytopathy
Smanjena hemostaza zbog kvalitativne inferiornosti ili disfunkcije trombocita, što je karakterizirano kršenjem vaskularne trombocitne hemostaze, pojavom krvarenja tkiva i organa

BEZ KRŠENJA REAKCIJE LIBERACIJE GRANULESA
Glantsmanova trombasthenija
* Nasljeđivanje - autosomno recesivno
*razlog - odsutnost glikoproteina 2b i 3a u ljusci trombocita
*patogeneza- trombociti ne djeluju u interakciji s fibrinogenom i ne agregiraju se
*simptomi: petehije, krvarenja iz nosa, krvarenje iz maternice ( može biti smrtonosno !!)

Nasljedna trombocitopatija
SA KRŠENJEM GRANULE LIBERACIJSKA REAKCIJA
baština - autosomno recesivni
razlog - oslabljena aktivnost cikloksigenaze, niska kontraktilna aktivnost proteina
patogeneza - nedostatak agregacije pri interakciji s kolagenom, nedostatak oslobađanja granula
simptomi:

Nasljedna trombocitopatija
SA INFRENCIJOM I OBJAVLJIVANJE SADRŽAJA GRANULA
Herjman-Pudlak bolest (AR)
* razlog - kršenje nakupljanja gustih granula (ADP, adrenalin, serotonin, Ca2 +)
* patogeneza - nema agregacije u interakciji s kolagenom, nema otpuštanja sadržaja granula
* simptomi: petehije, krvarenje iz nosa, krvarenje iz maternice

Nasljedna trombocitopatija
DISTURBANCIJOM SASTAVLJANJA I PLATELETNE AGREGACIJE
Von Willebrand-Jurgens sindrom (AR)
razlog - Manjak Willebrandovog faktora
patogeneza - oslabljena je adhezija trombocita zbog nedostatka faktora 8
Bolest Bernarda Sul-a (AR)
razlog - nedostatak glikoproteina 1 na trombocitima
patogeneza - interakcija trombocita s von Willebrand-ovim faktorom, f. 5, f. 11
Znakovi - kapilarno krvarenje ( posebno opasno tijekom puberteta ili porođaja)

Nasljedna trombocitopatija
DEFICIENCIJA I SMANJENA DOSTUPNOST f.3
Trombocitopatija Bowe i Ovna
razlog - manjak f.3 trombocita
patogeneza - nema interakcije trombocita i prokoagulanata
simptomi: petehije, krvarenje iz nosa, krvarenje iz maternice

Nasljedna trombocitopatija
Trombocitopatija kombinirana s drugim nasljednim anomalijama
Whiskott-Aldridge sindrom
- razlog - u trombocitima ima nekoliko gustih granula (ADP, serotonin, adrenalin, Ca2 +), alfa granule (beta-tromboglobulin, fibrinogen, fibronektin, faktor rasta)
- patogeneza –Dominirana adhezija i agregacija trombocita, poremećeno oslobađanje granula
- simptomi:hemoragični sindrom javlja se rano, može doći do smrtnog krvarenja

Stečena trombocitopatija (etiologija)
1. leukemija- nekoliko granula u trombocitima zbog ubrzanog sazrijevanja, smanjenog prijanjanja i agregacije
2. Nagomilajte seIg M - oštećenje receptora od strane imunih kompleksa, kršenje interakcije trombocita i prokoagulansa (imunološke bolesti)
3. hypovitaminosis B12 - poremećeno oslobađanje granula
4. Učinci lijekova

Trombocitopatija lijekova
* I inhibitori sinteze tromboksana A2
steroidni protuupalni lijekovi
- nesteroidni protuupalni lijekovi (aspirin blokira agregaciju trombocita 4-6 dana)
* Obrazovni stimulatori cAMP
-papaverin
- eufilin
-anabolički steroidi
* Ca ion antagonisti
-verapamil
-korinfar

VAZOPATIYA
Hemoragična dijateza zbog funkcionalne i morfološke inferiornosti vaskularnog zida
- kongenitalni
- stečeno

HORN VASOPATHY
Bol. Randyou-Osler (hemoragična telengiektazija)
Bol. Fabry (difuzni angioker-toma debla)
Nasljedna trombocitopenična mikroangiomatoza

HORN VASOPATHY
razlog - nasljedno kršenje razvoja vezivnog tkiva, uključujući vaskularni subendotel
svojstvo
- fokalno vaskularno stanjivanje
- širenje lumena mikrovesela
- nekoliko kolagenih vlakana u subendotelijumu
- plovila su lako ozlijeđena
- slaba adhezija i agregacija trombocita zbog nedostatka kolagenih vlakana
**Znakovi - nazalno krvarenje, plućni bronhijalni i gastrointestinalni (postoje smrtni)

POBOLJENA VASOPATIJA
1. i diopaticheskaya (Kaposijev sarkom)
- etiologija - nepoznato
2. ustajao (dermatitis Klotza, dermatitis Favra Rakusho)
- etiologija - kronično zatajenje srca, lokalna venska insuficijencija
3. dystrophic
Steroidna purpura - hiperfunkcija nadbubrežne žlijezde, liječenje kortikosteroidima - inhibiraju sintezu kolagena
Spalching - manjak Vit.S
Bol.Shenlein-Genokha - oštećenje krvnih žila imunoloških kompleksa
4. neurogeni
Klinički znakovi - kožni oblici krvarenja

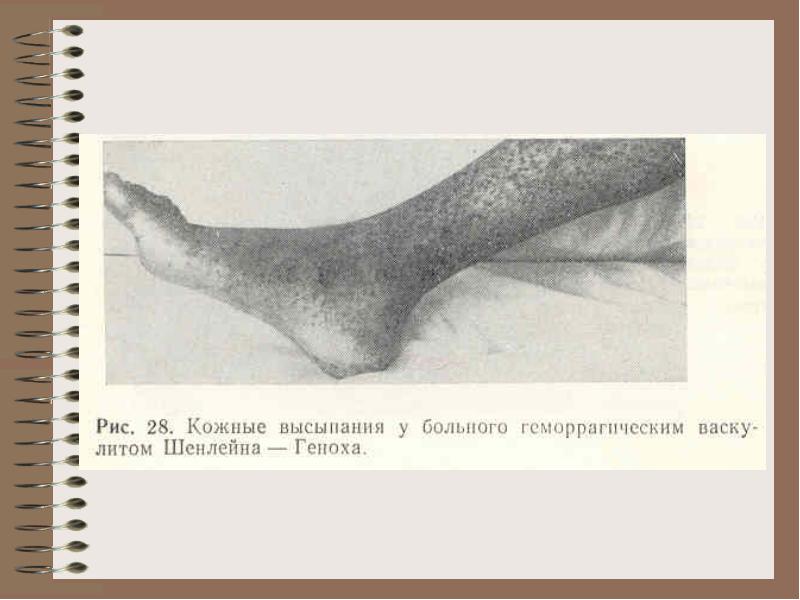
koagulopatija
Hemoragična dijateza, koja nastaje kao rezultat patologije koagulacijskog sustava hemostaze
** nasljedan
** stekao

Nasljedna koagulopatija
Genetski uzrokovan poremećaj koagulacije zbog nedostatka ili molekularne nepravilnosti tvari odgovornih za koagulacijsku hemostazu

Nasljedna koagulopatija
KLASIFIKACIJA
1. Koagulopatija zbog izoliranog kršenja unutarnjeg mehanizma stvaranja aktivnosti protrombinaze (hemofilija A, B, C, Willebrand b., Hageman-ov nedostatak)
2. Koagulopatija zbog izoliranog kršenja vanjskog mehanizma stvaranja aktivnosti protrombinaze (hipoprokonvertinemija - nedostatak 7 l.)
3. Kombinirano kršenje vanjskog i unutarnjeg mehanizma stvaranja aktivnosti protrombinaze (parahemofilija - nedostatak 5 lb., b.Steuart-Prouer - manjak od 10 lb.)
4. Kršenje završnog stadija koagulacije krvi (afibrinogenemija)

STATISTIKA
Među svim oblicima koagulopatije pate:
Hemofilija A 68 - 78%
B , Willebrand 9 - 18%
Hemofilija B 6 - 13%
Hemofilija C, parahemofilija i hipoprokonvertinemija 1 - 2%
Preostali oblici - klinička kazuistika

Hemofilija A
Hemoragična dijateza zbog nasljednog nedostatka prokoagulantnog dijela faktora 8
Faktor 8 (visoko molekularna bjelančevina)
1. Prokoagulans glikoproteina (VIII: K)
2. Glikoprotein koji vrši adheziju trombocita (VIII: FV)
3. Glikoprotein koji aktivira adheziju trombocita pod utjecajem ristomicina (VIII: Rkoff)
4. Antigeni marker VIII: K (VIII: K AG)
5. Antigeni marker VIII: Rkof (VIII: Rkof AG)
Aktivnost VIII: K i VIII: PV opada s opadanjem multimerne strukture i samo 8 čimbenika

Hemofilija A
* Uh tiologiya - anomalija gena u X kromosomu koji kontrolira sintezu prokoagulantni dio f. 8 (Viii: k)
** Bolesti - muškarci (46, XhY)
** vrste
- Hemofilija A + (antigen-pozitivni oblik - sintetizira se nepravilno VIII: K), Pate od 8–10%
- Hemofilija A- (antigen-negativni oblik - ne sintetizira se VIII: K), pate 90–92%
**** klinika: krvarenja u velikim zglobovima, hematomi (potkožni, intramuskularni), teška i produljena posttraumatska krvarenja. Moguće krvarenje u trbušnim organima, krvarenje u probavnom sustavu

hemofilija
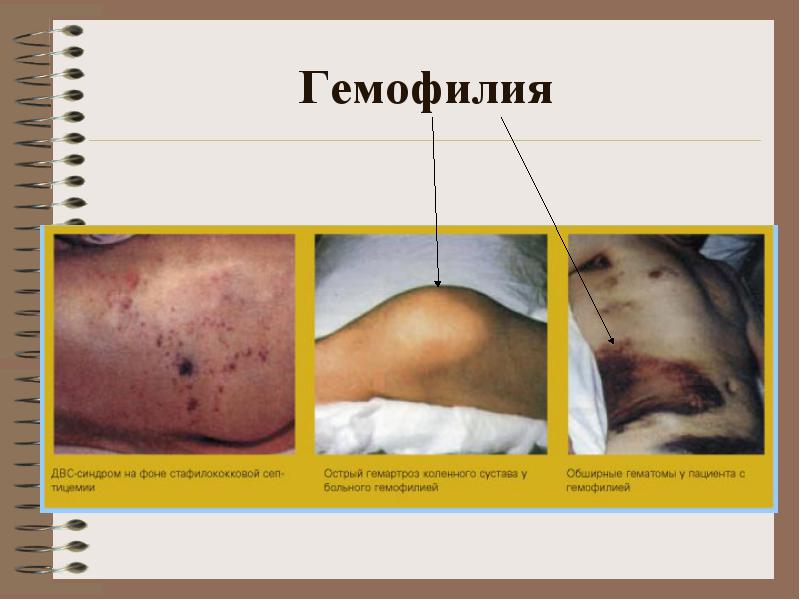
hemofilija
Hemofilija B
etiologija - anomalija gena u X kromosomu koji kontrolira sintezu f. 9
Bolesni - muškarci (46, XhY)
- žene (46, XhXh), (45, Xh O)
*** Prikazi
- Hemofilija B + (antigen-pozitivni oblik - sintetizira se anomalan f. 9)
- Hemofilija B- (antigen-negativni oblik - ne sintetizira se f. 9)
klinika: krvarenja u velikim zglobovima, hematomi (potkožni, intramuskularni), teška i produljena posttraumatska krvarenja. Moguće krvarenje u trbušnim organima, krvarenje u probavnom sustavu

POBOLJENA KOAGULOPATIJA
svojstvo - polideficijent
etiologija
1. Imunološka inhibicija prokoagulansa (rezusni sukob)
2. Nedostatak vit. K-ovisni faktori koagulacije (7, 10, 9, 2)
a) oslabljena sinteza u crijevima (disbakterioza, proliv)
b) kršenje apsorpcije vit. K (nedostatak žuči)
c) teška oštećenja jetre
3. Predoziranje heparinom

Hiperkoagulabilno
POVEĆAN KAPACITET KRVI ZA FORMIRANJE KRVI U PLOVILIMA
tromboza
ICE SINDROM

DIC-SINDROM (SINDROM DEKOMINIRANE INTRA-VASKULARNE Zgrušavanja krvi)
KLASIFIKACIJA
* Prema kliničkom tečaju
1) akutni (trenutni oblici karakteriziraju teški tijek)
2) kronični
* Po prevalenciji
1) lokaliziran
2) generalizirani

etiologija
Infekcije, septička stanja
šok (sa septičkom stopom - smrtnost od 100%)
Kirurške intervencije, opekline
Sva terminalna stanja, srčani zastoj
Akutna intravaskularna hemoliza
Akušerska patologija (20-25%)
Hemoblastoza (s o. Leukemijom - 33-45%)
Destruktivni procesi u parenhimskim organima
Alergijske reakcije

Faze DIC-a
1) Hiperkoagulacija (stvaranje više krvnih ugrušaka zbog aktiviranja koagulacijskog sustava)
2) Potrošnja koagulopatija (iscrpljivanje sustava koagulante, prekomjerna upotreba trombocita za stvaranje tromba)
3) Hipokoagulacija (pad aktivnosti koagulanata, aktiviranje antikoagulansa, aktivacija fibrinolize)
4) Završetak (oporavak, komplikacije, smrt)

Patogeneza DIC-a
1) hyperthrombinemia (tromboplastin ulazi u krv u velikim količinama iz oštećenih tkiva i potiče stvaranje trombina). Kod infekcija aktivirani monocitni makrofagi sintetiziraju vlastite koagulanse (f.7, f.10, f.9, f.2)

Patogeneza DIC-a
2) Masivna agregacija trombocita (uzrokuje razvoj potrošnje trombocitopenije nii i komplicirane krvarenjima)
3) Trauma i hemoliza eritrocita (ovo stvara puno ADP-a, što povećava prianjanje i agregaciju trombocita)

Patogeneza DIC-a
4) "Eksplozija humoralne proteaze" (kada se aktiviraju prokoagulanti, antikoagulansi, fibrinolitikov, proteini kallikrein-kinin sustava, sustav komplementa u krvi akumulira mnoge proizvode propadanja proteina, koji su vrlo toksični i oštećuju krvne žile i tkiva)

Patogeneza DIC-a
5) Iscrpljivanje sustava fibrino-leasinga
(doprinosi trombozi)
6) Iscrpljivanje faktora zgrušavanja krvi
(uzrokovati razvoj krvarenja)

Klinika DIC-a
1. Hemokoagulacijski šok
razlog
* oslabljena mikrocirkulacija (uzrokuje razvoj hipoksije tkiva)
* nakupljanje toksičnih produkata proteolize
manifestacije
* snižavanje krvnog tlaka
* snižavanje centralnog venskog pritiska
* krvarenje (izaziva hemoragični šok)

Klinika DIC-a
2. Hemostatski poremećaji
a) hiperkoagulacija
Glavna manifestacija je tromboza.
Krv se zgrušava in vitro
b) hypocoagulation
Glavna manifestacija je krvarenje.
(istodobno se sustav fibrinolize iscrpljuje)

Klinika DIC-a
3. trombocitopenija
Nastaje zbog stvaranja velikog broja krvnih ugrušaka u žilama (potrošnja trombocitopenije)

Djevojka nakon što je pretrpjela grlobolju pojavila se petehijalni osip na koži ekstremiteta i debla. Objektivno: broj trombocita 80 G / l, antitrombocitna antitijela. Koje su alergijske reakcije (prema Coombsu i Jelli) osnova ove bolesti?
@ II tip (humoralni citotoksični)
Tip I (anafilaktički)
Tip III (imunokompleks)
V tip (stimulativno)
Pacijentica trombocita trombocita na kolagen je oslabljena i opaža se krvarenje iz malih žila. Kršenje koje se veze hemostaza može tolerirati kod pacijenta?
@Vaskularni trombociti
Koagulacija i faza
Faza koagulacije III
fibrinolize
Faza koagulacije II
Pacijentu je dijagnosticirana trombocitopenija. Koje su kliničke manifestacije tipične za poremećaje hemostaze trombocita?
@ Petehije, ekhimoza (modrice)
hemarthrosises
hematom
Skraćeno vrijeme krvarenja
Povećano vrijeme zgrušavanja krvi
Pacijent je tijekom pregleda utvrdio trombocitopatiju. Navedite koja promjena igra važnu ulogu u patogenezi trombocitopatije?
@ Proizvodnja patoloških trombocita iz koštane srži
Smanjena antikoagulacijska aktivnost
Hiperaktivacija trombocitopoeze
Povećana koncentracija prokoagulansa u krvi
Inhibicija fibrinolize.
Prije operacije, ustanovljeno je da je osobi došlo do krvarenja povećanih na 10 minuta. Koji nedostatak formiranih elemenata u sastavu krvi može uzrokovati takve promjene?
@ Broj trombocita
Crvene krvne stanice
monociti
limfociti
Broj bijelih krvnih zrnaca
U bolesnika je dugotrajna primjena aspirina uzrokovala krvarenja. Cilj: trombocitopenija s oštećenom funkcionalnom aktivnošću trombocita. Trombocitopatija u ovom slučaju je uzrokovana inhibicijom aktivnosti:
@ Ciklo-oksigenaza
Citokrom oksidaza
lipoksigenzaza
Superoksid dismutaza
Fosfolipaza A 2.
Pacijentu je dijagnosticirano smanjenje vaskularnog endotelija vaskularnog endotela von Willebranda. Koja je kršenja hemostaze krvnih žila uočena u ovom slučaju?
@ Kršenje adhezije trombocita
Poremećaj agregacije trombocita
Hiperkoagulabilno
Kršenje polimerizacije fibrina
Jačanje fibrinolize
Djetetu s hemoragičnim osipom koji se razvio nakon akutnih respiratornih virusnih infekcija dijagnosticiran je hemoragični vaskulitis (Shenlein-Henoch-ova bolest). Koje su alergijske reakcije (prema Coombsu i Jelli) osnova ove bolesti?
Tip III (imunokompleks)
Tip I (anafilaktički)
Tip II (humoralni citotoksični)
Tip IV (stanični citotoksični)
V tip (stimulativno)
Djetetu s hemoragičnim osipom koji se razvio nakon akutnih respiratornih virusnih infekcija dijagnosticiran je hemoragični vaskulitis (Shenlein-Henoch-ova bolest). Što uzrokuje poremećaje hemostaze kod ove bolesti?
@ Oštećenja vaskularnog zida
Nasljedna oštećenja vezivnog tkiva vaskularne stijenke
Nasljedna manjka antikoagulansa
Inhibicija fibrinolize
Nasljedni nedostatak prokoagulansa
Žena koja boluje od žučne bolesti ima hemoragični sindrom uzrokovan nedostatkom vitamina K. Koji od sljedećih čimbenika nije adekvatan za hipovitaminozu K?
@ Stuart - Prouer (f. X)
Von Willebrand faktor
Fibrinstabiliziranje (f. XIII)
Fibrinogen (f. I)
Trombofilija (ubrzanje zgrušavanja krvi) pronađena je kod pacijenta tijekom pregleda. Što bi moglo uzrokovati kršenje pravila?
@ Nedostatak inhibitora proteolitičkih enzima
Povećana koncentracija prostaciklina
Smanjena koncentracija trombina u krvi
Povećana razina heparina u krvi
Povećanje koncentracije fibrinolizina u krvi
Pacijent s jetrenom bolešću ima smanjenje količine protrombina u krvi. Ovo će prije dovesti do kršenja:
@ Druga faza koagulacijske hemostaze
fibrinolize
Treća faza koagulacijske hemostaze
Hemostaza krvnih žila
Prva faza koagulacijske hemostaze
Dječak star 7 godina, nakon pada sa bicikla, pojavio se hemarthrosis koljena. Uvođenje krioprecipitata i ispumpavanje krvi iz zgloba dovelo je do značajnog poboljšanja stanja djeteta. O kojoj bolesti trebam razmišljati?
@Hemofilija A
Hemoragični vaskulitis.
thrombocytopathy
trombocitopenija
Reumatoidni artritis
Dječak s izraženim hemoragijskim sindromom u krvnoj plazmi nema antihemofilijski globulin A (faktor VIII). Koja je primarna faza hemostaze kod ovog djeteta?
@ Unutrašnji put aktivacije protrombinaze
Uvlačenje krvnog ugruška
Aktivacija vanjske staze protrombinaze
Dječak boluje od hemofilije. Koji su klinički znakovi oštećenja koagulacijske hemostaze?
Petehijalno krvarenje
microhematuria
Ekhimoza (modrice)
Oštrina vida
@ Hematomi, dugotrajno krvarenje
Žrtva nesreće neko vrijeme nakon pretrpljenog politrauma razvila je sindrom diseminirane intravaskularne koagulacije (DIC). Koji je faktor bio pokretač ove komplikacije?
@ Tromboplastin tkiva (f. III)
Fibrinogen (f. I)
Antihemofilni globulin A (f. VIII)
Pacijent s akutnim pankreatitisom razvio je diseminirani intravaskularni koagulacijski sindrom (DIC). Koja je tvar bila pokretač ove komplikacije?
@ Trypsin
Fibrinogen (f. I)
Antihemofilni globulin A (f. VIII)
Stuart Faktor - Prouer (f. X)
Antihemofilni globulin B (f. IX)
U bolesnika s politraumom i akutnim zatajenjem bubrega, stanje je bilo komplicirano unutarnjim krvarenjem. Koja je glavna poveznica u patogenezi ove faze DIC-a?
@ Potrošnja čimbenika zgrušavanja krvi
Oslobađanje leukocita iz skladišta
trombocitoza
Aktivacija protrombinaze
Inhibicija fibrinolize
Pacijent s opeklinom razvio je DIC sindrom kao komplikaciju. U koji se stadij DIC sindroma može posumnjati ako se zna da se pacijentova krv koagulira u manje od 3 minute?
'Hiperkoagulabilno
gipokoagulyatsii
oporavak
latentno
terminal
Pacijent s ozljedom razvio je DIC - sindrom. Koje se promjene u hemostazi primjećuju u drugoj fazi sindroma DIC-a?
'Hypocoagulation
Hypercoagulation.
fibrinolize
trombocitopenija
thrombocytopathy
Pacijentica nakon transfuzije nekompatibilne krvi imala je DIC - sindrom. Koja je glavna poveznica u patogenezi ove komplikacije u hemolizi?
@ Unos intracelularnih proteaza u krv
Akumulacija bilirubina u krvi
Višak tromboplastina u krvi
Višak protrombina u krvi
Povećanje sadržaja plazminogena
Pacijent s kroničnim zatajenjem bubrega razvio je DIC. Ispitivanjem je utvrđeno povećanje vremena zgrušavanja krvi, trombocitopenija, povećana razina kompleksa fibrin - monomera i produkata razgradnje fibrina. O kojoj fazi DIC-a treba razmišljati?
'gipokoagulyatsii
Hiperkoagulabilno
oporavak
latentno
nestabilan
Pacijent s kroničnom limfocitnom leukemijom razvio je krvarenja kao rezultat razvoja DIC sindroma. Koje će se promjene u perifernoj krvi primijetiti?
@ Hipokoagulacija, trombocitopenija
Eritrocitoza, povećana viskoznost krvi
Trombocitoza, skraćeno vrijeme zgrušavanja krvi
Hiperkoagulacija, povećana agregacija trombocita
Povećana je aktivnost prokoagulanta
Žena sa sepsom razvila je petehijalna krvarenja, smanjila broj trombocita i fibrinogena u krvi i pojavili se produkti razgradnje fibrina. Što bi mogao biti uzrok značajnih promjena?
@DIC sindrom
leukopenija
limfopenija
trombocitoza
 Novi znak zodijaka - Ophiuchus
Novi znak zodijaka - Ophiuchus Pismo na engleskom 10 rečenica
Pismo na engleskom 10 rečenica Fraze prijateljstva i kako ih koristiti na engleskom
Fraze prijateljstva i kako ih koristiti na engleskom